Желтуха новорожденных: лечить или не лечить
Желтуха у взрослых и детей старшего возраста всегда ассоциируется с опасным заболеванием. И это действительно так. А с чем связано появление желтухи у новорожденного? О том, что это за состояние, в каких случаях оно может стать опасным для новорожденного и на что стоит обратить внимание родителям, мы расспросили заведующую отделением стационарозамещающих технологий ФГАУ «НМИЦ здоровья детей» Минздрава России неонатолога Елену Зимину.
Что такое желтуха новорожденных (ЖН) и почему она возникает
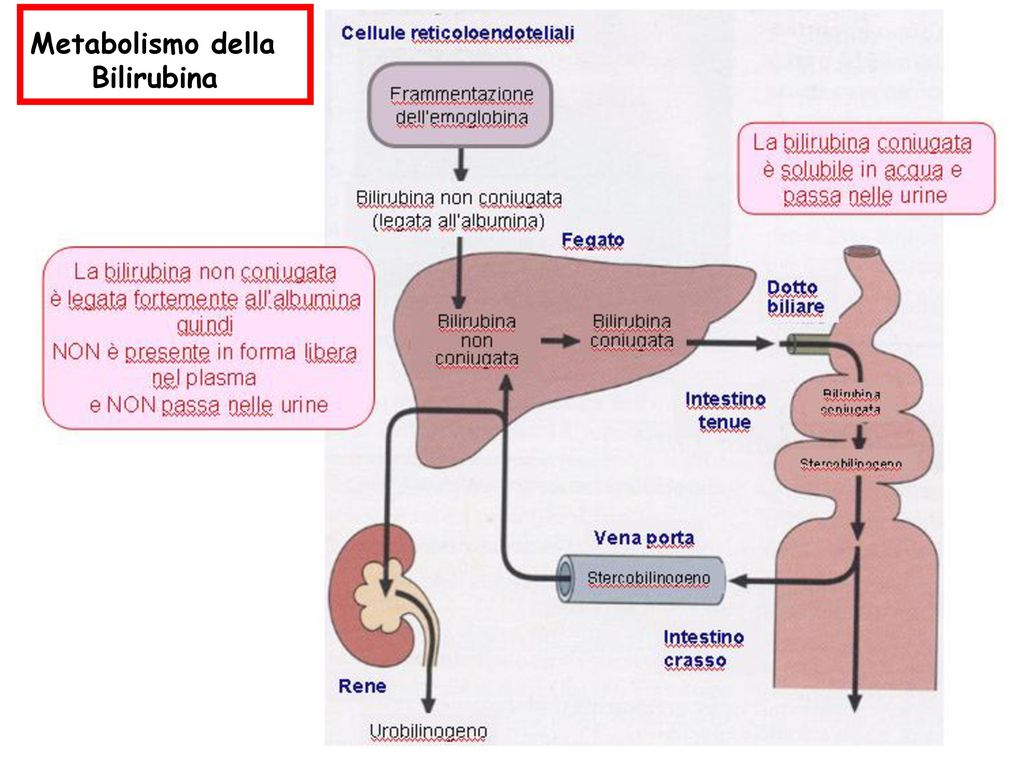
Это состояние ребенка в периоде новорожденности. Оно характеризуется желтушностью кожи и склер из-за избыточного накопления билирубина в организме. У детей в возрасте до 1 месяца совершенствуется пищеварительная система. В костном мозге и кроветворной системе происходят специфические процессы: разрушается фетальный гемоглобин и образуется так называемый взрослый гемоглобин. Один из продуктов распада — желчный продукт билирубин. Он накапливается в крови и окрашивает кожу в желтый цвет. В большинстве случаев ЖН протекает физиологично и возникает по причине незрелости ферментных систем новорожденного.
Он накапливается в крови и окрашивает кожу в желтый цвет. В большинстве случаев ЖН протекает физиологично и возникает по причине незрелости ферментных систем новорожденного.
Какие бывают виды ЖН
Физиологическая желтуха встречается у большинства малышей и появляется после 36 часов жизни. Это состояние — не болезнь и со временем проходит. Она убывает к 14 дню жизни у доношенного новорожденного и к 21 дню у недоношенного ребенка.
Желтуха, проявившаяся в первые 24 часа после рождения, — всегда признак патологии.
Патологическая желтуха — это, как правило, признак каких-либо других заболеваний. Она требует лечения, которое назначает врач. При очень сильном повышении уровня билирубина происходит его проникновение в нервную систему. Это может оказать токсическое действие, в первую очередь на жизненно важные нервные центры, головной мозг.
Такое состояние называют «ядерной желтухой», или «билирубиновой энцефалопатией». Высокий уровень билирубина может вызвать повреждение центральной нервной системы (ЦНС): заторможенность, сонливость, вялость, угнетение сосательного рефлекса — на ранней стадии. В промежуточной стадии — повышение мышечного тонуса, повышенную раздражительность, нередко повышение температуры тела. В развернутой стадии — поражение ЦНС: судороги, нарушение дыхания, кома. Ядерная желтуха необратимо поражает ЦНС, возникает потеря слуха, паралич взора, отставание в умственном развитии, детский церебральный паралич.
В промежуточной стадии — повышение мышечного тонуса, повышенную раздражительность, нередко повышение температуры тела. В развернутой стадии — поражение ЦНС: судороги, нарушение дыхания, кома. Ядерная желтуха необратимо поражает ЦНС, возникает потеря слуха, паралич взора, отставание в умственном развитии, детский церебральный паралич.
Специалисты отмечают:
- раннюю желтуху — проявляется в первые 36 часов жизни;
- затяжную желтуху — сохраняется более 14 дней у доношенных новорожденных и более 21 дня у недоношенных новорожденных;
- позднюю желтуху — проявляется после 7 дня жизни.
По каким факторам оценивается тяжесть желтухи
При осмотре новорожденного врачи оценивают: цвет кожных покровов, склер, слизистых оболочек, этапность проявления желтушного окрашивания (по шкале Крамера), время проявления желтухи, общее состояние новорожденного (степень активности, выраженность рефлексов, частоту мочеиспускания и характер мочи, размеры печени и селезенки, адекватность грудного вскармливания, лабораторные показатели).
Факторы риска для новорожденных
1. Рождение новорожденного ранее 38 недель гестации.
2. Наличие гипербилирубинемии у предыдущего ребенка в семье.
3. Проявление желтухи в первые 24 часа жизни.
Как влияет резус-фактор на появление и проявления ЖН
Несовместимость по резус-фактору матери и еще не рожденного малыша может спровоцировать резус-конфликт, что после рождения проявляется как гемолитическая болезнь новорожденных.
Женский организм с отрицательным резусом определяет положительный резус-белок молодого организма как чужеродный. При этом выделяются иммунные клетки — антитела.
Антитела разрушают эритроциты младенца, происходит высвобождение высокого уровня билирубина, который тяжело поражает ЦНС молодого организма. Желтуха, связанная с резус-конфликтом по группе крови матери и ребенка, обычно определяется в первые дни жизни ребенка.
Профилактика
Для того чтобы малыш рос крепким и здоровым, будущей маме нужно соблюдать здоровый образ жизни во время беременности. Если у женщины отрицательный резус-фактор, ей необходимо максимально полно проинформировать врача о возможных предыдущих беременностях, абортах, переливаниях крови и операциях. Кроме того, важно определить у беременной женщины уровень резус-антител и провести иммунологическое обследование будущего отца. После появления ребенка на свет крайне необходимо поддерживать адекватное естественное вскармливание.
Если у женщины отрицательный резус-фактор, ей необходимо максимально полно проинформировать врача о возможных предыдущих беременностях, абортах, переливаниях крови и операциях. Кроме того, важно определить у беременной женщины уровень резус-антител и провести иммунологическое обследование будущего отца. После появления ребенка на свет крайне необходимо поддерживать адекватное естественное вскармливание.
Лечение
Определить, опасна или не опасна желтуха для ребенка, сможет врач по уровню билирубина в крови младенца. Это позволит выработать тактику лечения и понять, нужна ли ребенку помощь специалиста или надо просто выждать время.
Один из методов лечения желтухи у новорожденных — фототерапия. Это лампы синего цвета с определенным типом волны, которые не опасны для ребенка. Они помогают билирубину разрушиться и быстрее выйти из организма.
Билирубин из организма выходит со стулом. Когда процесс дефекации у ребенка проходит регулярно и в достаточном объеме, то и уровень билирубина падает довольно быстро.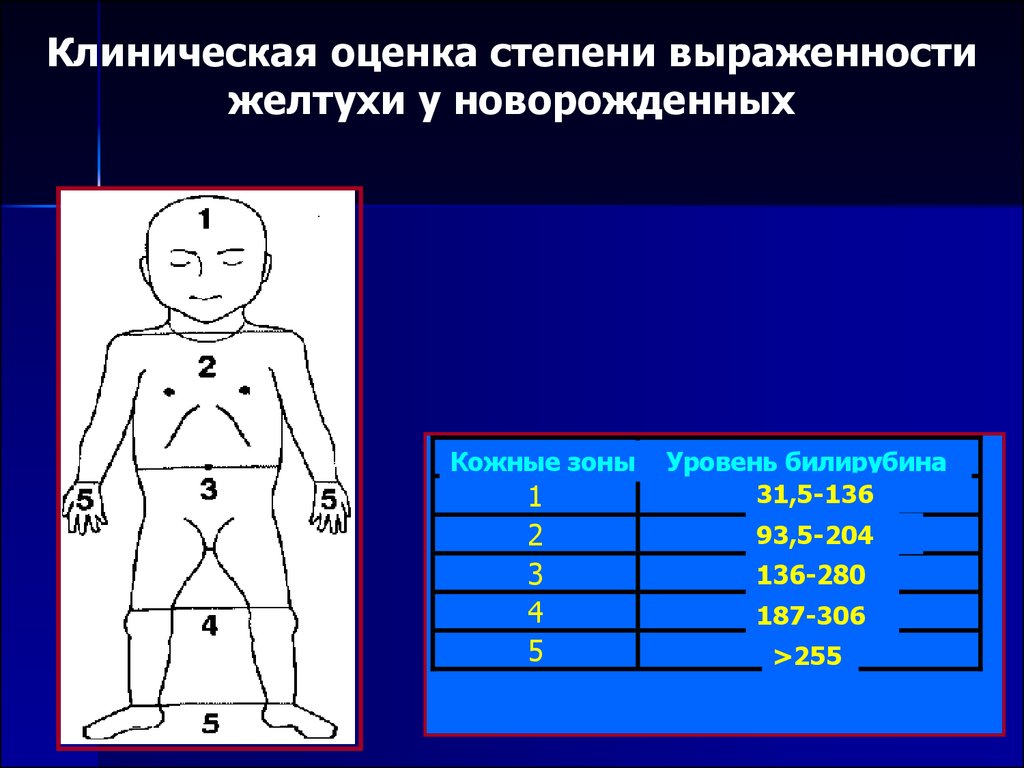 Если стул не регулярен, есть запоры, тогда необходимо принимать меры.
Если стул не регулярен, есть запоры, тогда необходимо принимать меры.
Советы родителям: как реагировать
1. Не паниковать, так как ЖН — физиологическое состояние новорожденного, которое в большинстве случаев не оказывает вредного воздействия на организм ребенка.
2. При появлении признаков желтухи у новорожденного (желтушное окрашивание кожи, склер, слизистых оболочек) необходимо обратиться к медицинским работникам.
Если признаки желтухи проявились в первые сутки жизни ребенка — обратиться к медицинскому персоналу немедленно!
3. Сообщить медикам следующую информацию: были ли желтухи у предыдущих детей, на каком сроке рожден ребенок, на каком вскармливании находится, охарактеризовать цвет стула и мочи младенца.
4. При сохранении желтухи у ребенка более 14 дней у доношенного и более 21 дня у недоношенного ребенка необходимы осмотр врача и обследование.
Беседовала Анна Демина
Фото: Коллекция/iStock
желтухи у новорождённых:задачи и тесты
Ситуационные задачи и тесты по теме «Желтухи у новорожденных и детей раннего возраста»
Задача N 1
Девочка О. , 4 дней, находится в родильном доме.
, 4 дней, находится в родильном доме.
Из анамнеза известно, что ребенок от первой беременности, протекавшей с токсикозом в 1-й половине. Роды срочные. Масса тела при рождении 3100 г, длина тела 51 см. Оценка по шкале Апгар 8/9 баллов. Закричала сразу, к груди приложена через два часа после рождения, сосала хорошо. На 3-й сутки появилась иктеричность кожных покровов.
При осмотре на 4-й день жизни состояние удовлетворительное, сосет хорошо, крик громкий. Кожные покровы чистые, умеренно иктеричны, пупочная ранка чистая. В легких дыхание пуэрильное, сердечные тоны звучные, живот мягкий, печень выступает из-под края реберной дуги на 1 см, селезенка не пальпируется. Стул желтого цвета. Физиологические рефлексы вызываются, мышечный тонус удовлетворительный.
Группа крови матери А(П) Rh-положительная.
Общий анализ крови: Нb- 196 г/л, Эр — 5,9х1012/л, ретикулоциты -1,5%, Ц.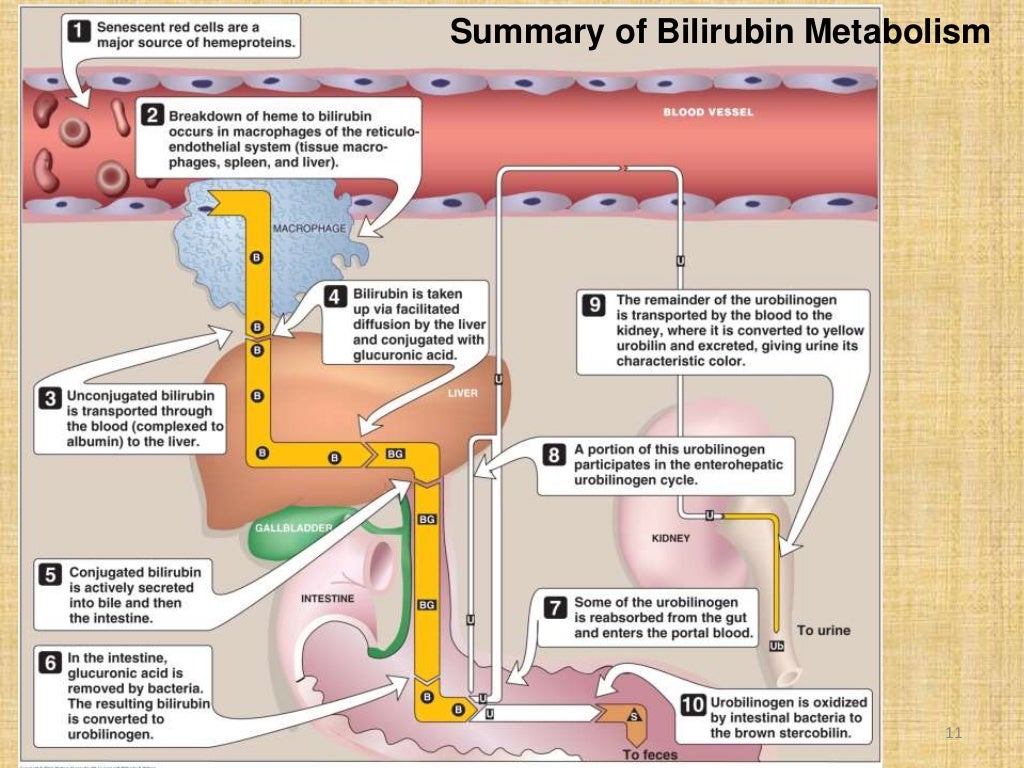 п. — 0,94, Лейк — 9,0х109/л, п/я — 5%, с — 42%, э — 1%, л — 47%, м -5%, СОЭ — 2 мм/час.
п. — 0,94, Лейк — 9,0х109/л, п/я — 5%, с — 42%, э — 1%, л — 47%, м -5%, СОЭ — 2 мм/час.
Общий анализ мочи: цвет — соломенно-желтый, реакция — кислая, удельный вес — 1004, белок отсутствует, эпителий плоский — немного, лейкоциты — 2-3 в п/з, эритроциты — нет, цилиндры — нет.
Биохимический анализ крови на 4-й день жизни: общий белок -52,4 г/л, билирубин: непрямой — 140 мкмоль/л, прямой — нет, мочевина -4,2 ммоль/л, холестерин — 3,6 ммоль/л, калий — 5,1 ммоль/л, натрий -141 ммоль/л, АЛТ — 25 ммоль/л, ACT -18 ммоль/л.
Задание
- Поставьте диагноз.
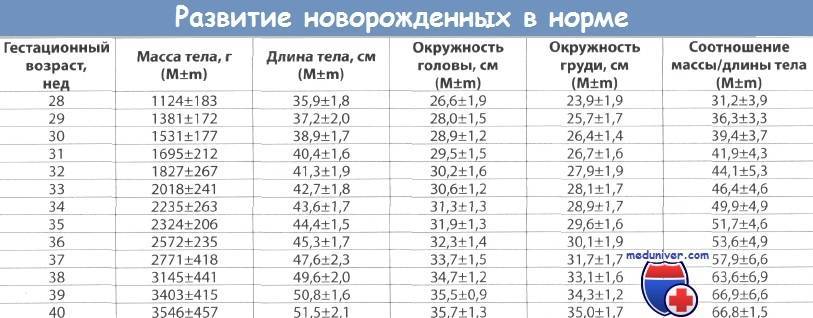
- Как Вы оцениваете массо-ростовой показатель при рождении?
- Оцените результаты общего анализа крови.
- Оцените результаты общего анализа мочи.
- Оцените результаты биохимического анализа крови. С чем связаны выявленные изменения?
- Расскажите об особенностях обмена билирубина у новорожденного.
7. Возможно ли развитие гемолитической болезни новорожденного в данном случае?
Возможно ли развитие гемолитической болезни новорожденного в данном случае?
- Каков генез желтухи в данном случае?
- Проведите дифференциальный диагноз конъюгационной и гемолитической желтухи у новорожденного.
10. При каких клинических синдромах новорожденного с желтухой следует показать невропатологу?
11.При каких цифрах непрямого билирубина новорожденному с желтухой необходимо сделать заменное переливание крови?
12.Требует ли лечения желтуха у данного ребенка?
13.Как кормить этого ребенка?
14.Каков прогноз для этого ребенка?
Задача 2
Мальчик Г., 1 суток жизни, находится в родильном доме.
Из анамнеза известно, что матери 25 лет, она имеет А(II) Rh-отрицательную группу крови. Первая беременность была 3 года назад, закончилась медицинским абортом при сроке 9 недель, осложнений не было.
Настоящая беременность вторая, протекала с токсикозом в первом триместре, в третьем триместре периодически отмечались подъемы АД до 145/90 мм рт. ст. В женской консультации наблюдалась нерегулярно. Роды срочные, самостоятельные. 1-й период — 6 часов 30 минут, 2-й — 25 минут, безводный промежуток — 3 часа. Масса тела при рождении 3300 г, длина тела 51 см. Оценка по шкале Апгар 7/8 баллов. Сразу при рождении было отмечено желтушное прокрашивание кожных покровов, оболочек пуповины и околоплодных вод.
ст. В женской консультации наблюдалась нерегулярно. Роды срочные, самостоятельные. 1-й период — 6 часов 30 минут, 2-й — 25 минут, безводный промежуток — 3 часа. Масса тела при рождении 3300 г, длина тела 51 см. Оценка по шкале Апгар 7/8 баллов. Сразу при рождении было отмечено желтушное прокрашивание кожных покровов, оболочек пуповины и околоплодных вод.
При первом осмотре педиатра выявлено увеличение размеров печени до +3 см и селезенки до +1,5 см.
При дополнительном обследовании:
билирубин пуповинной крови составил 105 мкмоль/л.
В биохимическом анализе крови новорожденного, взятом в возрасте 4 часов жизни, уровень непрямого билирубина составил 175 мкмоль/л.
Hb периферической крови, определенный по cito, 149 г/л. в первые сутки
Задание
1. О каком заболевании с большей вероятностью можно думать в данном случае?
2. Оцените результаты исследования, проведенного новорожденному в родильном доме.
3. Какое обследование следует провести ребенку для уточнения диагноза?
4. Каков патогенез настоящего заболевания?
5. Какие группы крови Вы знаете?
7. Назначьте и обоснуйте лечение.
8. Какие ранние и поздние осложнения могут возникнуть при данном заболевании?
9. Можно ли было предупредить возникновение данного заболевания?
10. Как должен наблюдаться участковым педиатром этот ребенок после выписки?
В наблюдении, каких специалистов будет нуждаться ребенок в дальнейшем?
Задача N 3
Мальчик А., 4 дней, поступил в отделение патологии новорожденных из родильного дома по поводу выраженной желтухи.
Из анамнеза известно, что ребенок от женщины 23 лет, имеющей 0(1) Rh-отрицательную группу крови. Отец ребенка имеет А(П) Rli-отрицательную групп}’ крови.
Первая беременность закончилась медицинским абортом при сроке 10 недель.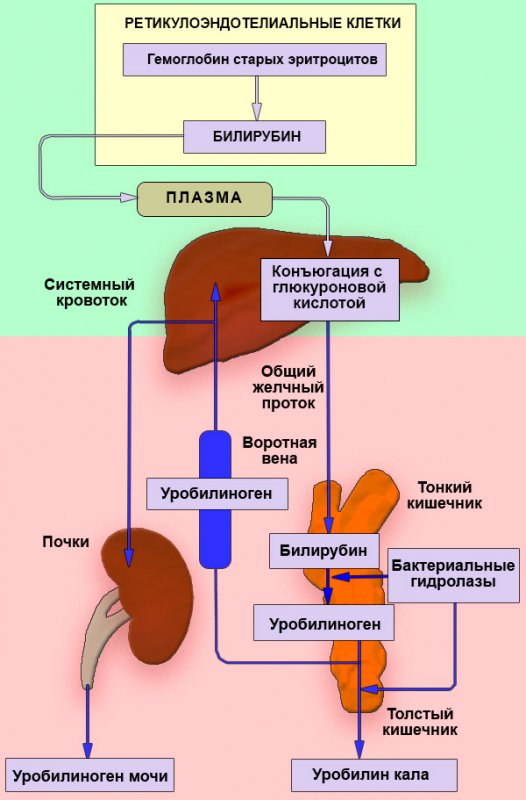 Настоящая беременность вторая, протекала с гестозом во второй половине. Роды срочные. Масса тела при рождении 3200 г, длина тела 52 см. Закричал сразу, крик громкий. К концу первых суток отмечена ик-теричность кожных покровов и склер. На вторые сутки желтуха усилилась.
Настоящая беременность вторая, протекала с гестозом во второй половине. Роды срочные. Масса тела при рождении 3200 г, длина тела 52 см. Закричал сразу, крик громкий. К концу первых суток отмечена ик-теричность кожных покровов и склер. На вторые сутки желтуха усилилась.
При поступлении в стационар состояние тяжелое, выраженная иктеричность кожных покровов и склер, ребенок вялый, отмечается мышечная
гипотония, гипорефлексия. Печень выступает из-под края реберной дуги на 2,5 см, селезенка у реберного края. Стул переходный.
Общий анализ крови: НЪ — 141 г/л, Эр — 3,9хЮ12/л, Ц.п. — 0,99, Лейк -9,4х109/л, п/я — 7%, с — 53%, э -1%, л — 32%, м — 7%, СОЭ — 2 мм/час.
Биохимический анализ крови на 2-й день жизни: общий белок -54,4 г/л, билирубин: непрямой — 180 мкмоль/л, прямой — нет.
Задание
- Поставьте и обоснуйте диагноз.
2. Какие обследования надо провести дополнительно для уточнения диагноза?
- Каковы возможные результаты дополнительного обследования?
- Каков патогенез выявленных клинических симптомов?
- Какие изменения могут быть выявлены при осмотре невропатолога?
- Какие результаты могут быть получены при УЗИ органов брюшной полости?
- С какими заболеваниями следует проводить дифференциальный диагноз в данном случае?
- Как следует кормить этого ребенка?
- Назначьте лечение.

10.Какие группы крови Вы знаете?
11.Чем следует делать заменное переливание крови в случае его необходимости? Как выбрать группу крови и Rh-фактор?
12.Может ли данный ребенок быть вакцинирован БЦЖ и когда?
13.Как следует наблюдать за ребенком после выписки из стационара?
14.К какой группе здоровья следует отнести данного ребенка после выздоровления?
Задача № 4
Девочка В., 5 дней, находится в родильном доме.
Из анамнеза известно, что матери 21 год, она имеет 0(1) Rh-отрицательную группу крови. Первая беременность закончилась родами 2 года назад, ребенок здоров, имеет 0(1) Rh-отрицательную группу крови. Настоящая беременность вторая, протекала с отеками на ногах в третьем триместре. Роды срочные. 1-й период 6 часов 30 минут, 2-й — 20 минут, безводный промежуток — 4 часа 10 мин. Масса тела при рождении 3400 г, длина тела 53 см. Оценка по шкале Апгар 7/8 баллов. Закричала сразу, крик громкий.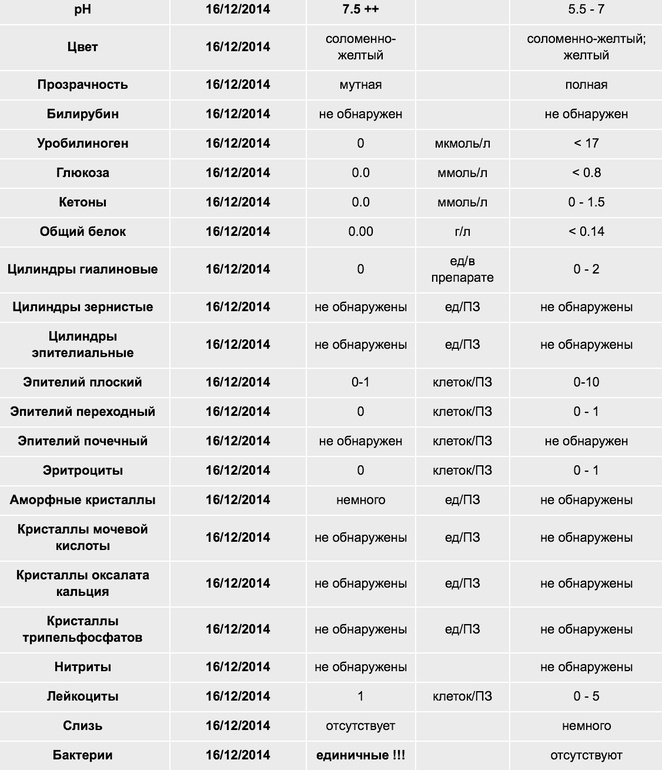 В возрасте 12 часов появилось желтушное прокрашивание кожи. Проводилась инфузионная и фототерапия.
В возрасте 12 часов появилось желтушное прокрашивание кожи. Проводилась инфузионная и фототерапия.
При осмотре на 5-й день жизни: кожные покровы интенсивно желтые с зеленоватым оттенком, склеры иктеричны, пупочная ранка сухая, в легких дыхание пуэрильное, хрипов нет, тоны сердца ясные, живот мягкий, печень выступает из-под края реберной дуги на 3,5 см, селезенка — на 1 см, моча имеет интенсивную окраску, физиологические рефлексы новорожденного снижены.
Общий анализ крови: НЬ — 152 г/л, Эр — 4,2х1012/л, ретикулоциты -6%, ц.п. — 0,99, Лейк — 12,0х109/л, п/я — 6%, с — 49%, э — 1%, л — 36%, м -8%, СОЭ — 2 мм/час.
Группа крови ребенка А(П) Rh-положительная.
Биохимический анализ крови на 4-й день жизни: общий белок -54,8 г/л, билирубин: непрямой — 328 мкмоль/л, прямой — 34 мкмоль/л, мочевина — 4,2 ммоль/л, холестерин — 7,0 ммоль/л, калий — 4,6 ммоль/л, натрий — 138 ммоль/л, кальций — 1,2 ммоль/л, ACT — 65 ед. , АЛТ — 71 ед., ЩФ — 350 ед.
, АЛТ — 71 ед., ЩФ — 350 ед.
Задание
- О каком заболевании можно думать в данном случае?
- Объясните патогенез данного заболевания.
- Оцените результаты общего анализа крови.
- Оцените результаты биохимического анализа крови.
- Какое дополнительное обследование следует провести ребенку для подтверждения диагноза?
- Можно ли было прогнозировать развитие этого заболевания гинекологами женской консультации?
- О каком осложнении основного заболевания можно думать в данном случае и почему?
- Какие осложнения могут возникнуть при проведении фототерапии?
- Назначьте лечение.
10.Какова тактика ведения акушерами женщины после родов?
Тестовый контроль
УКАЖИТЕ ОДИН ПРАВИЛЬНЫЙ ОТВЕТ
- 1. Неконъюгированный билирубин представляет собой комплекс
билирубина с:
а) жирными кислотами
б) глюкозой
в) альбумином
г) трансферрином
д) всем выше перечисленным
2. Коньюгированный билирубин – это комплекс билирубина с:
Коньюгированный билирубин – это комплекс билирубина с:
а) аминокислотами
б) глюкуроновой кислотой
в) глюкозой
г) витаминами
д) солями жирных кислот
3. Физиологическая желтуха новорожденного развивается в результате:
а) повышения образования непрямого билирубина из-за укороченной продолжительности жизни эритроцитов с фетальным гемоглобином
б) гипоальбуминемии
в) снижения активности глюкуронилтрансферазы
г) повышения образования непрямого билирубина из-за укороченной
продолжительности жизни эритроцитов с фетальным гемоглобином и
гипоальбуминемии д) повышения образования непрямого билирубина из-за укороченной продолжительности жизни эритроцитов с фетальным гемоглобином, гипоальбуминемии и снижения активности глюкуронилтрансферазы
4. При первичном гипотиреозе уровень ТТГ в крови:
При первичном гипотиреозе уровень ТТГ в крови:
а) повышен
б) не изменен
в) снижен
г) резко снижен
д) уровень ТТГ не имеет диагностического значения
5. Желтуха при синдроме Жильбера уменьшается при использовании:
а) фенобарбитала
б) антисекреторных препаратов
в) прокинетиков
г) эссенциале-форте
д) сульфаниламидов
6. При гипотиреозе у новорожденных процессы конъюгации билирубина:
а) замедляются
б) не изменяются
в) ускоряются
7. Причиной гемолитической болезни новорожденного является:
а) незрелость глюкуронилтрансферазы печени
б) изоиммунная гемолитическая анемия
в) гемоглобинопатия
г) внутриутробная инфекция
д) аутоиммунная гемолитическая анемия
8. При несовместимости крови матери и плода по резус-фактору гемолитическая болезнь новорожденного чаще развивается:
При несовместимости крови матери и плода по резус-фактору гемолитическая болезнь новорожденного чаще развивается:
а) при первой беременности
б) при повторных беременностях
9. Более тяжелое течение гемолитической болезни новорожденного отмечается при несовместимости крови матери и плода по:
а) резус-фактору
б) группе крови
10. Гемолитическая болезнь новорожденного при 1-й беременности обусловлена чаще несовместимостью крови матери и плода:
а) по АВО-системе
б) по резус-фактору
11. Желтуха при гемолитической болезни новорожденного появляется:
а) до 48 часов жизни
б) после 48 часов жизни
в) после 7 дня жизни
г) после 10 суток жизни
12. Выздоровление как исход фетального гепатита:
а) возможно
б) невозможно
13. Формирование атрезии желчевыводящих путей как результат перенесенного фетального гепатита:
Формирование атрезии желчевыводящих путей как результат перенесенного фетального гепатита:
а) возможно
б) невозможно
УКАЖИТЕ ВСЕ ПРАВИЛЬНЫЕ ОТВЕТЫ
14. К проявлениям гемолитической болезни новорожденного относятся:
а) гепатоспленомегалия
б) геморрагический синдром
в) тромбоцитопения
г) анемия
д) диспепсический синдром
15. В терапии гемолитической болезни новорожденного используют:
а) гормональную терапию
б) внутривенное введение стандартного иммуноглобулина
в) фототерапию
г) антибактериальную терапию
д) заменное переливание крови
16. Гипербилирубинемия с повышением уровня прямого билирубина отмечается при:
а) гемолитической болезни новорожденных
б) дефиците α-1-антитрипсина
в) конъюгационной желтухе, обусловленной морфо-функциональной незрелостью
г) атрезии желчевыводящих ходов
д) фетальном гепатите
Ответы на тесты:
1 – в
2 – б
3 – д
4 – а
5 – а
6 – а
7 – б
8 – б
9 – а
10 – а
11 – а
12 – а
13 – а
14 – а, г
15 – б, в, д
16 – б, г, д
Гипербилирубинемия у новорожденных: виды, причины, клинические обследования, меры профилактики и лечения: описательный обзор Статья
1. Олусанья Б.О., Осибанджо Ф.Б., Слашер Т.М.
(2015).
Факторы риска тяжелой неонатальной гипербилирубинемии в странах с низким и средним уровнем дохода: систематический обзор и метаанализ.
PLoS Один,
10
(2):
е0117229.
[Бесплатная статья PMC] [PubMed] [Google Scholar]
Олусанья Б.О., Осибанджо Ф.Б., Слашер Т.М.
(2015).
Факторы риска тяжелой неонатальной гипербилирубинемии в странах с низким и средним уровнем дохода: систематический обзор и метаанализ.
PLoS Один,
10
(2):
е0117229.
[Бесплатная статья PMC] [PubMed] [Google Scholar]
2. Бутани В.К., Зипурски А., Бленкоу Х., Ханна Р., Сгро М., Эббесен Ф. (2013). Неонатальная гипербилирубинемия и резус-болезнь новорожденных: оценки заболеваемости и нарушений на 2010 г. на региональном и глобальном уровнях. Педиатр Рез, 1: 86–100. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Параметр практики Американской академии педиатрии (1994). Лечение гипербилирубинемии у здорового доношенного новорожденного. Педиатрия, 94: 558–65. [PubMed] [Google Scholar]
4. Берк Б.Л., Роббинс Дж.М., Берд Т.М., Хоббс К.А., Несмит С., Тилфорд Дж.М. (2009). Тенденции госпитализации по поводу неонатальной желтухи и ядерной желтухи в США, 1988–2005 гг. Педиатрия, 123: 524–32. [PubMed] [Google Scholar]
5. Группа по изучению клинических признаков у младенцев раннего возраста
(2008).
Клинические признаки, предсказывающие тяжелое течение заболевания у детей в возрасте до 2 месяцев: многоцентровое исследование.
Ланцет,
371(
9607):
135–42.
[PubMed] [Google Scholar]
Группа по изучению клинических признаков у младенцев раннего возраста
(2008).
Клинические признаки, предсказывающие тяжелое течение заболевания у детей в возрасте до 2 месяцев: многоцентровое исследование.
Ланцет,
371(
9607):
135–42.
[PubMed] [Google Scholar]
6. Чоу Р.Х., Палмер Р.Х., Эжутачан С. и др. (2003). Ведение гипербилирубинемии у новорожденных: измерение эффективности с использованием модели сравнительного анализа. Педиатрия, 112: 1264–73. [PubMed] [Google Scholar]
7. Огунфовора О.Б., Даниэль О.Дж. (2006). Неонатальная желтуха и ее лечение: знания, отношение и практика общинных медицинских работников в Нигерии. Общественное здравоохранение BMC, 6: 19. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Шнайдер АП. (1986). Желтуха грудного молока у новорожденных: реальная сущность. ДЖАМА, 255( 23): 3270– 74. [PubMed] [Google Scholar]
9.
Наг Н., Гальдер С., Чаудхури Р., Адхикари С., Мазумдер С.
(2009).
Роль билирубина как антиоксиданта при желтухе новорожденных и влияние спиртового экстракта цедры сладкого лайма на экспериментально индуцированную желтуху у крыс. Индийская компания J Biochem Biophys,
46:
73–78.
[PubMed] [Google Scholar]
Индийская компания J Biochem Biophys,
46:
73–78.
[PubMed] [Google Scholar]
10. Юсефи М., Рахими Х., Барикбин Б., Тоосси П., Лотфи С., Хедаяти М. и др. (2011). Мочевая кислота: новый антиоксидант у больных вульгарной пузырчаткой. ЖДД, 56( 3): 278–281. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Барикбин Б., Юсефи М., Рахими Х., Хедаяти М., Разави С.М., Лотфи С. (2011). Антиоксидантный статус у больных красным плоским лишаем. Клин Эксп Дерматол, 36( 8): 851–54. [PubMed] [Google Scholar]
12. Палудетто Р., Манси Г., Раймонди Ф., Романо А., Криваро В., Бусси М., Д’Амброзио Г. (2002). Умеренная гипербилирубинемия вызывает временное изменение поведения новорожденного. Педиатрия, 110: е50. [PubMed] [Google Scholar]
13. Бу Нью-Йорк, Исхак С. (2007). Прогнозирование тяжелой гипербилирубинемии с помощью чрескожного билирубинометра Bilicheck. J Педиатр Детское здоровье, 43: 297–302. [PubMed] [Google Scholar]
14.
Насс Р.Д., Фрэнк Ю.
(2010). Когнитивные и поведенческие нарушения педиатрических заболеваний.
1-е изд.
Издательство Оксфордского университета.
[Google Scholar]
Когнитивные и поведенческие нарушения педиатрических заболеваний.
1-е изд.
Издательство Оксфордского университета.
[Google Scholar]
15. Гартнер Л.М., Ли К.С. (1999). Желтуха у грудного ребенка. Клин Перинатол, 26: 431–45. [PubMed] [Google Scholar]
16. Месич И., Милас В., Медимурек М., Римар З. (2014). Неконъюгированная патологическая желтуха у новорожденных. Колл Антропол, 38( 1): 173–8. [PubMed] [Академия Google]
17. Д’Сильва С., Колах Р.Б., Гош К., Мукерджи М.Б. (2014). Комбинированные эффекты полиморфизмов генов UGT1A1 и OATP2 как основного фактора риска неконъюгированной гипербилирубинемии у новорожденных в Индии. Ген, 547( 1): 18–22. [PubMed] [Google Scholar]
18. Хуан М.Дж., Куа К.Е., Тен Х.К., Тан К.С., Венг Х.В., Хуан К.С. (2004). Факторы риска тяжелой гипербилирубинемии у новорожденных. Педиатр Рез, 56( 5): 682–9. [PubMed] [Google Scholar]
19.
Ватко Дж. Ф., Лин З.
(2010).
Изучение генетической архитектуры неонатальной гипербилирубинемии. Semin Fetal Neonatal Med,
15:
169–175.
[PubMed] [Google Scholar]
Semin Fetal Neonatal Med,
15:
169–175.
[PubMed] [Google Scholar]
20. Сюй Л.И., Хе Ю.Дж., Чжан В., Дэн С., Ли К., Чжан В.С. и др. (2007). Гаплотипы полипептида-1B1, транспортирующие органический анион, у китайских пациентов. Акта Фармакол Син, 28: 1693–97. [PubMed] [Google Scholar]
21. Тирона Р.Г., Лик Б.Ф., Мерино Г. и Ким Р.Б. (2001). Полиморфизмы OATP-C: идентификация множественных аллельных вариантов, связанных с измененной транспортной активностью среди европейцев и афроамериканцев. Джей Биол Хим, 276: 35669–35675. [PubMed] [Google Scholar]
22. Санна С., Бусонеро Ф., Маскио А., Макардл П.Ф., Усала Г., Дей М. и др. (2009). Общие варианты в локусе SLCO1B3 связаны с уровнями билирубина и неконъюгированной гипербилирубинемией. Хум Мол Жене, 18: 2711–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23.
Аленкастро де Азеведу Л., Ревербель да Силвейра Т., Карвалью К.Г., Мартинс де Кастро С., Джульяни Р., Матте У.
(2012).
Полиморфизмы UGT1A1, SLCO1B1 и SLCO1B3 в сравнении с неонатальной гипербилирубинемией: есть ли связь?
Педиатр Рез,
72(
2):
169–73.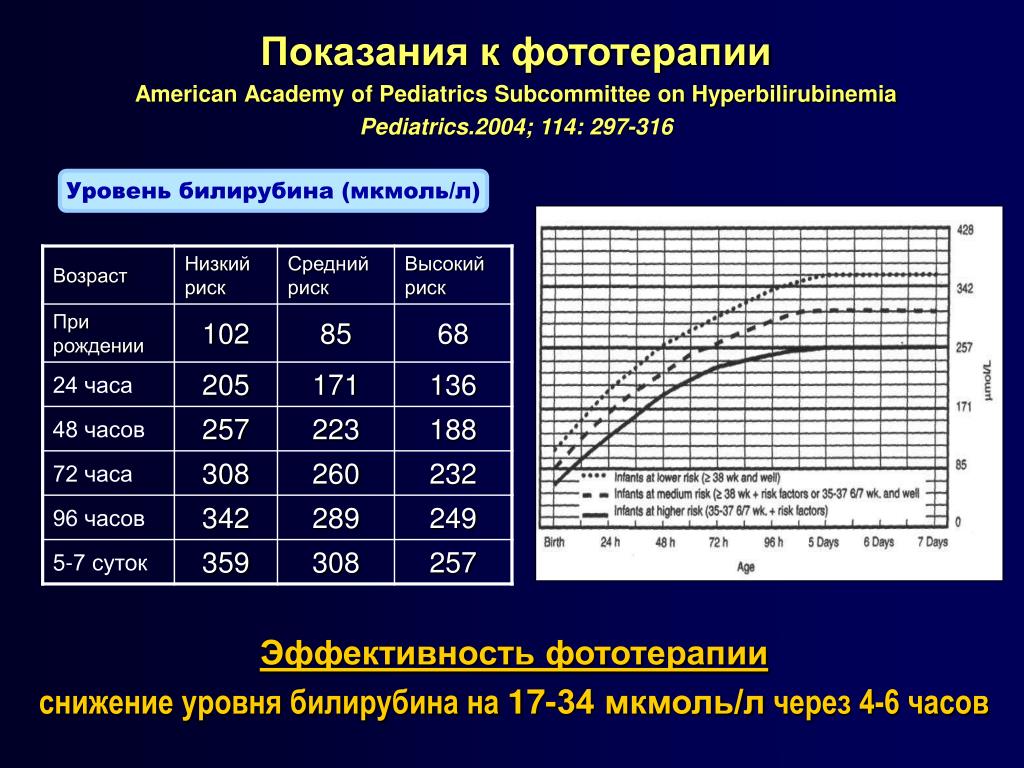 [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
24. Мишра С., Агарвал Р., Деорари А.К., Пол В.К. (2008). Желтуха у новорожденных. Индийский Дж. Педиатр, 75( 2): 157–163. [PubMed] [Google Scholar]
25. Бойд С. (2004). Лечение физиологической и патологической желтухи новорожденных. Нурс Таймс, 100( 13): 40–43. [PubMed] [Google Scholar]
26. Кларксон Дж. Э., Коуэн Дж. О., Хербисон Г.П. (1984). Желтуха у доношенных здоровых новорожденных: популяционное исследование. Ауст Педиатр Дж, 20: 303–8. [PubMed] [Академия Google]
27. Деннери П.А., Зайдман Д.С., Стивенсон Д.К. (2001). Неонатальная гипербилирубинемия. НЭЖМ, 344( 8): 581–290. [PubMed] [Google Scholar]
28. Майзелс М.Дж., Гиффорд К. (1983). Неонатальная желтуха у доношенных детей. Роль грудного вскармливания и других причин. АЖДК, 137: 561–2. [PubMed] [Google Scholar]
29. Алкок Г.С., Лили Х. (2002). Инфузия иммуноглобулина при изоиммунной гемолитической желтухе у новорожденных. ЦДСР, 3: CD003313. [PubMed] [Академия Google]
30. Аткинсон Л.Р., Эскобар Г.Дж., Такьяма Д.И., Ньюман Т.Б.
(2003).
Применение фототерапии у новорожденных с желтухой в крупной организации управляемой медицинской помощи: соблюдают ли клиницисты рекомендации?
Педиатрия,
111:
е555–61.
[PubMed] [Google Scholar]
Аткинсон Л.Р., Эскобар Г.Дж., Такьяма Д.И., Ньюман Т.Б.
(2003).
Применение фототерапии у новорожденных с желтухой в крупной организации управляемой медицинской помощи: соблюдают ли клиницисты рекомендации?
Педиатрия,
111:
е555–61.
[PubMed] [Google Scholar]
31. Хансен Т.В. (2003). Последние достижения в фармакотерапии гипербилирубинемии у новорожденных. Эксперт Опин Фармаколог, 4( 11): 1939–1948 гг. [PubMed] [Google Scholar]
32. Уинфилд Ч.Р., Макфол Р. (1978). Клиническое исследование продолжительной желтухи у детей, находящихся на грудном и искусственном вскармливании. Арч Дис Чайлд, 53: 506–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
33. Крамер ЛИ. (1969). Развитие кожной желтухи у новорожденных с желтухой. АЖДК, 118: 454–8. [PubMed] [Google Scholar]
34. Шапиро-Мендоса К. (2006). Факторы риска неонатальной заболеваемости и смертности среди «здоровых» поздних недоношенных новорожденных. Семин Перинатол, 30: 54–60. [PubMed] [Google Scholar]
35. Деннери Пенсильвания.
(2002).
Фармакологические вмешательства для лечения желтухи новорожденных.
Семин Неонатол,
7:
111–119.
[PubMed] [Академия Google]
Деннери Пенсильвания.
(2002).
Фармакологические вмешательства для лечения желтухи новорожденных.
Семин Неонатол,
7:
111–119.
[PubMed] [Академия Google]
36. Маруо Ю., Нисидзава К., Сато Х., Сава Х., Шимада М. (2000). Длительная неконъюгированная гипербилирубинемия, связанная с грудным молоком и мутациями гена билирубин-уридиндифосфат-глюкуронозилтрансферазы. Педиатрия, 106( 5): Е59. [PubMed] [Google Scholar]
37. Майзелс М.Дж. (1998). Желтуха. В: Taeugah HW, Ballard RA, Avery ME (редакторы). Болезни Шафферса и Эйвери у новорожденных ( 7-е изд.). Филадельфия: Компания WB Saunders; стр. 603– 708. [Академия Google]
38. Аль-Сваф Ф.Б., Джумаа Р.С., Саид И.С. (2009). Гемолитическая болезнь новорожденных вследствие несовместимости по системе АВО. Медицинский журнал Тикрит, 15( 2): 70–78. [Google Scholar]
39.
Стокман Дж.А.
(2001).
Обзор современного состояния резус-болезни: анамнез, текущее клиническое ведение и недавний прогресс.
J Pediatr Hematol Oncol,
23(
8):
554–62. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
40. Боуман Дж. (2003). Тридцать пять лет профилактики резус-фактора. переливание, 43: 1661–6. [PubMed] [Академия Google]
41. Ван Камп И.Л., Клумпер Ф.Дж., Оэпкес Д., Меерман Р.Х., Шерджон С.А., Ванденбусше Ф.П. и др. (2005). Осложнения внутриутробного внутрисосудистого переливания крови при анемии плода вследствие аллоиммунизации эритроцитов матери. Am J Obstet Gynecol, 192( 1): 171–7. [PubMed] [Google Scholar]
42. Мюррей Н.А., Робертс И.А. (2007). Гемолитическая болезнь новорожденных. ADC Fetal Neonatal Ed, 92: 83–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
43. Йигит С., Гурсой Т., Канра Т. и др. (2005). Цельная кровь в сравнении с эритроцитами и плазмой для обменного переливания при гемолитической болезни АВО. Трансфус Мед, 15: 313–8. [PubMed] [Академия Google]
44.
Ясин Х., Халаф М., Рашид Н., Дарвич М.
(2005).
Предотвращает ли профилактическая фототерапия гипербилирубинемию у новорожденных с АВО-несовместимостью и положительной пробой Кумбса?
Дж. Перинатол,
25:
590–4.
[PubMed] [Google Scholar]
Перинатол,
25:
590–4.
[PubMed] [Google Scholar]
45. Каплан М., Наамад М., Кенан А., Руденски Б., Хаммерман С., Времан Х.Дж., Вонг Р.Дж., Стивенсон Д.К. (2009). Неспособность предсказать гемолиз и гипербилирубинемию по подклассу IgG у детей с группой крови А или В, рожденных от матерей с группой О. Педиатрия, 123( 1): e132–7. [PubMed] [Академия Google]
46. Мойз Б., Насир А., Хан С.А., Херани С.А., Кадир М. (2012). Неонатальная гипербилирубинемия у младенцев с вариантом G6PD c.563C > T. БМС Педиатрия, 12: 126–133. [Бесплатная статья PMC] [PubMed] [Google Scholar]
47. Марзбан А, Мосавинасаб Н. (2008). Корреляция между гемолизом и желтухой у новорожденных с дефицитом глюкозо-6-фосфатдегидрогеназы. Акта Медика Ираника, 47( 5): 379–83. [Google Scholar]
48. Каплан М., Хаммерман С. (1998). Тяжелая неонатальная гипербилирубинемия. Потенциальное осложнение дефицита глюкозо-6-фосфатдегидрогеназы. Клин Перинатол, 25( 3): 575–90. [PubMed] [Google Scholar]
49.2007/ukr/6/1.png) Бутани В.К., Джонсон Л., Сивьери М.Э.
(1999).
Прогностическая способность часового билирубина сыворотки перед выпиской для последующей значительной гипербилирубинемии у здоровых доношенных и доношенных новорожденных.
Педиатрия,
103(
1):
6–16.
[PubMed] [Google Scholar]
Бутани В.К., Джонсон Л., Сивьери М.Э.
(1999).
Прогностическая способность часового билирубина сыворотки перед выпиской для последующей значительной гипербилирубинемии у здоровых доношенных и доношенных новорожденных.
Педиатрия,
103(
1):
6–16.
[PubMed] [Google Scholar]
50. Кэшор В.Дж. (2000). Билирубин и желтуха в микропремии. Клин Перинатол, 27: 171–9. [PubMed] [Google Scholar]
51. Джонсон Л., Бутани В.К. (1998). Рекомендации по ведению доношенных и недоношенных детей с желтухой. Клин Перинатол, 25: 555–574. [PubMed] [Академия Google]
52. Уотсон Д., Роджерс Дж.А. (1961). Исследование шести репрезентативных методов анализа билирубина плазмы. Джей Клин Патол, 14: 271–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
53. Яманучи И., Ямаути Ю., Игараши И. (1980). Чрескожная билирубинометрия: предварительные исследования неинвазивного чрескожного измерителя билирубина в Национальной больнице Окаяма. Педиатрия, 65: 195–202. [PubMed] [Google Scholar]
54. Maisels MJ, Ostrea EM, Touch S, Clune SE, Cepeda E, Kring E и др.
(2004).
Оценка нового чрескожного билирубинометра.
Педиатрия,
113:
1628–35.
[PubMed] [Академия Google]
Maisels MJ, Ostrea EM, Touch S, Clune SE, Cepeda E, Kring E и др.
(2004).
Оценка нового чрескожного билирубинометра.
Педиатрия,
113:
1628–35.
[PubMed] [Академия Google]
55. Гохманн К., Розер М., Ролински Б., Кадов И., Мюллер С., Герлах-Гроу А. и др. (2006). Измерение билирубина у новорожденных: сравнение 9 часто используемых методов. Педиатрия, 117( 4): 1174–83. [PubMed] [Google Scholar]
56. Пуппалвар П.В., Госвами К., Дхок А. (2012). Обзор на тему «Эволюция методов оценки билирубина». IOSR-JDMS, 1( 3): 17–18. [Google Scholar]
57. Королевская больница принца Альфреда (2003). Гемолитическая желтуха, резус-изоиммунизация. Рекомендации RPA по уходу за новорожденными: Королевская больница принца Альфреда, Сидней, Австралия. [Академия Google]
58. Bosschaart N, Kok JH, Newsum AM, Ouwenee DM, Mentink R, van Leeuwen TG, et al. (2012). Ограничения и возможности чрескожного измерения билирубина. Педиатрия, 129: 689–97. [PubMed] [Google Scholar]
59. Кришнасами М., Бакри Д.Р.
(2009).
Неинвазивный ручной чрескожный билирубинометр.
Отдел развития медицины, Министерство здравоохранения,
Малайзия.
[Google Scholar]
Кришнасами М., Бакри Д.Р.
(2009).
Неинвазивный ручной чрескожный билирубинометр.
Отдел развития медицины, Министерство здравоохранения,
Малайзия.
[Google Scholar]
60. Робертсон А., Казмерчак С., Вос П. (2002). Усовершенствованная чрескожная билирубинометрия: сравнение SpectRx Bilicheck и измерителя желтухи Minolta JM-102 для оценки общей сыворотки в нормальной популяции новорожденных. Джей Перинатоло, 22( 1): 12–14. [PubMed] [Академия Google]
61. Американская академия педиатрии (2004б). Клиническое практическое руководство: Подкомитет по гипербилирубинемии, Ведение гипербилирубинемии у новорожденных на 35-й и более неделе беременности. Педиатрия, 114( 1): 297–316. [PubMed] [Google Scholar]
62. Ватко Дж. Ф., Майзелс М. Дж. (2003). Желтуха у детей с низкой массой тела при рождении: патобиология и исход. Arch Dis Child Fetal Neonatal Ed, 88: Ф455–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
63.
Okwundu CI, Okoromah CAH, Shah PS.
(2012).
Профилактическая фототерапия для предотвращения желтухи у недоношенных или маловесных детей при рождении.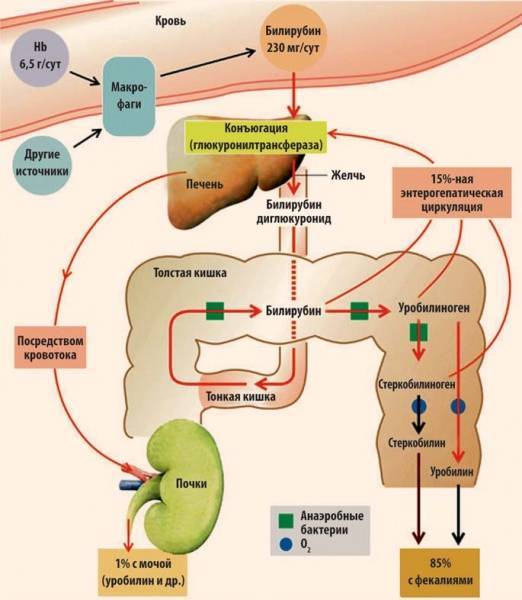 Cochrane Database Syst Rev,
2012 (1):
CD007966.
[PubMed] [Google Scholar]
Cochrane Database Syst Rev,
2012 (1):
CD007966.
[PubMed] [Google Scholar]
64. Майзелс М.Дж., Ватко Дж.Ф., Бутани В.К., Стивенсон Д.К. (2012). Подход к лечению гипербилирубинемии у недоношенных детей до 35 недель гестации. Дж. Перинатол, 32: 660–4. [PubMed] [Google Scholar]
65. Фрэнк Дж. Э. (2005). Диагностика и лечение дефицита G6PD. Ам Фам Врач, 72( 7): 1277–1282 гг. [PubMed] [Google Scholar]
66. Энгл В.Д., Джексон Г.Л., Сендельбах Д., Мэннинг Д., Фроули В. (2002). Оценка чрескожного устройства в оценке неонатальной гипербилирубинемии в преимущественно латиноамериканском населении. Педиатрия, 110: 61–67. [PubMed] [Академия Google]
67. Шумахер Р. (2002). Чрескожная билирубинометрия и диагностические тесты: «правильный выбор инструмента». Педиатрия, 110: 407–408. [PubMed] [Google Scholar]
68.
Ип С., Гликен С., Кулиг Дж., Обриен Р., Сеге Р., Лау Дж.
(2003).
Лечение неонатальной гипербилирубинемии.
Роквилл, Мэриленд:
Министерство здравоохранения и социальных служб США, Агентство медицинских исследований и качества. Публикация AHRQ 03-E011.
[Google Scholar]
Публикация AHRQ 03-E011.
[Google Scholar]
69. Каппас А., Драммонд Г.С., Мансон Д.П., Маршалл Дж.Р. (2001). Sn-мезопорфириновая профилактика тяжелой гипербилирубинемии у новорожденных Свидетелей Иеговы как альтернатива обменному переливанию крови. Педиатрия, 108: 1374–137. [PubMed] [Академия Google]
70. Энневер Дж. Ф. (1990). Синий свет, зеленый свет, белый свет, больше света: лечение желтухи новорожденных. Клин Перинатол, 17: 467–81. [PubMed] [Google Scholar]
71. Кремер Р.Дж., Перриман Р.В., Ричардс Д.Х. (1958). Влияние света на гипербилирубинемию у детей раннего возраста. Ланцет, 1: 1094–107. [PubMed] [Google Scholar]
72. Браун А.К., Ким М.Х., Ву П.Ю., Брыла Д.А. (1985). Эффективность фототерапии в профилактике и лечении гипербилирубинемии новорожденных. Педиатрия, 75: 393–400 [PubMed] [Google Scholar]
73. Векки К., Донцелли Г.П., Мильорини М.Г., Сбрана Г. (1983). Зеленый свет в фототерапии. Педиатр Рез, 17: 461–3. [PubMed] [Google Scholar]
74. Тан КЛ.
(1989).
Эффективность флуоресцентных ламп дневного света, синих и зеленых ламп при лечении негемолитической гипербилирубинемии.
Джей Педиатр,
114:
132–7.
[PubMed] [Google Scholar]
Тан КЛ.
(1989).
Эффективность флуоресцентных ламп дневного света, синих и зеленых ламп при лечении негемолитической гипербилирубинемии.
Джей Педиатр,
114:
132–7.
[PubMed] [Google Scholar]
75. Тан КЛ. (1991). Фототерапия желтухи новорожденных. Клин Перинатол, 18: 423–39. [PubMed] [Академия Google]
76. Амато М., Хоуальд Х., фон Муральт Г. (1985). Прерывание грудного вскармливания по сравнению с фототерапией в лечении гипербилирубинемии у доношенных детей. Гельветика Педиатрика Акта, 40: 127–31. [PubMed] [Google Scholar]
77. Кальдера Р., Майнье М., Сендер А., Броссар Ю., Тортрат Д., Галиай Ж.С., Бадуаль Ж. (1993). Эффект человеческого альбумина в сочетании с интенсивной фототерапией при лечении желтухи новорожденных. арх о. Педиатр, 50: 399–402. [PubMed] [Академия Google]
78. Майзелс М.Дж. (2001). Фототерапия – традиционная и нетрадиционная. Дж. Перинатол, 21( приложение 1): С93–7. [PubMed] [Google Scholar]
79.
Зайдман Д.С., Мойзе Дж., Эргаз З. , Лаор А., Времан Х.Дж., Стивенсон Д.К., Гейл Р.
(2000).
Новое устройство для фототерапии, излучающее синий свет: проспективное рандомизированное контролируемое исследование.
Джей Педиатр,
136(
6):
771–4.
[PubMed] [Google Scholar]
, Лаор А., Времан Х.Дж., Стивенсон Д.К., Гейл Р.
(2000).
Новое устройство для фототерапии, излучающее синий свет: проспективное рандомизированное контролируемое исследование.
Джей Педиатр,
136(
6):
771–4.
[PubMed] [Google Scholar]
80. Харрис М., Бернбаум Дж., Полин Дж., Циммерман Р., Полин Р.А. (2001). Наблюдение за развитием доношенных и недоношенных детей с выраженной гипербилирубинемией, находящихся на грудном вскармливании. Педиатрия, 107: 1075–1080. [PubMed] [Академия Google]
81. Американская академия педиатрии (2004а). Подкомитет по гипербилирубинемии. Ведение гипербилирубинемии у новорожденных в возрасте 35 и более недель гестации. Педиатрия, 114 ( 3): 297–316. [PubMed] [Google Scholar]
82. Королевская больница принца Альфреда (2006). Чрескожные билирубинометры. Руководство по уходу RPA Newbon, Королевская больница принца Альфреда, Сидней, Австралия. [Google Scholar]
83.
Ся ДЙЙ, Аллен Ф.Х., Геллисс С.С., Драммонд Л.К.
(1952).
Эритробластоз плода, VIII: исследование билирубина в сыворотке в связи с ядерной желтухой. N Engl J Med,
247:
668–71.
[PubMed] [Академия Google]
N Engl J Med,
247:
668–71.
[PubMed] [Академия Google]
84. Моллисон П.Л., Катбуш М. (1954). Гемолитическая болезнь новорожденных. В: Гэрднер Д., изд. Последние достижения педиатрии. Нью-Йорк, штат Нью-Йорк: П. Блэкистон и сын, стр.: 110. [Google Академия]
85. Габилан Дж. (1998). Фармакологическое лечение желтухи новорожденных. Новый подход. Архив педиатрии, 5( 11): 1274–8. [PubMed] [Google Scholar]
86. Cuperus FJ, Hafkamp AM, Hulzebos CV, Verkade HJ. (2009). Фармакологическая терапия неконъюгированной гипербилирубинемии. Карр Фарм Дес, 15( 25): 2927–38. [PubMed] [Google Scholar]
87. Касем Л.М., Абдельрахим М.А., Нагиб Х.Ф. (2013). Изучение эффективности и безопасности силимарина при лечении гипербилирубинемии при желтухе новорожденных. Медицинские науки, 2( 2): 575–590. [Google Scholar]
88.
Валаес Т., Петмезаки С., Хеншке С., Драммонд Г.С., Каппас А.
(1994).
Контроль желтухи у недоношенных новорожденных с помощью ингибитора продукции билирубина: исследования с оловом-мезопорфирином. Педиатрия,
93(
1):
1–11.
[PubMed] [Академия Google]
Педиатрия,
93(
1):
1–11.
[PubMed] [Академия Google]
89. Мари С, Крестейл Т. (1989). Индуцируемая фенобарбиталом экспрессия генов в развивающейся печени крыс: связь с функцией гепатоцитов. Биохимика и Биофизика Акта, 1009( 3): 221–8. [PubMed] [Google Scholar]
90. Шанкаран С., Папиле Л.А., Райт Л.Л., Эренкранц Р.А., Меле Л., Лемонс Дж.А. и соавт. (1997). Влияние антенатальной терапии фенобарбиталом на неонатальное внутричерепное кровоизлияние у недоношенных детей. N Engl J Med, 337( 7): 466–471. [PubMed] [Академия Google]
91. Шанкаран С., Уолдт Э., Нельсон Дж., Бедард М., Делани-Блэк В. (1996). Антенатальная фенобарбитальная терапия и неонатальные исходы. II: Исход развития нервной системы через 36 месяцев. Педиатрия, 97( 5): 649–52. [PubMed] [Google Scholar]
92. Хансен Т.В., Томмарелло С. (1998). Влияние фенобарбитала на метаболизм билирубина в мозге крыс. Биол Неонат, 73( 2): 106–11. [PubMed] [Google Scholar]
93.
Кроутер, Калифорния, Henderson-Smart DJ.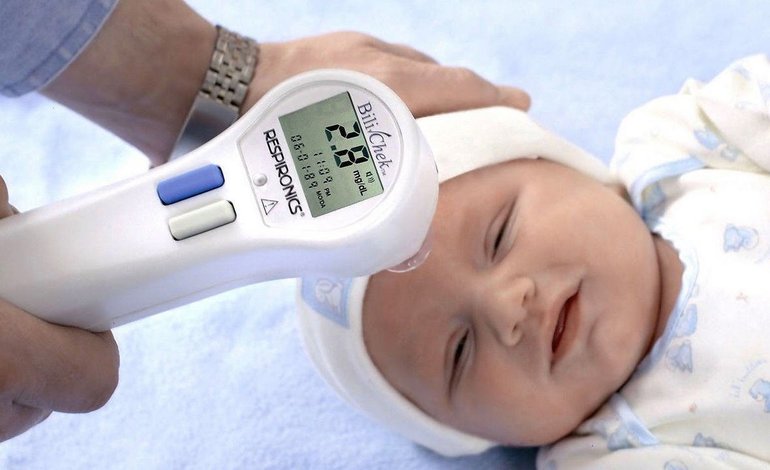 (2000).
Фенобарбитал перед преждевременными родами для предотвращения неонатального перивентрикулярного кровотечения.
Cochrane Database Syst Rev,
2000 г.;
2
CD000164.
[PubMed] [Академия Google]
(2000).
Фенобарбитал перед преждевременными родами для предотвращения неонатального перивентрикулярного кровотечения.
Cochrane Database Syst Rev,
2000 г.;
2
CD000164.
[PubMed] [Академия Google]
94. Уайтлоу А. (2001). Постнатальный фенобарбитон для профилактики внутрижелудочковых кровоизлияний у недоношенных детей. Cochrane Database Syst Rev, 2001 г.; 1 CD001691. [PubMed] [Google Scholar]
95. Сато К., Хара Т., Кондо Т., Ивао Х., Хонда С., Уэда К. (1991). Высокодозная внутривенная терапия гаммаглобулином при неонатальной иммуногемолитической желтухе из-за несовместимости групп крови. Acta Paediatr Scand, 80: 163–6. [PubMed] [Google Scholar]
96. Рубо Дж., Альбрехт К., Лаш П., Лауфкоттер Э., Лейтитис Дж., Марсан Д. и др. (1992). Внутривенное введение высоких доз иммуноглобулинов при гипербилирубинемии, вызванной резус-гемолитической болезнью. Джей Педиатр, 121: 93–7. [PubMed] [Google Scholar]
97.
Эргаз З., Арад И.
(1993).
Внутривенная иммуноглобулиновая терапия при иммуногемолитической желтухе новорожденных. J Перинат Мед,
21(
3):
183–7.
[PubMed] [Google Scholar]
J Перинат Мед,
21(
3):
183–7.
[PubMed] [Google Scholar]
98. Хаммерман С., Каплан М., Времан Х.Дж., Стивенсон Д.К. (1996). Внутривенный иммуноглобулин при АВО-изоиммунизации новорожденных: факторы, связанные с клинической эффективностью. Биол Неонат, 70: 69–74. [PubMed] [Google Scholar]
99. Алпай Ф., Саричи С.У., Окутан В., Эрдем Г., Озджан О., Гокчай Э. (1999). Высокодозная внутривенная иммуноглобиновая терапия при иммуногемолитической желтухе новорожденных. Акта Педиатрика, 88: 216–219. [PubMed] [Google Scholar]
100. Гириш Г., Чавла Д., Агарвал Р., Пол В.К., Деорари А.К. (2008). Эффективность двух режимов дозирования внутривенного иммуноглобулина при резус-гемолитической болезни новорожденных – рандомизированное контролируемое исследование. индийская педиатрия, 45: 653–9. [PubMed] [Google Scholar]
101.
Смитс-Винтдженс В.Е., Вальтер Ф.Дж., Рат М.Е., Линденбург И.Т., те Пас А.Б., Крамер К.М., Оепкес Д., Бранд А., Лоприоре Э.
(2011).
Внутривенный иммуноглобулин у новорожденных с резус-гемолитической болезнью: рандомизированное контролируемое исследование.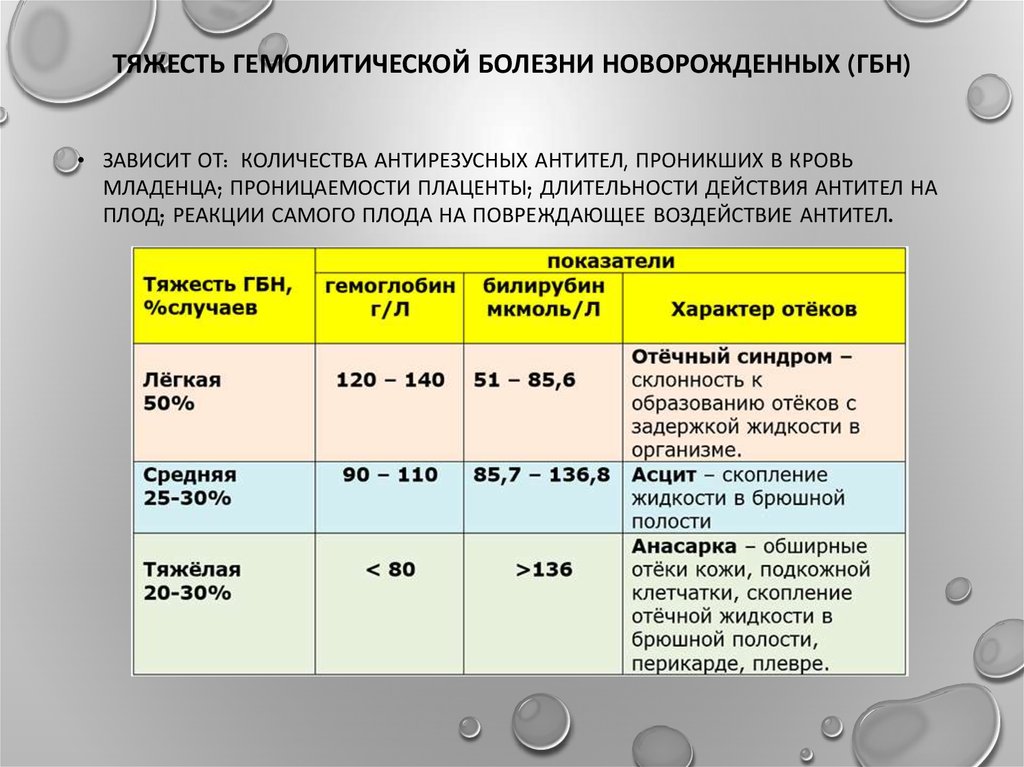 Педиатрия,
127:
680–6.
[PubMed] [Google Scholar]
Педиатрия,
127:
680–6.
[PubMed] [Google Scholar]
102. Корти А., Эльзааби М., Вагеманс Т., Рош Б., Ожар Ю. (2014). Эффективность и безопасность внутривенных иммуноглобулинов при лечении неонатальной гипербилирубинемии из-за несовместимости по системе АВО: метаанализ. Архив педиатрии, 21( 9): 976–83. [PubMed] [Google Scholar]
103. Qato MK, Мэн MD. (1985). Профилактика неонатальной гипербилирубинемии у нечеловеческих приматов с помощью Zn-протопорфирина. Биохим Дж, 226( 1): 51–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
104. Времан Х.Дж., Экстранд Б.С., Стивенсон Д.К. (1993). Выбор ингибиторов металлопорфирингемовой оксигеназы на основе активности и фотореактивности. Педиатр Рез, 33( 2): 195–200. [PubMed] [Google Scholar]
105.
Каппас А., Драммонд Г.С., Хеншке С., Валеес Т.
(1995).
Прямое сравнение Sn-мезопорфирина, ингибитора продукции билирубина, и фототерапии в борьбе с гипербилирубинемией у доношенных и доношенных новорожденных.
Педиатрия,
95(
4):
468–74.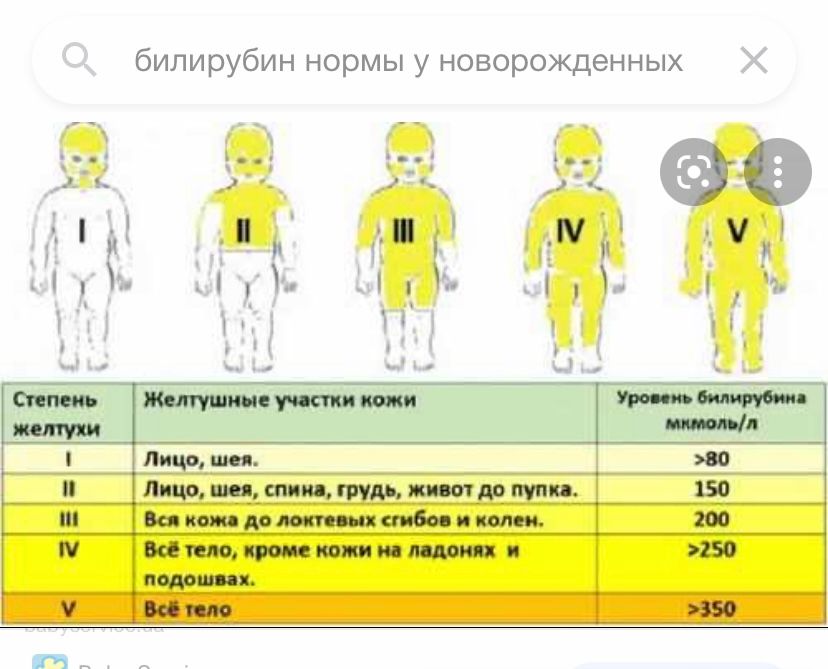 [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
106. Валаес Т., Драммонд Г.С., Каппас А. (1998). Контроль гипербилирубинемии у новорожденных с дефицитом глюкозо-6-фосфатдегидрогеназы с помощью ингибитора продукции билирубина Sn-мезопорфирина. Педиатрия, 101 (5): Е1. [PubMed] [Google Scholar]
107. Мартинес Х.С., Гарсия Х.О., Отегай Л.Е., Драммонд Г.С., Каппас А. (1999). Контроль тяжелой гипербилирубинемии у доношенных новорожденных с помощью ингибитора продукции билирубина Sn-мезопорфирина. Педиатрия, 103( 1): 1–5. [PubMed] [Google Scholar]
108. Facchini FP, Mezzacappa MA, Rosa IRM, Filho FM, Netto AA, Marba STM. (2007). Диспансеризация желтухи новорожденных у доношенных и поздних недоношенных новорожденных. Джей Педиатр (Рио Джей), 83( 4): 313–8. [PubMed] [Google Scholar]
109.
Шарма П., Чангани Н.П., Мина К.Р., Джора Р., Шарма Н., Гупта Б.Д.
(2006).
Аудиометрия вызванной реакции ствола мозга (BAER) у новорожденных с гипербилирубинемией.
Индийский Дж. Педиатр,
73 (
5):
413–6. [PubMed] [Академия Google]
[PubMed] [Академия Google]
110. Бутани ВК. (2012). Желтуха из-за дефицита глюкозо-6-фосфатдегидрогеназы. Нео Рев, 13( 3): e166–79. [Google Академия]
111. Кубои Т., Кусака Т., Кавада К., Кояно К., Накамура С., Окубо К. и др. (2013). Почасовая номограмма транскутанного билирубина у новорожденных в Японии. Педиатр Инт, 55: 608–11. [PubMed] [Google Scholar]
От новорожденных до 2 месяцев
%PDF-1.4 % 1 0 объект > эндообъект 4 0 объект >поток doi:10.1542/pir.2015-0132application/pdf
 0.0 (Windows)uuid:993dd606-1dd1-11b2-0a00-ec09279d8f00uuid:993dd609-1dd1-11b2-0a00-b30000000000
конечный поток
эндообъект
3 0 объект
>
эндообъект
2 0 объект
>
эндообъект
5 0 объект
>
эндообъект
6 0 объект
>
эндообъект
18 0 объект
>/ExtGState>/Font>/ProcSet[/PDF/Text/ImageC/ImageI]/Properties>/XObject>>>/Rotate 0/Thumb 65 0 R/Type/Page>>
эндообъект
19 0 объект
>/ExtGState>/Font>/ProcSet[/PDF/Text/ImageC]/XObject>>>/Rotate 0/Thumb 74 0 R/Type/Page>>
эндообъект
254 0 объект
>/ProcSet[/PDF/Text/ImageB]/XObject>>>/Type/Page>>
эндообъект
255 0 объект
>/ProcSet[/PDF/Text/ImageB/ImageC]/XObject>>>/Type/Page>>
эндообъект
270 0 объект
[273 0 Р 274 0 Р 275 0 Р]
эндообъект
271 0 объект
>поток
д
364,4989014 0 0 62.369812 109.7505493 635.630188 см
/Im0 Делать
Вопрос
БТ
/T1_0 1 тс
12 0 0 12 222,83817 557,99991 Тм
(DOI: 10.1542/pir.2015-0132)Тж
7,49899 1 тд
(2017;38;499)Тдж
/T1_1 1 тс
-8,52701 0 Тд
(Обзор педиатрии\240)Tj
/T1_0 1 тс
0,154 1,00001 Тд
(Дебра Х. Пэн и Иоланда Ривас) Tj
/T1_2 1 тс
-1,18148 1 тд
(желтуха: от новорожденных до 2 месяцев) Tj
ET
БТ
/T1_0 1 тс
12 0 0 12 432,32797 475,99994 Тм
( )Tj
0 0 1 рг
-23,388 0 тд
(http://pedsinreview.
0.0 (Windows)uuid:993dd606-1dd1-11b2-0a00-ec09279d8f00uuid:993dd609-1dd1-11b2-0a00-b30000000000
конечный поток
эндообъект
3 0 объект
>
эндообъект
2 0 объект
>
эндообъект
5 0 объект
>
эндообъект
6 0 объект
>
эндообъект
18 0 объект
>/ExtGState>/Font>/ProcSet[/PDF/Text/ImageC/ImageI]/Properties>/XObject>>>/Rotate 0/Thumb 65 0 R/Type/Page>>
эндообъект
19 0 объект
>/ExtGState>/Font>/ProcSet[/PDF/Text/ImageC]/XObject>>>/Rotate 0/Thumb 74 0 R/Type/Page>>
эндообъект
254 0 объект
>/ProcSet[/PDF/Text/ImageB]/XObject>>>/Type/Page>>
эндообъект
255 0 объект
>/ProcSet[/PDF/Text/ImageB/ImageC]/XObject>>>/Type/Page>>
эндообъект
270 0 объект
[273 0 Р 274 0 Р 275 0 Р]
эндообъект
271 0 объект
>поток
д
364,4989014 0 0 62.369812 109.7505493 635.630188 см
/Im0 Делать
Вопрос
БТ
/T1_0 1 тс
12 0 0 12 222,83817 557,99991 Тм
(DOI: 10.1542/pir.2015-0132)Тж
7,49899 1 тд
(2017;38;499)Тдж
/T1_1 1 тс
-8,52701 0 Тд
(Обзор педиатрии\240)Tj
/T1_0 1 тс
0,154 1,00001 Тд
(Дебра Х. Пэн и Иоланда Ривас) Tj
/T1_2 1 тс
-1,18148 1 тд
(желтуха: от новорожденных до 2 месяцев) Tj
ET
БТ
/T1_0 1 тс
12 0 0 12 432,32797 475,99994 Тм
( )Tj
0 0 1 рг
-23,388 0 тд
(http://pedsinreview.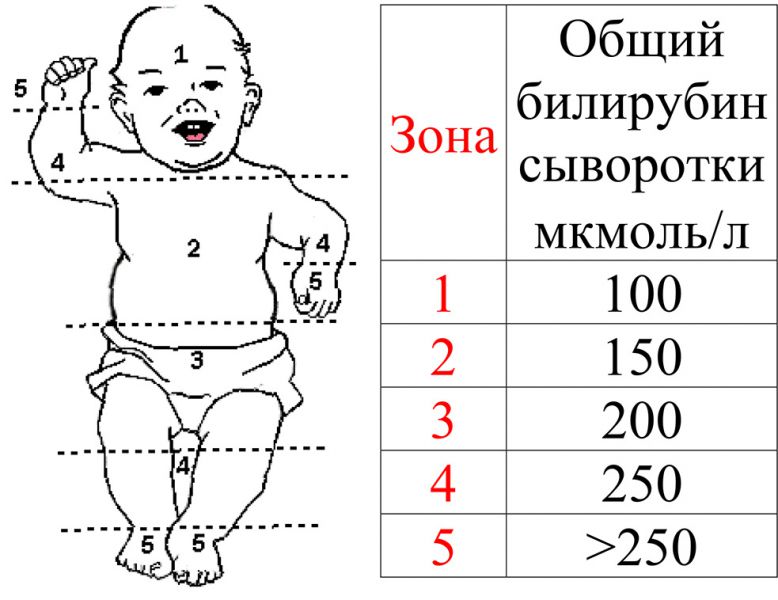 aappublications.org/content/38/11/499)Tj
0 г
4.45951 1 тд
(размещено во всемирной паутине по адресу: )Tj
-9.0135 1.00001 Тд
(Онлайн-версия этой статьи вместе с обновленной информацией и
услуги, есть)Tj
ET
БТ
0 0 1 рг
/T1_0 1 тс
10 0 0 10 128,24995 417,99997 Тм
(http://pedsinreview.aappublications.org/content/suppl/2017/10/31/38.11.4\
99.DC1)Тж
0 г
12.29201 1 тд
(Дополнение к данным: )Tj
ET
84 167 416 62 рэ
0 0 м
С
БТ
/T1_0 1 тс
10 0 0 10 94 172,99988 Тм
(Педиатрия. Все права защищены. Печатный ISSN: 0191-9601.) Tj
0 1 ТД
(Бульвар, Элк-Гроув-Виллидж, Иллинойс, 60007. Copyright \251 2017 by th\
Американская академия )Tj
0 1.00001 ТД
(опубликовано и зарегистрировано под торговой маркой Американской академии педиатрии, 141 №\
rthwest Point)Tj
0 1 ТД
(издание, выходит непрерывно с 1979. Педиатрия i\
n Обзор принадлежит, )Tj
Т*
(Pediatrics in Review — официальный журнал Американской академии
Педиатрия. Ежемесячно)Tj
ET
д
268 0 0 40,75 158 72,25 см
-1 TL /Im1 Do
Вопрос
БТ
/T1_0 1 тс
8 0 0 8 334,32794 18 Тм
(гость, 27 ноября 2017 г.
aappublications.org/content/38/11/499)Tj
0 г
4.45951 1 тд
(размещено во всемирной паутине по адресу: )Tj
-9.0135 1.00001 Тд
(Онлайн-версия этой статьи вместе с обновленной информацией и
услуги, есть)Tj
ET
БТ
0 0 1 рг
/T1_0 1 тс
10 0 0 10 128,24995 417,99997 Тм
(http://pedsinreview.aappublications.org/content/suppl/2017/10/31/38.11.4\
99.DC1)Тж
0 г
12.29201 1 тд
(Дополнение к данным: )Tj
ET
84 167 416 62 рэ
0 0 м
С
БТ
/T1_0 1 тс
10 0 0 10 94 172,99988 Тм
(Педиатрия. Все права защищены. Печатный ISSN: 0191-9601.) Tj
0 1 ТД
(Бульвар, Элк-Гроув-Виллидж, Иллинойс, 60007. Copyright \251 2017 by th\
Американская академия )Tj
0 1.00001 ТД
(опубликовано и зарегистрировано под торговой маркой Американской академии педиатрии, 141 №\
rthwest Point)Tj
0 1 ТД
(издание, выходит непрерывно с 1979. Педиатрия i\
n Обзор принадлежит, )Tj
Т*
(Pediatrics in Review — официальный журнал Американской академии
Педиатрия. Ежемесячно)Tj
ET
д
268 0 0 40,75 158 72,25 см
-1 TL /Im1 Do
Вопрос
БТ
/T1_0 1 тс
8 0 0 8 334,32794 18 Тм
(гость, 27 ноября 2017 г.
