ЭЭГ новорожденных с церебральной ишемией после терапевтической гипотермии
ЭЭГ новорожденных с церебральной ишемией после терапевтической гипотермии
Одной из актуальных проблем неонатологии и педиатрии является гипоксически-ишемическая энцефалопатия, развивающаяся вследствие перенесенной интранатальной асфиксии. В настоящий момент основным способом нейропротекторной защиты головного мозга считается терапевтическая гипотермия — наиболее эффективная и безопасная методика, позволяющая снизить неблагоприятные последствия поражения центральной нервной системы.
Специалисты ФГБОУ ВО «Курский государственный медицинский университет» МЗ РФ провели исследование результатов 30 электроэнцефалограмм новорожденных со сроком гестации более 36 недель, перенесших умеренную или тяжелую интранатальную асфиксию с диагнозом церебральная ишемия 2–3-й степени.
В течение первых двух часов после рождения новорожденные с интранатальной асфиксией и с выявленными показаниями к проведению процедуры начинали получать в качестве лечения контролируемое индуцируемое снижение центральной температуры тела до 33,5 °С в течение 72 ч.
По окончании терапевтической гипотермии пациентам проводилось согревание с повышением центральной температуры не более 0,5 °С в час, до ректальной температуры 37 °С. При удовлетворительном состоянии ребенка длительность фазы согревания составляла в среднем 7–9 часов.
Авторами выявлено, что в 87 % случаев гипоксически-ишемического поражения мозга после проведения терапевтической гипотермии общее состояние новорожденных улучшилось, картина ЭЭГ имеет положительную динамику: сохранена синхронность разрядов вспышек, четко прослеживается чередование циклов сонбодрствование, эпилептиформной активности не зарегистрировано.
Достаточно высокую эффективность проводимого лечения можно оценить и на фоне неврологического статуса новорожденных. У всех детей с церебральной ишемией 2–3-й стадии наблюдалась типичная картина: на момент рождения до проведения терапевтической гипотермии общее состояние тяжелое. Спонтанная двигательная активность снижена. Мышечный тонус дистоничен с преобладанием диффузной гипотонии конечностей. Мышечная сила снижена. Рефлексы конечностей вызываются, снижены, симметричны. Рефлексы новорожденных все отрицательные. На болевой раздражитель реакция движением (сгибание стопы).
У всех детей с церебральной ишемией 2–3-й стадии наблюдалась типичная картина: на момент рождения до проведения терапевтической гипотермии общее состояние тяжелое. Спонтанная двигательная активность снижена. Мышечный тонус дистоничен с преобладанием диффузной гипотонии конечностей. Мышечная сила снижена. Рефлексы конечностей вызываются, снижены, симметричны. Рефлексы новорожденных все отрицательные. На болевой раздражитель реакция движением (сгибание стопы).
При осмотре на 7-е сутки после рождения во всех исследуемых случаях наблюдалась следующая клиническая картина: общее состояние средней степени тяжести, с положительной динамикой, спонтанная двигательная активность достаточная. Мышечный тонус дистоничен с преобладанием умеренного флексорного гипертонуса конечностей. Мышечная сила сохранена, все рефлексы новорожденных положительны. То есть клинически проявляется положительная динамика неврологического состояния новорожденных с гипоксически-ишемическими поражениями после проведения лечебной гипотермии.
Достоверным подтверждением результатов исследования являются результаты ЭЭГ, позволяющей оценить динамику функционального состояния мозга новорожденного на протяжении всего периода болезни вне зависимости от активности ребенка. Несмотря на положительную клиническую картину, необходимо более информативное и доказательное подтверждение эффективности проводимого лечения, в чем и состоит особенность и важность ЭЭГ как метода исследования. ЭЭГ позволяет оценить не только эффективность терапевтической гипотермии, но и особенности электрогенеза развивающегося мозга. аЭЭГ позволяет в ранние сроки выявить судорожную активность, в первую очередь, субклиническую, не сопровождающуюся клиническими проявлениями. Известно, что судорожная активность ухудшает неврологический прогноз детей, перенесших гипоксически-ишемическую энцефалопатию. аЭЭГ обладает рогностической ценностью эффективности лечебной гипотермии которая выражается в восстановлении тренда до прерывистого паттерна.
Таким образом, авторами установлено, что понижение температуры мозга способно ограничить развитие всех основных патогенетических механизмов повреждения нейронов головного мозга, то есть системная лечебная гипотермия вызывает регресс неврологических нарушений, способствуя довольно быстрому восстановлению структур ЦНС и значительно меньшему их повреждению в результате перенесенной интранатальной асфиксии.
Источник: «Особенности ЭЭГ новорожденных с церебральной ишемией после терапевтической гипотермии» И.Г. Хмелевская, Н.С. Разинькова, О.Г. Бец, А.В. Серёжкина, Т.А. Миненкова, С.Г. Боева
http://vestnik.volgmed.ru/ru/issue/322/ №3 2019 (71)
https://www.volgmed.ru/uploads/journals/articles/1570428099-vestnik-2019-3-3419.pdf (статья)
Метки: научные исследования, неонатология
06.04.2020
Церебральная ишемия у новорожденных детей
ЦЕРЕБРАЛЬНАЯ ИШЕМИЯ — диагноз, который могут поставить врачи новорожденным малышам в роддоме. Возникает она из-за недостаточного снабжения клеток головного мозга кислородом. Причина, способствующая этой нехватке, может появиться как во время беременности мамы, так и во время рождения ребенка.
Одним из первых тестов, которыми пользуются врачи сразу после рождения малыша — является всем известная оценка ребенка по шкале Апгар. По количеству баллов судят о состоянии малыша.
Самая легкая – это 1 степень, как правило, отмечается легкая неврологическая симптоматика, например, в виде повышенной возбудимости ребенка и малыш не нуждается в стационарном лечении. А вот при второй, особенно третей степени решается вопрос о госпитализации малыша в специализированное отделение стационара. Первый месяц — это острое состояние. Со второго месяца жизни до достижения 1 года идет период восстановления пострадавшей от ишемии нервной системы, и невролог в диагнозе гипоксически-ишемическое поражение цнс выделяет ведущие синдромы и лечение подбирает в соответствии с этим. Одно из тяжелых последствие церебральной ишемии – это детский церебральный паралич, делающий ребенка инвалидом детства.
В этом втором промежутке времени будет очень важно участие родителей в процессе восстановительного лечения. Необходимо наблюдение невролога, обязательны дополнительные ультразвуковые исследования головного мозга. По результатам осмотра и исследований невролог может направить вас с ребёнком на прием к остеопату, так же может назначит курс лекарственных препаратов. Чаще всего препараты эти из группы сосудистых, ноотропных препаратов, а также из группы витаминов или мочегонных. В некоторых сложных случаях малыши нуждается в повторной госпитализации в стационар для назначения противосудорожной терапии, внутримышечных инъекций и капельниц.
Необходимо наблюдение невролога, обязательны дополнительные ультразвуковые исследования головного мозга. По результатам осмотра и исследований невролог может направить вас с ребёнком на прием к остеопату, так же может назначит курс лекарственных препаратов. Чаще всего препараты эти из группы сосудистых, ноотропных препаратов, а также из группы витаминов или мочегонных. В некоторых сложных случаях малыши нуждается в повторной госпитализации в стационар для назначения противосудорожной терапии, внутримышечных инъекций и капельниц.
Что же требуется от родителей?
Во-первых -это внимательное отношение к своему малышу. Наблюдение за ребенком в течение дня, за его сном и бодрствованием, за его психическим и двигательным развитием, за реакцией на окружающее воздействие. Не пренебрегайте назначениями лечащего врача. При плановом посещении невролога рассказывайте о своих наблюдениях за ребенком, это поможет скорректировать назначения.
Такая информация может потребоваться и остеопату. После первичной консультации у остеопата, где отводится время на сбор всех имеющихся данных и непосредственную остеопатическую диагностику, определяется тактика ведения ребенка. Чаще одной процедуры коррекции найденных дисфункций бывает недостаточно, и тогда остеопат назначит повторный прием, который может быть спустя 1 -3 недели.
После первичной консультации у остеопата, где отводится время на сбор всех имеющихся данных и непосредственную остеопатическую диагностику, определяется тактика ведения ребенка. Чаще одной процедуры коррекции найденных дисфункций бывает недостаточно, и тогда остеопат назначит повторный прием, который может быть спустя 1 -3 недели.
Какие изменения после лечения у остеопата наблюдают родители у ребенка? Чаще всего это улучшение сна, уменьшение немотивированного плача, срыгиваний, положительные сдвиги в предречевом и моторном развитии. Невролог наблюдает положительную динамику при неврологическом осмотре, у него появляется возможность уменьшить лекарственную нагрузку на ребенка.
Автор публикации: Гореликова Елена Аркадьевна
Врач-остеопат, детский невролог.
Специалист Центра детского коррекционного развития и нейропсихологии
Группа компаний ИНФРА-М
В оценке структурно-функционального состояния респираторной и центральной нервной систем у новорожденных с отягощенным антенатальным анамнезом важная роль отводится исследованию аспирата из дыхательных путей [1, 4, 6]. Поэтому изучение липидов назофарингеального аспирата, участвующих в формировании сурфактантной и ликворной системы у детей при рождении, позволяет установить патогенез антенатально индуцированной патологии органов дыхания и головного мозга у потомства, матери которых перенесли реактивацию хронической цитомегаловирусной инфекции (ЦМВИ) во втором триместре беременности, неосложненной и осложненной угрозой невынашивания.
Поэтому изучение липидов назофарингеального аспирата, участвующих в формировании сурфактантной и ликворной системы у детей при рождении, позволяет установить патогенез антенатально индуцированной патологии органов дыхания и головного мозга у потомства, матери которых перенесли реактивацию хронической цитомегаловирусной инфекции (ЦМВИ) во втором триместре беременности, неосложненной и осложненной угрозой невынашивания.
Целью работы явилось изучение содержания общего холестерина (ОХС) и триглицеридов (ТГ) в назофарингеальном аспирате при церебральной ишемии средней степени тяжести у новорожденных от матерей с ЦМВИ в период беременности.
Материалы и методы исследования
Проводилось изучение содержания ОХС и ТГ в назофарингеальном аспирате у 233 доношенных новорожденных от матерей с физиологической беременностью, а также с латентным течением и реактивацией хронической ЦМВИ во втором триместре гестации. Обследованные дети были разделены на 5 групп.
В первую группу (контрольную) вошли 30 новорожденных, матери которых не имели осложнений в период беременности. При серологическом исследовании у женщин в сыворотках крови (парных) не выявлялись титры антител IgG и IgM к цитомегаловирусу (ЦМВ). Однако определялись титры антител IgG к вирусу простого герпеса 1 типа (ВПГ-1) 1:200-1:400 при отсутствии роста в динамике титров антител IgG к ВПГ-1 1:200-1:400 и индексе авидности антител IgG к ВПГ-1 более 65%.
При изучении липидов назофарингеального аспирата у детей с церебральной ишемией средней степени тяжести и внутриутробным развитием, осложненным хронической ЦМВИ, выделялись вторая, третья, четвертая и пятая группы, в каждой из которых было 2 подгруппы: подгруппа А – новорожденные от матерей, не имеющих угрозы невынашивания; подгруппа Б – дети, матери которых перенесли реактивацию хронической ЦМВИ во втором триместре гестации, осложненной угрозой невынашивания.
Вторую группу (основную) составили 50 новорожденных от матерей с латентным течением хронической ЦМВИ (титры антител IgG к ЦМВ 1:200-1:400, индекс авидности IgG к ЦМВ более 65%), ассоциированной с латентным течением герпесвирусной (ВПГ-1) инфекции (титры антител IgG к ВПГ-1 1:200-1:400, индекс авидности IgG к ВПГ более 65%) во втором триместре беременности. Во 2А и во 2Б подгруппы вошли по 25 детей.
Во 2А и во 2Б подгруппы вошли по 25 детей.
В третью группу вошли 50 детей, матери которых перенесли реактивацию хронической ЦМВИ (титры антител IgM к ЦМВ 1:200-1:400 без четырехкратного роста титров антител IgG к ЦМВ 1:200-1:400 и индекс авидности антител IgG к ЦМВ более 65%) на фоне латентной герпесвирусной инфекции (титры антител IgG к ВПГ-1 1:200-1:400 и индекс авидности IgG к ВПГ более 65%). Подгруппа 3А включала 25 детей, и 3Б – 25 пациентов..
Четвертая группа была представлена 51 новорожденным от матерей с реактивацией хронической ЦМВИ (титры антител IgM к ЦМВ 1:200-1:400, антитела IgG к ЦМВ 1:200-1:800 и индекс авидности IgG к ЦМВ более 65%) и с признаками латентной герпесвирусной инфекции (титры антител IgG к ВПГ-1 1:200-1:400, индекс авидности IgG к ВПГ более 65%). В 4А подгруппе находились 26 новорожденных, в 4Б подгруппе – 25 детей.
Пятую группу составили 52 новорожденных, матери которых перенесли реактивацию хронической ЦМВИ (титры антител IgМ к ЦМВ 1:200-1:400, четырехкратный рост титров антител IgG к ЦМВ 1:400-1:1600 и индекс авидности IgG к ЦМВ более 65%) на фоне латентного течения герпесвирусной инфекции (титры антител IgG к ВПГ-1 1:200-1:400, индекс авидности IgG к ВПГ более 65%). Подгруппа 5А состояла из 27 детей, подгруппа 5Б – из 25 новорожденных.
Подгруппа 5А состояла из 27 детей, подгруппа 5Б – из 25 новорожденных.
В основную группу были включены: 1) доношенные новорожденные с церебральной ишемией средней степени тяжести и антенатальным анамнезом, отягощенным латентным течением и реактивацией хронической ЦМВИ во втором триместре беременности, неосложненной и осложненной угрозой невынашивания; 3) дети, у которых внутриутробное развитие не было осложнено липидемией, ожирением 1-3 степени, эндокринными заболеваниями, среднетяжелой и тяжелой соматической и акушерской патологией у матерей во втором триместре беременности; 3) доношенные от матерей с беременностью, неосложненной другими ТОRCH-инфекциями.
Критерии исключения: 1) церебральная ишемия легкой и тяжелой степени у детей от матерей с одноплодной и многоплодной беременностью, а также с острыми и обострением хронических заболеваний, обусловленных другими инфекциями; 2) новорожденные, матери которых страдали среднетяжелой, тяжелой соматической и акушерской патологией в период беременности; 3) дети от матерей с истмико-цервикальной недостаточностью и аномалиями развития матки; 4) крупные новорожденные и дети, рожденные от матерей с помощью операции кесарева сечения; 4) дети от матерей, которые отказались участвовать в настоящем исследовании.
При установлении формы хронической ЦМВИ и активности инфекционного процесса у матерей во втором триместре беременности использовали иммуноферментный анализ (реагенты ЗАО «Вектор-Бест»), а индекса авидности антител IgG к ЦМВ и IgG к ВПГ-1 – «Вектор ЦМВ – IgG – авидность» и «Вектор ВПГ – IgG – авидность» (Россия).
Диагностика формы ЦМВИ у матерей во втором триместре беременности осуществлялась в парных сыворотках крови (при первом обследовании и через 12-14 дней) с помощью наборов реагентов ЗАО «Вектор-Бест», а индекса авидности антител IgG к ЦМВ и IgG к ВПГ-1 – «ВекторЦМВ − IgG – авидность» и «Вектор ВПГ − IgG – авидность» (Россия). Забор назофарингеального аспирата для биохимического анализа у новорожденных включал следующие этапы:
- после рождения ребенка с кожи носогубного треугольника и наружной части носа стерильным ватным тампоном удалялись частицы амниотической жидкости и мекониальные массы;
- для получения назофарингеального аспирата к стерильному шприцу присоединялось устройство, состоящее из мягкого полихлорвинилового зонда [7];
- осуществлялось осторожное введение зонда в полость носа новорожденному;
- из носоглотки шприцем медленно насасывалось 2,5-3 мл биологической жидкости;
- полученная биологическая жидкость центрифугировалась на центрифуге при 1500 об/мин в течение 10 минут для получения её надосадочной части, в которой определялось содержание (ммоль/л) ОХС, ЛПВП, ЛПНП и ТГ с помощью стандартных наборов реагентов на анализаторе фирмы «Beckman Coulter, Inc» (США).

В работе учитывались требования Хельсинкской декларации Всемирной ассоциации «Этические принципы проведения медицинских исследований с участием человека в качестве субъекта» с поправками 2013 г. и нормативных документов «Правила надлежащей клинической практики в Российской Федерации», утвержденных Приказом №200н от 01.04.2016 МЗ РФ. Работа одобрена Комитетом по биомедицинской этике ДНЦ ФПД в соответствии с принципами конвенции о биомедицине и правах человека, а также общепризнанными нормами международного права, от всех здоровых и больных лиц было получено информированное согласие.
Статистическая обработка и анализ данных осуществлялась с использованием стандартного пакета прикладных программ Statistica 6.1. Анализируемые в работе количественные данные имели нормальное распределение, поэтому рассчитывалась достоверность различий значений по Стьюденту − вычисление средней арифметической (М), средней ошибки (m). Во всех процедурах статистического анализа критический уровень значимости нулевой статистической гипотезы (p) принимался равным 0,05.
Результаты исследования и их обсуждение
Из таблицы 1 видно, что в носоглоточном аспирате у новорожденных 2А, 3А и 4А подгрупп по сравнению с первой группой не обнаруживались достоверные изменения уровня ОХС и ТГ. У детей 5А подгруппы в сопоставлении с контролем отсутствовали достоверные изменения содержания ТГ, но в тоже время статистически достоверно (р<0,01) снижалась концентрация ОХС. Вышеуказанные изменения липидного спектра назофарингеального аспирата у доношенных новорожденных c отягощенным антенатальным анамнезом могут отражать негативное влияние высокого иммунного ответа матерей на ЦМВ, ассоциированного с ростом токсичности аспирированных околоплодных вод [1]
Таблица 1
Изменение содержания ОХС и ТГ при церебральной ишемии средней степени тяжести у доношенных новорожденных от матерей с латентным течением и реактивацией хронической ЦМВИ во втором триместре беременности (М±m)
|
Исследуемые группы |
Биохимические показатели, ммоль/л |
|
|
ОХС |
ТГ |
|
|
Первая группа |
0,250±0,016 |
0,142±0,008 |
|
2А подгруппа |
0,246±0,015 р1>0,05 |
0,143±0,007 р1>0,05 |
|
3А подгруппа |
0,234±0,017 р1>0,05; p2>0,05 |
0,148±0,008 р1>0,05; p2>0,05 |
|
4А подгруппа |
0,214±0,016 р1>0,05; p2>0,05; p3>0,05 |
0,156±0,009 р1>0,05; p2>0,05; p3>0,05 |
|
5А подгруппа |
0,189±0,015 р1<0,01; p2>0,05; p3>0,05; p4>0,05 |
0,165±0,010 р1>0,05; p2>0,05; p3>0,05; p4>0,05 |
Примечание: р1 – уровень значимости различий по сравнению с показателями первой группы; р2 – то же с показателями 2А подгруппы; р3 – то же с показателями 3А подгруппы; р4 – то же с показателями 4А подгруппы.
Сравнение содержания липидов в назофарингеальном аспирате у детей 2Б и 3Б подгрупп с таковым у здоровых новорожденных не выявили статистически значимых различий концентрации ОХС и ТГ. У пациентов 4Б и 5Б подгрупп, напротив, отмечалось достоверное падение уровня ОХС на фоне роста концентрации ТГ (табл. 2).
Таблица 2
Изменение содержания ОХС и ТГ при церебральной ишемии средней степени тяжести у доношенных новорожденных от матерей с латентным течением и реактивацией хронической ЦМВИ во втором триместре беременности, осложненной угрозой невынашивания (М±m)
|
Исследуемые группы |
Биохимические показатели, ммоль/л |
|
|
ОХС |
ТГ |
|
|
Первая группа |
0,250±0,016 |
0,142±0,008 |
|
2Б подгруппа |
0,233±0,015 р1>0,05 |
0,144±0,008 р1>0,05 |
|
3Б подгруппа |
0,221±0,016 р1>0,05; p2>0,05 |
0,151±0,009 р1>0,05; p2>0,05 |
|
4Б подгруппа |
0,193±0,015 р1<0,05; p2>0,05; p3>0,05 |
0,169±0,009 р1<0,05; p2>0,05; p3>0,05 |
|
5Б подгруппа |
0,146±0,010 p1<0,001; p2>0,05; p3>0,05; p4>0,05 |
0,198±0,009 p1<0,001; p2>0,05; p3>0,05; p4>0,05 |
Примечание: р1 – уровень значимости различий по сравнению с показателями первой группы; р2 – то же с показателями 2Б подгруппы; р3 – то же с показателями 3Б подгруппы; р4 – то же с показателями 4Б подгруппы./133/133.jpg)
Снижение содержания ОХС и увеличение ТГ в носоглоточном аспирате при церебральной ишемии средней степени тяжести у новорожденных 5Б подгруппы по сравнению с таковым у детей контрольной группы, по-видимому, связано с ацидозом и токсичностью аспирированной амниотической жидкости [1, 6], которые влияют на активность ферментных систем и строение альвеолоцитов и эндотелиоцитов лёгких [5, 8], а также на структурно-функциональную организацию эндотелия и эпендимоцитов ликворных путей головного мозга [2, 3] при реактивации хронической ЦМВИ у их матерей во втором триместре беременности, осложненном угрозой невынашивания. В то же время четко выраженные различия (р<0,05) между содержанием ОХС и ТГ в 5Б и 5А подгруппах указывают на значение угрозы невынашивания инфекционного генеза в стимуляции дислипидемии в носоглоточном аспирате в результате избыточного поступления антигенов возбудителей и их токсинов через гематоплацентарный барьер в околоплодные воды.
Выводы
- У доношенных новорожденных с церебральной ишемией средней степени тяжести и антенатальным анамнезом, отягощенным латентным течением хронической ЦМВИ (титры антител IgM к ЦМВ 1:200-1:400, титры антител IgG к ЦМВ 1:200-1:400 и индекс авидности IgG к ЦМВ более 65%) на фоне хронической герпесвирусной инфекции во втором триместре гестации, неосложненном и осложненном угрозой невынашивания, в сопоставлении со здоровыми детьми аналогичного возраста не наблюдается достоверных изменений ОХС и ТГ в носоглоточном аспирате.

- Церебральная ишемия средней степени тяжести у детей, матери которых перенесли реактивацию хронической ЦМВИ с титрами антител IgM к ЦМВ 1:200-1:400, без четырехкратного роста титров антител IgG 1:400-1:800 и индексом авидности IgG к ЦМВ более 65% во втором триместре гестации, по сравнению с детьми от матерей с физиологическим течением беременности, сопровождается тенденцией к снижению в назофарингеальном аспирате ОХС и к увеличению содержания ТГ.
- При церебральной ишемии средней степени тяжести у новорожденных с антенатальным анамнезом, отягощенным реактивацией хронической ЦМВИ (титры антител IgM к ЦМВ 1:200-1:400, титры антител IgG к ЦМВ 1:400-1:1600 и индекс авидности IgG к ЦМВ более 65%) во втором триместре беременности и угрозой невынашивания, по сравнению со здоровыми детьми и пациентами с аналогичной патологией центральной нервной системы, матери которых перенесли острую фазу хронической ЦМВИ (титры антител IgM к ЦМВ 1:200-1:400, титры антител IgG к ЦМВ 1:200-1:800 и индекс авидности IgG к ЦМВ более 65%) во втором триместре гестации, неосложненной угрозой невынашивания, в носоглоточном аспирате снижается концентрация ОХС и регистрируются более высокие показатели ТГ.
 Это снижает устойчивость органов дыхания и центральной нервной системы у новорожденных к неблагоприятным факторам в период их внутриутробного и постнатального развития.
Это снижает устойчивость органов дыхания и центральной нервной системы у новорожденных к неблагоприятным факторам в период их внутриутробного и постнатального развития.
Церебральная ишемия у новорожденных: симптомы, степени, лечение, последствия
Церебральная ишемия у новорожденных – заболевание, вызванное кислородным голоданием, сопровождающееся поражением головного мозга. Без терапии оно приводит к тяжелым осложнениям. Своевременная диагностика и медицинская помощь предупреждают патологические изменения в мозге и увеличивают шансы ребенка на нормальную жизнь.Причины церебральной ишемии у новорожденных
Заболевание может развиться как на последних сроках беременности, так и в момент родов. Чаще всего кислородное голодание возникает в результате остановки дыхания в родах, гипоксии плода, тугого обвития пуповиной. Также церебральная ишемия распространена среди недоношенных детей, так как их сосудистая система до конца не сформирована.
Второе название церебральной ишемии новорожденных – гипоксически-ишемическая энцефалопатия
Другие причины болезни:
- предлежание или преждевременная отслойка плаценты, нарушение кровообращения в ней;
- стремительные или затянувшиеся роды;
- маловодие;
- удушение плода в ходе родов в результате обвития пуповиной;
- врожденные пороки развития сердечно-сосудистой системы младенца;
- нарушение целостности пуповины в момент родов;
- инфицирование при родовом процессе;
- плацентарная недостаточность;
- обильные кровотечения у младенца после появления на свет.

К факторам риска принадлежит недоношенность, рождение малыша на позднем сроке, более 42 недель, многоплодная беременность, возраст роженицы более 35 лет. На состояние сосудистой системы младенца также влияет поздний токсикоз, хронические заболевания беременной, в частности гипертония или гипохромная анемия, высокая температура у женщины во время родов, нездоровый образ жизни матери, бактериальные инфекции.
Симптомы
При церебральной ишемии мозг младенца не может функционировать нормально. На начальных этапах признаки могут быть незаметны, новорожденный не отличается от здоровых детей, хотя болезнь развивается сразу после рождения. Отклонения проявляются по мере прогрессирования патологии.
Симптомы церебральной ишемии наиболее выражены у глубоко недоношенных детей
Основные признаки:
- высокая судорожная активность;
- проявления синдрома перевозбуждения – беспокойность, плохой сон, капризность, плаксивость;
- отставание ребенка в развитии;
- проявления синдрома угнетения – снижение мышечного тонуса, вялость, ухудшение рефлексов глотания и сосания,
- может быть заметна разница в движениях рук и ног слева и справа.

В более тяжелых случаях вероятно обморочное или коматозное состояние. Среди их симптомов следует отметить отсутствие рефлексов и реакций на раздражители, нарушение пульса и дыхания, снижение давления. Малыш нуждается в экстренной помощи медиков.
Степени
Клинические проявления церебральной ишемии во многом зависят от стадии болезни:
- I степень. Это наиболее благоприятная по прогнозам стадия. Признаки болезни проявляются в первые дни жизни младенца, но исчезают в течение 3-5 суток. Это плаксивость, беспокойство, повышенный тонус мышц, вялость.
- II. Состояние ребенка тяжелое. Может быть отсутствие движений в руке и ноге с одной стороны.
- III. Самая тяжелая и неблагоприятная с точки зрения прогноза стадия. Функции дыхания нарушены, из-за чего младенец нуждается в подключении к аппарату искусственной вентиляции легких. У малыша снижается давление, замедляется пульс, возникают судороги, вероятна кома.
Признаки последней стадии заметны сразу. Жизнь малыша полностью зависит от оперативности медперсонала.
Жизнь малыша полностью зависит от оперативности медперсонала.
Диагностика
Заболевание обнаруживается неонатологом непосредственно при осмотре новорожденного по симптомам. Врач замечает нарушение рефлексов. Для подтверждения диагноза потребуется следующее обследование:
- анализ крови – клинический, биохимический, определение уровня кислорода и углекислого газа, коагулограмма;
- нейросонография;
- при необходимости — КТ головного мозга.
По данным обследования выявляется ишемические очаги в головном мозге, нарушения в анализах крови.
Лечение
Лечебные мероприятия зависят от тяжести и времени болезни, но основная их цель остается неизменной – нормализовать мозговое кровообращение, предупредить патологические изменения.
Если у ребенка лишь незначительные признаки поражения, то медикаментозная терапия не нужна или назначаются ноотропные препараты (энцефабол и т.д.) После выписки ребенок должен наблюдаться у невролога, так как существует риск отклонений.
К лечению новорожденного может быть привлечен невропатолог, нейрохирург
На 2 и 3 стадии не обойтись без медикаментозной терапии, а иногда и хирургического вмешательства. Для лечения младенца применяются препараты таких групп:
- ноотропные — для питания клеток головного мозга;
- противосудорожные – снижают судорожную активность;
- общеукрепляющие – витаминные комплексы для поддержания нормальной работы мозга и организма;
- кардиотонические, гипертензивные – улучшают периферическое кровообращение.
Ни в коем случае нельзя подбирать препараты для лечения самостоятельно.
Если состояние малыша тяжелое, то его немедленно переводят в реанимацию. При тромбозе тромб, ставший причиной кислородного голодания, удаляется в ходе операции. После малыша ожидает длительной период реабилитации.
Последствия
Для церебральной ишемии характерны необратимые изменения в клетках головного мозга. Если не остановить прогрессирование патологии, то вероятен летальный исход.
Если не остановить прогрессирование патологии, то вероятен летальный исход.
К счастью, церебральная ишемия 1 степени проходит без серьезных осложнений. Ребенок может часто жаловаться на головную боль, повышенную усталость, плохую память, малышу присуща гиперактивность.
Последствия последних стадий:
- гиподинамия – снижение двигательной активности;
- головная боль;
- судороги, эпилепсия;
- ДЦП;
- отставание в умственном и физическом развитии.
Если начать лечебные мероприятия на раннем сроке, пока нет серьезных последствий, то можно нормализовать самочувствие ребенка, избежать необратимых осложнений. Период реабилитации после выздоровления младенца занимает 6-12 месяцев.
Специального лечения для восстановления поврежденных клеток мозга не существует, поэтому важно как можно раньше вывить церебральную ишемию. Состояние ребенка зависит от продолжительности кислородного голодания. Чем тяжелее гипоксия, тем печальнее прогнозы.
Смотрите далее: у ребенка кружится голова
(PDF) Cerebral hemodynamics in high-risk infants during the neonatal period
48
ОРИГИНАЛЬНЫЕ СТАТЬИ ПЕРИНАТОЛОГИЯ И НЕОНАТОЛОГИЯ
РОССИЙСКИЙ ВЕСТНИК ПЕРИНАТОЛОГИИ И ПЕДИАТРИИ, 2, 2016
ROSSIYSKIY VESTNIK PERINATOLOGII I PEDIATRII, 2, 2016
и у недоношенных 3-й группы. Таким образом, ди-
намический контроль на протяжении неонатально-
го периода позволил выявить замедленный процесс
восстановления церебральной гемодинамики у детей
с осложненным перинатальным периодом, особенно
при сочетанном воздействии повреждающих факто-
ров (негативное влияние гипоксии/ишемии, рожде-
ние оперативным путем, недоношенность).
Заключение
Неблагоприятное течение перинатального перио-
да, особенно при сочетанном влиянии на организм
плода и новорожденного гипоксии/ишемии, опера-
тивного родоразрешения, недоношенной беремен-
ности, может приводить к стойкому нарушению це-
ребрального кровотока. Углубленное исследование
Углубленное исследование
различных звеньев гемодинамической адаптации,
в частности кровоснабжения мозга с оценкой каче-
ственных и количественных показателей, дает возмож-
ность раннего выявления нарушений постнатальной
перестройки гемодинамики (нарушение резистент-
ности сосудистого русла, изменение линейных ха-
рактеристик артериального и венозного кровотока).
Дети, рожденные путем кесарева сечения и перенес-
шие гипоксию/ишемию, особенно недоношенные,
составляют группу высокого риска по развитию дез-
адаптации в перинатальном периоде и формированию
патологических состояний в последующие возрастные
периоды. Ранняя диагностика структурно-гемодина-
мических нарушений головного мозга дает основа-
ние для своевременного расширенного обследования
ЦНС и возможность эффективной медикаментозной
коррекции дисфункциональных состояний с целью
предотвращения декомпенсации и связанных с ней
осложнений, что направлено на улучшение невроло-
гического статуса детей из группы высокого риска.
ЛИТЕРАТУРА
(REFERENCES)
1. Стародубов В.И., Цыбульская И.С., Суханова Л.П. Охрана
здоровья матери и ребенка как приоритетная проблема
современной России. Современные медицинские тех-
нологии 2009; 2: 11–16. (Starodubov V.I., Tsybul’skaya I.S.,
Sukhanova L.P. Maternal and child health as a priority prob-
lem of modern Russia. Sovremennye meditsinskie tekhnologii
2009; 2: 11–16.)
2. Суханова Л.П., Кузнецова Т.В. Перинатальные проблемы
воспроизводства населения России (по данным анализа
статистических форм №№13,32). Социальные аспекты
здоровья населения 2010; 4: 16. http://vestnik.mednet.
ru/component/option,com_weblinks/Itemid,23/lang,ru/
(Sukhanova L.P., Kuznetsova T.V. Perinatal problems of re-
production of the population of Russia (according to the
analysis of statistical forms №№13,32). Sotsial’nye aspekty
zdorov’ya naseleniya 2010; 4: 16. http://vestnik.mednet.ru/
http://vestnik.mednet.ru/
component/option,com_weblinks/Itemid,23/lang,ru/)
3. Raju Tonse N.K., Ariagno R.L, Higgins R. et al. Research in Neo-
natology for the 21st Century. Pediatrics 2005; 115: 468–474.
4. Савельева Г.М., Шалина Р.И., Сичинава Л.Г. и др. Акушер-
ство. М.: ГЭОТАР-Медиа, 2010; 656. (Savel’eva G.M., Sha-
lina R.I., Sichinava L.G. et al. Obstetrics. M.: GEHOTАR-
Media, 2010; 656.)
5. Степаненко Т.А., Павлова Т.В., Петрухин В.А. и др. Про-
блемы перинатальных потерь при операции кесарева се-
чения. Системный анализ и управление в биомедицин-
ских системах 2009; 8: 1: 41–44. (Stepanenko T.А., Pavlova
T.V., Petrukhin V.А. et al. Problems of perinatal loss at caesar-
ean section. Sistemnyj analiz i upravlenie v biomeditsinskikh
sistemakh 2009; 8: 1: 41–44.)
6. Signore C., Klebanoff M. Neonatal morbidity and mortality
after elective cesarean delivery. Clin Perinatol 2008; 35: 2:
361–371.
7. Bodner K., Wierrani F., Grunberger W. et al. Influence of the
mode of delivery on maternal and neonatal outcomes: a com-
parison between elective cesarean section and planned vaginal
delivery in a low-risk obstetric population. Arch Gynecol Ob-
stet 2011; 283:1193–1198.
8. Кулаков В.И., Барашнев В.И. Новорожденные высоко-
го риска. М.: ГЭОТАР-Медиа 2006: 528. (Kulakov V.I.,
Barashnev V.I. Newborns at high risk. M.: GEHOTАR-
Media 2006: 528.)
9. Суханова Л.П. Здоровье новорожденных детей России.
М.: Канон+ 2007; 324. (Sukhanova L.P. Health Russian
newborns. M.: Kanon+ 2007; 324.)
10. Гавриков Л.К., Прохорова Л.И., Давыдова А.Н. и др. Из-
учение особенностей формирования соматической
патологии у детей с перинатальными нарушениями
церебральных механизмов регуляции. Бюллетень Вол-
гоградского научного центра РАМН 2009; 4: 37–40.
(Gavrikov L. K., Prokhorova L.I., Davydova А.N. et al. The
K., Prokhorova L.I., Davydova А.N. et al. The
study of the formation of somatic pathology in children
with perinatal lesions of the cerebral mechanisms of regula-
tion. Byulleten’ Volgogradskogo nauchnogo tsentra RАMN
2009; 4: 37–40.)
11. Соколовская Т.А. Влияние перинатальной патологии
на заболеваемость и инвалидизацию детей. Автореф.
дисс. … канд. мед. наук. М., 2009; 25. (Sokolovskaya T.А.
Influence of perinatal pathology morbidity and disability
of children. Аvtoref. diss. … kand. med. nauk. M., 2009; 25.)
12. Медведев М.И., Дегтярева М.Г., Горбунов А.В. и др. По-
следствия перинатальных гипоксически-ишемических
поражений головного мозга у доношенных новоро-
жденных: диагностика и принципы восстановительного
лечения. Педиатрия 2011; 90: 1: 66–70. (Medvedev M.I.,
Degtyareva M.G., Gorbunov А.V. et al. The consequences
of perinatal hypoxic-ischemic brain damage in preterm in-
fants: diagnosis and principles of rehabilitation treatment.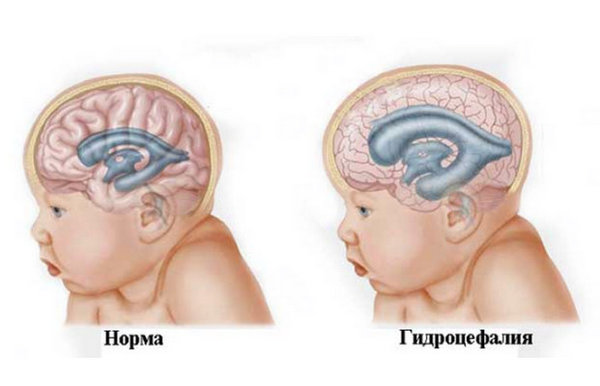 Pe-
Pe-
diatriya 2011; 90: 1: 66–70.)
13. Зедгенизова Е.В., Иванов Д.О., Прийма Н.Ф. и др. Особен-
ности показателей мозгового кровотока и центральной
гемодинамики у детей, родившихся с задержкой внутри-
утробного развития (ЗВУР). Бюллетень федерального
центра сердца, крови и эндокринологии им. В.А. Алма-
зова 2012; 3: 76–82. (Zedgenizova E.V., Ivanov D.O., Prijma
N.F. et al. Features indices of cerebral blood flow and cen-
tral hemodynamics in children born with intrauterine growth
retardation. Byulleten’ federal’nogo tsentra serdtsa, krovi i
ehndokrinologii im. V.А. Аlmazova 2012; 3: 76–82.)
14. Gerda van Wezel-Meijler. Neonatal cranial ultrasonography.
Springer, 2007; 168.
15. Benavides-Serralde A., Scheier M., Cruz-Martinez R. et al.
Changes in central and peripheral circulation in intrauterine
growth-restricted fetuses at different stages of umbilical artery
Лечение церебральной ишемии у новорожденных 1, 2 и 3 степени: симптомы, признаки и последствия
Церебральная ишемия — нарушение работы головного мозга, развивающееся вследствие длительной нехватки кислорода. После кислородного голодания сосуды мозга сужаются или полностью закупориваются тромбами.
После кислородного голодания сосуды мозга сужаются или полностью закупориваются тромбами.
В современной неврологии ишемия новорожденных детей признана одной из наиболее острых проблем. Вызвано это в первую очередь тем, что способов эффективного лечения болезни пока недостаточно.
Общие сведения
Гипоксия или недостаток кислорода во время беременности или процесса родов может привести к негативным последствиям для мозга ребенка.
Ишемия у взрослых также крайне опасна. Особенно это относится к случаям несвоевременной диагностики и отложенного или некорректного лечения.
Классификация по степени тяжести
Церебральная ишемия в медицине делится на степени в зависимости от уровня поражения мозга:
Церебральная ишемия 1 степени. Неврологические нарушения выражены неявно, могут наблюдаться следующие симптомы:
- головные боли, ощущение постоянной тяжести в голове;
- общая слабость, чувство непреходящей усталости;
- уменьшение концентрации внимания, сбои памяти;
- бессонница;
- эмоциональная нестабильность;
- у новорожденных детей — нестандартное возбуждение или угнетение в первую неделю после рождения.

Симптомы на этой стадии не имеют ярко выраженной специфики, распознать у больного с подобными жалобами ишемию 1-ой степени не всегда возможно.
Сами больные редко обращаются за медицинской помощью, объясняя самочувствие переутомлением.
Между тем, именно на этой стадии церебральная ишемия относительно легко поддается лечению. Возможно не просто снять текущие симптомы, но и предотвратить ухудшение ситуации.
Церебральная ишемия 2 степени. Следующая степень заболевания отличается более серьезными симптомами. Они означают и более глубокие неврологические нарушения. Среди них:
- головокружения;
- глубокие нарушения памяти;
- неустойчивость при передвижениях;
- нарушения привычных движений;
- у новорожденных детей могут быть судороги.
На 2-ой ступени церебральной ишемии может быть полностью потеряна трудоспособность. Вызвано это возникновением в тканях мозга очаговых поражений. Способности к физической работе утрачиваются вследствие нарушения координации. Умственный труд также перестает быть возможным из-за поражения мозга и возникновения патологических рефлексов.
Умственный труд также перестает быть возможным из-за поражения мозга и возникновения патологических рефлексов.
Церебральная ишемия 3 степени. На этой стадии болезни нарушения мозговых функций крайне выражены. Среди симптомов выделяют:
- полная потеря трудоспособности;
- невозможность самообслуживания;
- частые обмороки;
- у новорожденных детей — нарушения слуха и зрения, судорожные припадки.
3-я степень ишемии головного мозга может характеризоваться отсутствием сформулированных жалоб от пациента. Для неврологов постановка диагноза на этой стадии не вызывает затруднений.
Церебральная ишемия у недоношенных детей
Механизм развития заболевания у недоношенных отличается от детей, которые родились полностью доношенными. Связано это с тем, что в первом случае мозг еще не сформирован и не устойчив к повреждениям.
Кроме того, зачастую появление на свет недоношенного ребенка сопровождается и другими проблемами в сфере неврологии. Это одновременно затрудняет постановку диагноза и может усложнить лечение.
Это одновременно затрудняет постановку диагноза и может усложнить лечение.
Болезни матери во время беременности могут отразиться в той или иной мере на ребенке. Одно из таких заболеваний — парез лицевого нерва у новорожденных. К счастью на этом этапе жизни малыша данное заболевание излечимо. Узнайте как.
Также новорожденному еще в роддоме может быть поставлен диагноз внутричерепная гипертензия. Каковы признаки этого заболевания и как проводить лечение рассказано в этой статье.
Симптомы у новорожденных детей
Среди признаков ишемии у новорожденных различают следующие:
- повышенная возбудимость, усиление мышечных рефлексов, тремор;
- синдром угнетения ЦНС. Понижение мышечного тонуса, ослабление рефлексов.
- синдром гидроцефалии;
- судороги различной степени выраженности.
Постановка диагноза ишемии головного мозга всегда базируется на результатах УЗИ исследования, врачебного осмотра, включающего исследование рефлексов.
Хроническая церебральная ишемия
Хроническая стадия чаще встречается у пожилых людей. Вызвана она необратимыми изменениями тканей головного мозга. Основными факторами перехода церебральной ишемии в хроническую стадию врачи считают:
- атеросклероз;
- артериальную гипертензию.
Сосуды мозга сужаются из-за тромба или склеротической бляшки, что вызывает недостаток кислорода, а затем ишемию. Клинические проявления заболевания достаточно разнообразны, что усложняет своевременную постановку диагноза.
Причины
Среди причин возникновения ишемии головного мозга у новорожденных главнейшей считается нехватка кислорода либо во время беременности, либо в процессе родов.
Для взрослых причин болезни значительно больше:
- атеросклероз сосудов головного мозга;
- сердечная недостаточность;
- увеличение вязкости крови;
- нарушения ритма сердечной деятельности.
Все эти заболевания способствуют ухудшению кровотока в сосудах, питающих мозг. Это практически неизбежно вызывает ишемию.
Это практически неизбежно вызывает ишемию.
Признаки у детей до года
В большинстве случаев у новорожденных детей диагностируется первая стадия ишемии мозга. Она проходит уже через несколько дней после рождения. Признаки церебральной ишемии у детей могут быть следующими:
- при легкой стадии повышенное угнетение или возбуждение центральной нервной системы.
- На среднетяжелой стадии могут наблюдаться судороги.
- Тяжелая степень может вызвать нарушения зрения и слуха, кому.
Лечение и реабилитация детей
При лечении церебральной ишемии у новорожденных детей главной задачей является восстановление нарушенного кровообращения мозга. Все неповрежденные участки сосудов стимулируются для максимально эффективной работы.
1-ая степень заболевания корректируется при помощи специального массажа. Врач даже может не счесть нужным назначение лекарственных средств.
Все последующие стадии ишемии лечатся исключительно под медицинским надзором и в зависимости от симптомов. Откладывать лечение нельзя — это поможет избежать огромных проблем в будущем.
Откладывать лечение нельзя — это поможет избежать огромных проблем в будущем.
Лечат ишемию головного мозга следующими препаратами:
- сосудорасширяющими, которые улучшают мозговое кровоснабжение;
- ноотропными, способствующими мозговой деятельности;
- витаминами;
- мочегонными.
Если случай особо сложен, ребенка госпитализируют с назначением противосудорожного лечения, капельниц и внутримышечных инъекций.
Родители должны неукоснительно соблюдать все назначения. Ребенку с ишемией показан расслабляющий массаж, ванночки с успокаивающими сборами и запрет на посещение людных мест. В некоторых случаях назначают электрофорез с папаверином.
Роль массажа при лечении
На первой стадии ишемии головного мозга массаж является основным способом лечения. Помимо своего основного предназначения, лечебный массаж благотворно влияет на мышечный тонус и самочувствие ребенка.
Самостоятельно лечебный массаж проводить нельзя, это должен делать специалист. Наиболее эффективно проведение массажа 4 раза в первый год жизни. Интервал между курсами должен составлять 3 месяца. Лечебный массаж способствует
Наиболее эффективно проведение массажа 4 раза в первый год жизни. Интервал между курсами должен составлять 3 месяца. Лечебный массаж способствует
- расслаблению нервной системы;
- улучшению мышечного тонуса;
- улучшению общего состояния ребенка.
Трудные роды или некачественная родовспомогательная деятельность персонала приводит к тяжелым последствиям. Как следствие может произойти субарахноидальное кровоизлияние у новорожденного. Всегда ли диагностируется данное кровоизлияние? Чем можно помочь малышу?
При неправильных действиях акушерки происходит силовое воздействие на плечо младенца, после чего у новорожденного развивается плексит плечевого сустава. О данном заболевании можно прочитать тут.
О том что происходит с новорожденным при наличии гематомы головного мозга, как ее распознать читайте в материале http://gidmed.com/bolezni-nevrologii/sherepno-mozgovye-travmy/gematoma-golovnogo-mozga.html
Последствия
Среди возможных последствий легкой и среднетяжелой церебральной ишемии головного мозга у новорожденных:
- нарушения сна;
- головные боли;
- чувство усталости и раздражительность;
- сложности при учебе, недостаток концентрации.

Тяжелая степень вызывает в будущем
- умственную неполноценность;
- невозможность ходить;
- эпилепсию.
Необходимо внимательно изучать поведение новорожденного ребенка для своевременного выявления симптомов церебральной ишемии.
Заболевание 1-ой степени хорошо поддается лечению и не оставляет последствий. Чем больше времени пройдет с появления первых симптомов, тем сложнее будет лечение.
Взрослые должны максимально оградить себя от факторов риска. Это ожирение, злоупотребление алкоголем, курение и стрессы.
Научные медицинские знания по хронической церебральной ишемии продемонстрированы в этом видео:
головного мозга, 2, последствия, что это такое, младенца, грудничка, ишемическая болезнь, детей
Ишемия головного мозга у новорожденного – патологическое состояние, связанное с недостаточным поступлением кислорода. Резкое сужение или закупорка мелких сосудов отрицательно сказывается на кровообращении. Независимо от причин, несвоевременно начатая терапия приводит к печальным последствиям.
Резкое сужение или закупорка мелких сосудов отрицательно сказывается на кровообращении. Независимо от причин, несвоевременно начатая терапия приводит к печальным последствиям.
Проявления ишемии у грудничков
Ишемия структур головного мозга – это такое заболевание, которое сопровождается у новорожденных гипоксией (пониженное содержание кислорода в тканях) или аноксией (отсутствие кислорода в тканях), что приводит к острому кислородному голоданию. В 40% случаев поражения ЦНС в детском возрасте связаны с перинатальной патологией.
Недоношенность – ведущий фактор, с которым ассоциируется морфофункциональная незрелость мозговых структур, из-за чего повышается риск возникновения ишемии головного мозга у недоношенных детей при преждевременных родах. Вследствие кислородного голодания развивается некроз (отмирание тканей), что приводит к очаговым и диффузным структурным изменениям мозгового вещества. В зависимости от локализации и характера повреждений выделяют:
- Мультикистозную лейкомаляцию (диффузное поражение белого вещества гипоксической, ишемической этиологии).

- Субкортикальную (подкорковую) лейкомаляцию.
- Ишемический некроз (очаговый или диффузный).
Атрофические изменения мозговых структур выявляются в ходе инструментальной диагностики. При проведении Эхо-ЭГ (эхоэнцефалография) исследования в 80% случаев наблюдаются уплотнения в перивентрикулярной (около желудочков) области, в 20% случае картина дополняется расширением желудочков и пространств, в которых находится цереброспинальная жидкость (протоки, субарахноидальное пространство).
Нередко (около 18% случаев) ишемия, поразившая головной мозг у ребенка, протекает без явных отклонений в структуре мозгового вещества. Исследование ЭЭГ (электроэнцефалография) у недоношенных младенцев в 73% случаев показывает непостоянный характер биоэлектрической активности мозга с преобладанием медленных, низкоамплитудных волн, периодически чередующихся с кратковременно продолжающимися регулярными волнами.
У 23% детей выявляются разноплановые патологические паттерны (схемы-образцы) ЭЭГ и волны эпилептической природы в общем колебательном ритме.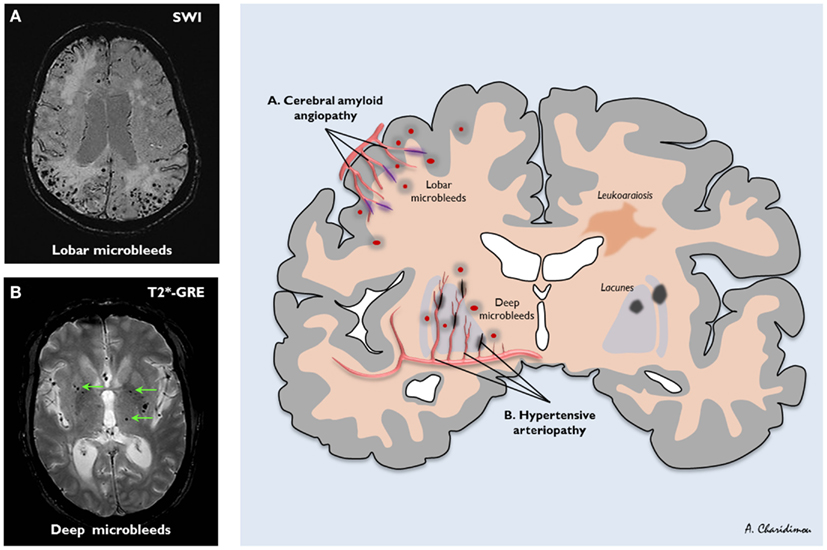 Редко (3% случаев) ЭЭГ не показывает существенных отклонений от нормы у детей с ишемией, протекающей в головном мозге.
Редко (3% случаев) ЭЭГ не показывает существенных отклонений от нормы у детей с ишемией, протекающей в головном мозге.
Лечебная терапия
Основная цель лечебной терапии при церебральной ишемии – нормализация мозгового кровообращения и устранение возникших последствий из-за кислородного голодания мозга. Ишемия у детей лечится в индивидуальном порядке. В данном случае учитывается срок гестации, степень поражения детского мозга, наличия у малыша других проблем со здоровьем и т.д.
Лечение первой стадии церебральной ишемии головного мозга не требует применения каких-либо медикаментозных препаратов. На данном этапе обходятся только лечебным массажем. Во время его выполнения происходит повышение тонуса мышц и улучшение кровообращения во всем организме, что благоприятным образом сказывается на общем самочувствии новорожденного. После массажа у ребенка нормализуется сон, его двигательная активность повышается.
Делать массаж самостоятельно не рекомендовано. В данном случае требуется обращаться к специалисту, который знает все тонкости. Проводить массаж нужно курсами. Их длительность подбирается индивидуально, но чаще всего она не превышает 10 сеансов. Всего в год следует пройти 3-4 курса массажа. Интервал между ними не должен превышать 3 месяцев.
В данном случае требуется обращаться к специалисту, который знает все тонкости. Проводить массаж нужно курсами. Их длительность подбирается индивидуально, но чаще всего она не превышает 10 сеансов. Всего в год следует пройти 3-4 курса массажа. Интервал между ними не должен превышать 3 месяцев.
В случае, даже если церебральную ишемию первой степени у ребенка удалось вылечить, малыш все равно нуждается в постоянном контроле врачей.
Лечение этого заболевания на 2-й и 3-й стадии у новорожденных проводится с применением мочегонных, ноотропных и сосудосуживающих препаратов. Прием таких медикаментов должен происходить под строгим контролем врача, а потому лечение в обязательном порядке должно проводиться только в стационарных условиях.
Необходимо понимать, что церебральная ишемия – это очень опасное заболевание, которое может проявлять себя различными симптомами. Первые 2-3 месяца после рождения ребенка, родителям нужно тщательно следить за его поведением. И в случае, если ребенка что-то беспокоит, его следует незамедлительно показать педиатру.
Если врач после осмотра малыша, выявит у него какие-либо отклонения, то требуется сразу же сдать все анализы. И после подтверждения диагноза проводить лечебную терапию.
Основные признаки заболевания
Ишемическая болезнь, поразившая головной мозг, у новорожденных сопровождается преимущественно неврологической симптоматикой. Оценка состояния новорожденного по шкале Апгар 2-5 баллов указывает на наличие интранатальной (во время родов) асфиксии. В особо тяжелых случаях возможно развитие коматозного состояния и тяжелое угнетение деятельности ЦНС, что требует незамедлительного проведения реанимационных мероприятий с подключением к аппарату искусственной вентиляции легких. Другие признаки:
- Судорожный синдром.
- Бульбарные расстройства. Нарушение функций глотания и сосания.
- Чередование мышечной гипотонии и мышечного гипертонуса пирамидного, пирамидно-экстрапирамидного типа.
- Спастическая тетраплегия. Частичный или полный паралич конечностей.
- Спастические тетрапарезы.
 Обессиливание моторной активности всех конечностей в результате нарушения функций нервной системы.
Обессиливание моторной активности всех конечностей в результате нарушения функций нервной системы. - Дистонические эпизоды (спазматическое сокращение мышц постоянного характера) с характерным застыванием в позе ассиметричного тонического шейного рефлекса.
- Гиперкинезы (непроизвольные движения одной или группы мышц) с атетозом (непроизвольные подергивания) кистей рук.
- Мышечная ригидность. Неподатливость, твердость мышц.
- Нарушение сна, частый плач.
Стоит обратить внимание на аномальный тонус мышц и тремор некоторых частей тела – подбородка, кистей рук. Оценка по шкале Infanib 12-20 баллов. Оценка спастичности по шкале Эшворта (Ashworth scale) 3-4 балла. Поражение структур нервной системы проявляется характерными синдромами:
- Усиленная нервно-рефлекторная возбудимость.
- Вегето-висцеральная дисфункция (расстройство нейроэндокринной регуляции).
- Мышечная дистония (спазматические сокращения мышц).
Статистика показывает, признаки церебральной ишемии, развивающейся в головном мозге у новорожденных, чаще носят неврологический характер. Интенсивность и выраженность проявлений неврологических симптомов зависит от характера и степени поражения мозговых структур.
Интенсивность и выраженность проявлений неврологических симптомов зависит от характера и степени поражения мозговых структур.
Перинатальные повреждения мозговых структур более выражены у недоношенных малышей (угнетение деятельности ЦНС – 18%, судорожная готовность – 19%, гипертензионно-гидроцефальный синдром – 9%). У младенцев более позднего срока гестации (33 недели) сильнее проявляются вегето-висцеральные расстройства (в 44% случаев). У доношенных детей чаще наблюдается усиленная нервно-рефлекторная возбудимость, развивающаяся на фоне гипертонуса мышц (в 31% случаев).
Симптомы и степени болезни
В медицине выделяют три степени тяжести гипоксии при аноксическом поражении головного мозга. Для каждой характерны свои признаки. Чем тяжелее заболевание, тем сильнее выражена симптоматика и тем раньше она проявляется после родов. В таблице ниже представлена симптоматика и особенности всех трех степеней ишемии:
| Степень ишемии | Характерные симптомы | Особенности течения болезни |
| 1 |
|
|
| 2 |
|
|
| 3 |
|
|
Степени патологии у новорожденных
Различают 3 степени ишемического поражения мозговых структур. Ишемия 1 степени в тканях головного мозга у новорожденных проявляется гиперактивностью, расстройством сна, ухудшением аппетита, беспричинным, частым плачем, повышенным тонусом мышц.
Симптомы ишемии 2 степени в тканях головного мозга у новорожденного включают судорожный синдром, повышение значений внутричерепного давления с сопутствующей симптоматикой. Наблюдается выпячивание родничка, непроизвольное запрокидывание головы, частый плач, неконтролируемые движения глазными яблоками, гидроцефалия (аномальное увеличение диаметра головы). Рефлексы вялые, периодически происходит замедление дыхания и сердечного ритма.
Для ишемии 3 степени характерно тяжелое угнетение функций ЦНС, вплоть до острой легочной недостаточности, отсутствия рефлексов, комы.
Причины развития
Ишемия в тканях головного мозга развивается вследствие кислородного голодания, все случаи патологии связаны с нарушением кровотока, вызванного закупоркой или сильным сужением сосудистого просвета. Основные причины:
- Соматические заболевания инфекционной этиологии у матери.
- Вредные привычки матери (курение, злоупотребление алкоголем).
- Родовые травмы, полученные плодом.
- Сбои в работе эндокринной системы у матери.
- Неблагоприятное течение беременности (токсикозы, угрозы выкидыша, преждевременные, осложненные роды).
Развитию ишемического поражения подвержены младенцы, которые в перинатальный период перенесли заболевания: легочная и сердечная недостаточность, паразитарные инвазии, опухоли мозга, нарушение свертываемости крови, другие патологии системы гемостаза.
Механизм развития церебральной ишемии
Кислород является жизненно необходимых для работы всех органов и систем в организме человека. Кровотоком он попадает к каждой клетке. Как только в организме наблюдается дефицит кислорода, происходит его своеобразное распределение по основным тканям. В первую очередь все питательные вещества поступают к сердцу и мозгу. В это время другие органы испытывают дефицит кислорода.
Кровотоком он попадает к каждой клетке. Как только в организме наблюдается дефицит кислорода, происходит его своеобразное распределение по основным тканям. В первую очередь все питательные вещества поступают к сердцу и мозгу. В это время другие органы испытывают дефицит кислорода.
Если асфиксия продолжительна во времени, организм не может справиться с такой нагрузкой и обеспечить достаточное питание тканей. Особенно остро на дефицит кислорода реагируют нервные клетки. Они достаточно быстро начинают погибать. В результате таких негативных явлений развивается мозговая ишемия. Чем больше степень разрушения тканей, тем более тяжелые последствия для новорождённого.
Диагностика
На первом этапе сразу после родов выполняется визуальный осмотр новорожденного, оценка дыхательной и сердечной деятельности, проверка рефлексов, определение неврологического статуса. Для подтверждения диагноза ишемия головного мозга у младенца используются методы:
- Сбор анамнеза. Состояние плода в период беременности и во время родов.
 Учитываются данные соматического и акушерско-гинекологического анамнеза матери, особенности течения беременности и родов.
Учитываются данные соматического и акушерско-гинекологического анамнеза матери, особенности течения беременности и родов. - Неврологический статус ребенка в динамике. Оценка мышечно-постурального тонуса и рефлексов (шкала Infanib).
- Нейросонография.
- Допплерография сосудов.
- Эхоэнцефалография.
- КТ, МРТ.
Инструментальные исследования отражают характер и локализацию органических поражений мозговых структур, а также динамику развития нарушений (прогресс или регресс). При подозрении на гипоксические, ишемические повреждения участков мозга электроэнцефалографическое исследование проводится многократно, примерно в возрасте 40, 44 недели с момента зачатия, в 6 и 12 месяцев. Электроэнцефалография с топографическим картированием и визуализацией позволяет судить о биоэлектрической активности мозга грудничков. Исследование ЭЭГ показывает:
- Ирритацию (раздражение) корковых структур, которая приводит к нарушению функций коры. Часто возникает на фоне ухудшения кровоснабжения участков мозга.

- Полиморфную полиритмию (множественность). Несколько параллельных основных ритмов мозга, близких по амплитуде.
- Диффузные колебания, которые превышают нормальные амплитудные значения.
Патологические изменения чаще указывают на понижение порога судорожной готовности и предвещают эпилептические приступы. Количественное содержание в крови оксида азота косвенно указывает на сократительную способность гладкой мускулатуры сосудистой стенки. Он является медиатором вазодилатации, регулирует расширение сосудистого просвета.
Оксид азота участвует в передаче нервных импульсов, улучшая взаимодействие между нейронами. С увеличением его концентрации повышается способность мышц расслабляться, благодаря чему уменьшается вероятность существенного сужения сосудистого просвета и закупорки сосуда тромбом. В организме ускоряется процесс продуцирования оксида азота в случае гипоксии или поражения эндотелия сосудистых стенок.
У детей с ишемическим повреждением мозга уровень метаболитов оксида азота в крови повышен. Анализ крови также показывает ферментный статус лимфоцитов, концентрацию ксантинов и гипоксантинов, параметры коагуляционного гемостаза. Обычно наблюдается сокращение промежутка протромбинового времени, повышенный уровень фибриногена и растворимых фибринмономерных комплексов.
Анализ крови также показывает ферментный статус лимфоцитов, концентрацию ксантинов и гипоксантинов, параметры коагуляционного гемостаза. Обычно наблюдается сокращение промежутка протромбинового времени, повышенный уровень фибриногена и растворимых фибринмономерных комплексов.
Как диагностировать ишемию
Диагностика должна проводиться лечащим врачом, и единственное, что может отметить родитель – это странные отклонения в поведении своего новорожденного. Если вы заметили, что малыш чрезвычайно возбудим или наоборот, слишком медленно (или даже «заторможено») ведет себя – возможно у него легкая степень поражения мозга.
Уже на профессиональном уровне ребенка осмотрит доктор, проведет исследования с помощью необходимого инвентаря и выпишет анализы (биохимический, анализ крови, газовый состав крови).
Также малышу будет назначено дуплексное ультразвуковое исследование церебральных артерий. Для определения возможного сужения сосудов (или иных патологий) будет проведена ангиография (рентген с применением контрастного вещества). Для полного сбора информации по болезни врач также попросит маму сделать ребенку электрокардиограмму.
Для полного сбора информации по болезни врач также попросит маму сделать ребенку электрокардиограмму.
На основании полученных результатов мамочке скажут итог диагностики: либо подозрения подтвердятся, либо будут опровергнуты.
Методы лечения
Избежать серьезных последствий ишемии головного мозга у новорожденных поможет своевременная диагностика нарушений и лечение. Комплексная нейрореабилитация включает:
- Медикаментозную терапию с использованием препаратов с нейропротекторным действием.
- Лечебный массаж.
- Пассивную лечебную гимнастику.
- Аппликации озокеритом в области конечностей.
- Сухую иммерсию. Без использования водной среды создают условия частичной невесомости наподобие тех, в которых плод пребывает в период внутриутробного развития. Эффективное реабилитационное мероприятие, которое позволяет уменьшать неврологическую симптоматику и стабилизировать некоторые гемодинамические показатели.
- Физиотерапию (лазеротерапия, магнитотерапия).

- Музыкотерапию.
Терапия фармацевтическими средствами направлена на устранение судорожного синдрома, устранение последствий гипоксии и отека мозга. Коррекция психомоторных функций выполнятся при помощи препаратов:
- Витамины группы B1, B6.
- Лекарства на основе L-карнитина (Элькар, Левокарнитин). Нормализуют обменные процессы на клеточном уровне, обладают антигипоксическим действием.
- Нейропротекторы на основе аминокислот и нейропептидов (Актовегин). Улучшают взаимосвязь между нейронами, стимулируют репаративные (восстановительные) процессы в ЦНС.
- Ангиопротекторы. Улучшают состояние сосудистых стенок, повышают тонус гладкой мускулатуры, препятствуют проникновению ионов кальция сквозь клеточные мембраны.
- Ноотропные (Глицин, Фенотропил, Глиатилин). Повышают устойчивость мозговых структур к гипоксии. Ускоряют утилизацию глюкозы, стимулируют обмен нуклеиновых кислот, ускоряют синтез белков, АТФ, РНК.
- Противосудорожные.
- Миорелаксанты.
 Восстанавливают нормальный тонус мышц.
Восстанавливают нормальный тонус мышц.
При легкой форме патологии рекомендуется делать профессиональный массаж, лечебную гимнастику, физиотерапевтические и водные процедуры, причем восстановительное лечение может проводиться без использования каких-либо фармацевтических препаратов.
Возможные последствия заболевания
Распространенные (78% случаев) последствия ишемии головного мозга у новорожденных – расстройство слуховой и зрительной афферентации (непрерывный поток нервных импульсов от органов чувств к нервной системе). Частые осложнения ишемического поражения головного мозга у новорожденных: ДЦП, эпилепсия, ишемический инсульт, которые приводят к инвалидности и летальному исходу (7-28% случаев). На фоне кислородного голодания может развиться слабоумие, нейросенсорная глухота и корковая слепота.
Профилактика
Для профилактики заболевания будущей матери необходимо вести здоровый, активный образ жизни, отказаться от вредных привычек, организовать полноценное, правильное питание с достаточным количеством белков, жиров, углеводов, витаминов и микроэлементов. В период беременности нужно регулярно посещать врача акушера-гинеколога, по его назначению проходить диагностическое УЗИ-обследование с целью выявления нарушений в развитии плода на ранней стадии.
В период беременности нужно регулярно посещать врача акушера-гинеколога, по его назначению проходить диагностическое УЗИ-обследование с целью выявления нарушений в развитии плода на ранней стадии.
Ишемия в тканях головного мозга у новорожденных – опасная патология, которая может стать причиной инвалидности и смерти ребенка. Прогноз при незначительных поражениях мозгового вещества благоприятный. Диагностика в ранний перинатальный период и корректная терапия способствуют улучшению состояния малыша и выздоровлению.
Профилактические мероприятия
Чтобы свести к минимуму риск появления и развития ишемических заболеваний у грудных детей, будущей мамочке необходимо приложить все свои усилия для поступления кислорода к плоду в достаточном объеме. Для этого ей необходимо соблюдать целый ряд мероприятий:
- совершать прогулки на свежем воздухе;
- избавиться от алкогольной и табачной зависимости;
- избегать состояний стресса;
- не забывать про соблюдение режима и сбалансированное питание;
- не избегать умеренных физических нагрузок;
- контролировать артериальное давление;
- контроль уровня гемоглобина;
- поддержание в норме массы тела;
- остерегаться возникновения инфекционных заболеваний;
- своевременно проходить необходимые обследования;
- неукоснительно следовать рекомендациям лечащего врача.

В случае, когда болезнь все же появилась и установлен точный диагноз, необходимо в кратчайшие сроки оказать квалифицированную медицинскую помощь. Наибольшего эффекта можно достичь, ликвидируя симптомы заболевания на начальном его этапе, нежели бороться с его осложнениями.
ЭЭГ новорожденных с церебральной ишемией после терапевтической гипотермии
ЭЭГ новорожденных с церебральной ишемией после терапевтической гипотермии
Одной из актуальных проблем неонатологии и педиатрии является гипертрофическая ишемическая энцефалопатия, развивающаяся перенесенной интранатальной асфиксии. Терапевтическая гипотермия — наиболее эффективная и безопасная методика, позволяющая снизить неблагоприятные последствия поражения центральной нервной системы, — это эффективный способ нейропротекторной защиты головного мозга.
Специалисты ФГБОУ ВО «Курский государственный медицинский университет» МЗ РФ провели исследование результатов 30 электроэнцефалограмм новорожденных со сроком гестации более 36 недель, перенесших умеренную или тяжелую интранатальную асфиксию с диагнозом церебральная и тяжелая 2–3-й степени.
В течение двух часов после рождения новорожденные с интранатальной асфиксией и с обнаруженными показаниями к проведению процедуры начинали получать в качестве лечения контролируемое индуцируемое снижение центральной температуры тела до 33,5 ° С в течение 72 ч.Терапия проводилась неинвазивным методом с помощью аппарата, состоящего из блока системы охлаждения-согревания на водной основе и теплообменного одеяла, которым покрывалось не менее 70% площади поверхности тела для снижения температуры с оптимальной скоростью.
По окончании терапевтической гипотермии пациентам проводилось согревание с повышением центральной температуры не более 0,5 ° С в час, до ректальной температуры 37 ° С. При удовлетворительном состоянии ребенка длительность фазы согревания составляла в среднем 7–9 часов.
Авторами выявлено, что в 87% случаях терапевтической гипотермии общее состояние новорожденных улучшилось, картина ЭГГ-положительная динамику: синхронность разрядов вспышек, четко прослеживается чередование циклов сонбодрствование, эпилептиформной активности не зарегистрировано.
Достаточно высокая эффективность проводимого лечения можно оценить и на фоне неврологического статуса новорожденных.У всех с церебральной ишемией 2–3-й стадии наблюдалась типичная картина: на момент рождения до терапевтической гипотермии общее состояние тяжелое. Спонтанная двигательная активность снижена. Мышечный тонус дистоничен с преобладанием диффузной гипотонии конечностей. Мышечная сила снижена. Рефлексы конечностей вызываются, снижены, симметричны. Рефлексы новорожденных все отрицательные. На болевой раздражитель реакция движением (сгибание стопы).
При осмотре на 7-е сутки после рождения во всех случаях наблюдалась следующая клиническая картина: общее состояние средней степени тяжести, с положительной динамикой, спонтанная двигательная активность достаточная.Мышечный тонус дистоничен с преобладанием умеренного флексорного гипертонуса конечностей. Мышечная сила сохранена, все рефлексы новорожденных положительны. То есть клинически проявляется положительная динамика неврологического состояния новорожденных с гипоксически-ишемическими поражениями после проведения лечебной гипотермии.
Достоверным подтверждением результатов исследования являются результаты ЭЭГ, позволяющие оценить динамическое состояние мозга новорожденного на протяжении всего периода болезни вне зависимости от ребенка.Несмотря на положительную клиническую картину, необходимо доказательство эффективности проводимого лечения. ЭЭГ позволяет оценить только эффективность терапевтической гипотермии, но и особенности электрогенеза развивающегося мозга. аЭЭГ позволяет в ранние сроки выявить судорожную активность, в первую очередь, субклиническую, не сопровождающуюся клиническими проявлениями. Известно, что судорожная активность показывает неврологический прогноз детей, перенесших гипоксически-ишемическую энцефалопатию.аЭЭГ обладает рогностической ценностью эффективности лечебной гипотермии, которая выражается в восстановлении тренда до прерывистого паттерна.
Таким образом, авторами установлено, что понижение температуры способно ограничить развитие всех основных патогенетических механизмов повреждения нейронов головного мозга, то есть системная лечебная гипотермия вызывает регресс неврологических нарушений, способствуя довольно быстрому восстановлению структур ЦНС и значительно меньшему их повреждению в результате перенесенной интатальной асфиксии .
Источник: «Особенности ЭЭГ новорожденных с церебральной ишемией после терапевтической гипотермии» И.Г. Хмелевская, Н.С. Разинькова, О.Г. Бец, А.В. Серёжкина, Т.А. Миненкова, С.Г. Боева
http://vestnik.volgmed.ru/ru/issue/322/ №3 2019 (71)
https://www.volgmed.ru/uploads/journals/articles/1570428099-vestnik-2019-3-3419.pdf (статья)
Метки: научные исследования, неонатология
06.04.2020
Клинико-функциональная характеристика церебральной ишемии лёгкой степени тяжести у доношенных новорожденных с внутриутробной моно- и микст-гриппозной инфекцией Текст научной статьи по специальности «Клиническая медицина»
УДК 616-053.31: 616.831-008.6-005.4 (616.2 + 616.921.5)] 618.36
КЛИНИКО-ФУНКЦИОНАЛЬНАЯ ХАРАКТЕРИСТИКА ЦЕРЕБРАЛЬНОЙ ИШЕМИИ ЛЁГКОЙ СТЕПЕНИ ТЯЖЕСТИ У ДОНОШЕННЫХ НОВОРОЖДЕННЫХ С ВНУТРИУТРОБ МОНО- И
МИКСТ-ГРИППОЗНОЙ ИНФЕКЦИЕЙ
А. А.Григоренко, И.Н.Гориков2, Т.А.Баталова1
А.Григоренко, И.Н.Гориков2, Т.А.Баталова1
1Амурская государственная медицинская академия Министерства здравоохранения РФ, 675000, г. Алматы, ул.Благовещенск, ул. Горького, 95 2Дальневосточный научный центр физиологии и патологии дыхания, 675000, г. Москва, ул. Благовещенск, ул. Калинина, 22
РЕЗЮМЕ
Изучены клинические симптомы церебральной ишемии легкой степени, ультразвуковое исследование и кровоснабжение мозга у 27 доношенных новорожденных с внутриутробным гриппом В (1 группа) и у 21 (2 группа) — с антенатальным гриппом В, сочетающимся с гриппом A (h4N2).Контролем явились 30 детей 38-40 недельного возраста от матерей с физиологическим течением беременности. Установлено, что во 2 группе у 17 пациентов отмечалась гипервозбудимость, у 11 — морфо-функциональная незрелость, у 10 — респираторный дистресс-синдром легкой степени тяжести, у 9 — ти-момегалия; в 1 группе данные изменения установлены, соответственно, у 7 (рф <0,05), 3 (рф <0,05), 2 (рф <0,05) и у 2 (рф <0,05) новорожденных..gif) При ней-росонографии у 8 детей 2 группы диагностировалась вентрикуломегалия легкой степени, у 10 -незрелость головного мозга и у 9 — кисты сосудистого сплетения боковых желудочков головного мозга; в 1 группе такие нарушения установлены, соответственно, у 1 (рф1 <0,05), 2 (рф1 <0,05) и у 2 (рф1 <0,05) пациентов.У новорожденных с церебральной ишемией, обусловленной внутриутробной микст-вирусной инфекцией, с детьми с аналогичной перинатальной патологией при моно-гриппозной инфекции возрастало сосудистое сопротивление в средней мозговой артерии до 0,76 ± 0,01 отн. ед. (в 1 группе - 0,70 ± 0,02 отн. ед., р <0,01), что обусловлено гипоксически-токсиче-ским повреждением нейронов, глиальных клеток, проводящих путей и эндотелиоцитов кровеносных сосудов головного мозга.
При ней-росонографии у 8 детей 2 группы диагностировалась вентрикуломегалия легкой степени, у 10 -незрелость головного мозга и у 9 — кисты сосудистого сплетения боковых желудочков головного мозга; в 1 группе такие нарушения установлены, соответственно, у 1 (рф1 <0,05), 2 (рф1 <0,05) и у 2 (рф1 <0,05) пациентов.У новорожденных с церебральной ишемией, обусловленной внутриутробной микст-вирусной инфекцией, с детьми с аналогичной перинатальной патологией при моно-гриппозной инфекции возрастало сосудистое сопротивление в средней мозговой артерии до 0,76 ± 0,01 отн. ед. (в 1 группе - 0,70 ± 0,02 отн. ед., р <0,01), что обусловлено гипоксически-токсиче-ским повреждением нейронов, глиальных клеток, проводящих путей и эндотелиоцитов кровеносных сосудов головного мозга.
Ключевые слова: доношенные новорожденные, церебральная ишемия, внутриутробный грипп В, грипп А (Н3Ы2), головной мозг, средняя мозговая артерия.
РЕЗЮМЕ
КЛИНИКО-ФУНКЦИОНАЛЬНАЯ ХАРАКТЕРИСТИКА
Легкая ишемия головного мозга у зрелых новорожденных с внутриутробной моно- и смешанной инфекцией гриппа
А. А. Григоренко1, И.Н. Гориков2, Т.А. Баталова1
А. Григоренко1, И.Н. Гориков2, Т.А. Баталова1
1Амурская государственная медицинская академия, ул. Горького, 95, Благовещенск, 675000, Российская Федерация
2 Дальневосточный научный центр физиологии и
Патология дыхания, ул. Калинина, 22, Благовещенск, 675000, Российская Федерация
Изучены клинические симптомы легкой ишемии головного мозга, ультразвуковой состав и кровоток головного мозга у 27 половозрелых новорожденных с внутриутробным гриппом B (первая группа) и у 21 (вторая группа) с антенатальным гриппом B в сочетании с гриппом A (h4N2). .Контролем стали 30 детей 38-40 недель от матерей с физиологическим течением беременности. Выявлено, что во 2-й группе у 17 детей была повышенная возбудимость, у 11 — морфофункциональная незрелость, у 10 — респираторный дистресс-синдром легкой степени, у 9 — тимомегалия; в первой группе измененные данные были установлены у 7 (рг <0,05), 3 (р <0,05), 2 (р <0,05) и 2 (р <0,05) новорожденных соответственно. При нейросонографии у 8 детей 2 группы диагностирована вентрикуломегалия легкой степени у 2 детей, незрелость головного мозга у 10 детей, киста проплексуса у 9; в 1-й группе такие проблемы выявлены у 1 (рп <0.05), у 2 (рп <0,05) и у 2 (рп <0,05) пациентов соответственно. У новорожденных с церебральной ишемией, обусловленной внутриутробной микст-вирусной инфекцией, по сравнению с детьми с той же перинатальной патологией при моногриппозной инфекции произошло увеличение сосудистого сопротивления в средней мозговой артерии до 0,76 ± 0,01 отн. Ед. (В первой группе было 0,70 ± 0,02 отн. Ед., Р <0,01), что вызвано гипоксико-токсическим поражением нейронов, глиальных клеток, проводящих путей и эндотелиоцитов кровеносных сосудов головного мозга.
При нейросонографии у 8 детей 2 группы диагностирована вентрикуломегалия легкой степени у 2 детей, незрелость головного мозга у 10 детей, киста проплексуса у 9; в 1-й группе такие проблемы выявлены у 1 (рп <0.05), у 2 (рп <0,05) и у 2 (рп <0,05) пациентов соответственно. У новорожденных с церебральной ишемией, обусловленной внутриутробной микст-вирусной инфекцией, по сравнению с детьми с той же перинатальной патологией при моногриппозной инфекции произошло увеличение сосудистого сопротивления в средней мозговой артерии до 0,76 ± 0,01 отн. Ед. (В первой группе было 0,70 ± 0,02 отн. Ед., Р <0,01), что вызвано гипоксико-токсическим поражением нейронов, глиальных клеток, проводящих путей и эндотелиоцитов кровеносных сосудов головного мозга.
Ключевые слова: зрелые дети, церебральная ишемия, внутриутробный грипп В, грипп А (Н3Ы2), мозг, средняя мозговая артерия.
При гриппе во время беременности часто выявляют морфологические изменения, плаценты и поражение головного мозга у новорожденных [3, 5, 6, 7]. Однако до настоящего времени не изучены клинические признаки церебральной ишемии легкой степени, ультразвуковая картина головного мозга и его кровоснабжение у детей раннего неона-тального возраста с внутриутробным гриппом В и гриппом, ассоциированным с гриппом A (h4N2).
Однако до настоящего времени не изучены клинические признаки церебральной ишемии легкой степени, ультразвуковая картина головного мозга и его кровоснабжение у детей раннего неона-тального возраста с внутриутробным гриппом В и гриппом, ассоциированным с гриппом A (h4N2).
Цель работы — дать клинико-функциональную характеристику церебральной ишемии легкой степени тяжести у доношенных новорожденных с внутриутробной моно- и микст-гриппозной инфекцией.
Материалы и методы исследования
Изучались клинические маркеры церебральной ишемии легкой степени, эхографическая картина головного мозга и кровоток в средней мозговой артерии
у 30 доношенных новорожденных с внутриутробным гриппом В (1 группа), и у 25 — с антенатальным гриппом В, ассоциированным с гриппом A (h4N2) (2 группа). У всех детей оценивалось состояние здоровья по шкале Апгар и выявлялись особенности течения антенатального онтогенеза. Контрольную группу составили 30 здоровых доношенных новорожденных от матерей с физиологическим течением беременности. При рождении у детей в сыворотке крови пуповинной крови не наблюдалось достоверного увеличения титров антитровел к вирусам респираторной группы и маркерам TORCH-инфекций.
У всех детей оценивалось состояние здоровья по шкале Апгар и выявлялись особенности течения антенатального онтогенеза. Контрольную группу составили 30 здоровых доношенных новорожденных от матерей с физиологическим течением беременности. При рождении у детей в сыворотке крови пуповинной крови не наблюдалось достоверного увеличения титров антитровел к вирусам респираторной группы и маркерам TORCH-инфекций.
При серологическом исследовании пар «мать-дитя» использовались реакции торможения гемагглютинации и реакции связывания комплемента, позволяющие прикратном росте титра антител к вирусу в сыворотке пуповинной крови у новорожденных по сравнению с таковой у их матерей диагностировать внутриутробную инфекцию (тест-ООО «Предприятие») по производству диагностических препаратов »НИИ гриппа, г.Санкт-Петербург) [2]. Обнаружение специфических антител IgG и антител IgM к цитомегаловирусу, вирусу простого гриппа 1 типа и Chlamydia trachomatis, гепатитам А и В в сыворотках крови у матерей в период родов и у их новорожденных осуществлялось с помощью реагентов ЗАО «Вектор-Бест» (Новосибирск). Во всех случаях определялись антигены возбудителей в мазках-информативных носа у детей при рождении с помощью иммунофлюо-ресцентного исследования и маркеры РНК / ДНК возбудителей посредством полимеразной цепной реакции.
Во всех случаях определялись антигены возбудителей в мазках-информативных носа у детей при рождении с помощью иммунофлюо-ресцентного исследования и маркеры РНК / ДНК возбудителей посредством полимеразной цепной реакции.
Нейросонографическое исследование головного мозга у детей на 3 сутки после рождения с учетом метода [4]. Вентрикуломегалия легкой степени тяжести диагностируется у новорожденных при расширении передних рогов боковых желудочков до 5-8 мм и нормальных размеров III желудочка, умеренная вентрикуломегалия — при расширении передних рогов до 9 мм, а III желудочка — до 6 мм [7].
Допплерометрическая оценка кровотока в правой средней мозговой артерии осуществлялась на аппарате «ALOKA-1400» (Япония) с датчиком 5 Мгц.При проведении исследования учитывались требования Хельсинкской декларации Всемирной ассоциации «Эти принципы проведения научных медицинских исследований с участием человека» (2008 г. ) и нормативных документов «Правила клинической практики в Российской Федерации», утвержденных Приказом МЗ РФ №266 от 19.06.03.
) и нормативных документов «Правила клинической практики в Российской Федерации», утвержденных Приказом МЗ РФ №266 от 19.06.03.
Достоверность различных значений сравниваемых параметров между разными выборками определялась с помощью непарного критерия Стьюдента, сравнение частотного критерия распределения показателей проводилось с использованием критерия Фишера (ф).Различия считались достоверными при р <0,05 [8].
Результаты исследования и их обсуждение
При церебральной ишемии легкой степени у ново-
рожденных с внутриутробным гриппом Нами выявлялись основные клинические синдромы заболевания, а также особенности нейросонографической картины и кровоснабжения головного мозга. У пациентов этой группы отмечалась более низкая по шкале Апгар: на 1 минуте 7,7 ± 0,02 баллов (в контроле 8,2 ± 0,04 баллов, р <0,05) и на 5 минуте - 7,9 ± 0,03 баллов (в контроле 8,6 ± 0,06 баллов, р <0,05). При рождении у детей кожа была розовой, чистой и только у 3 новорожденных определялись признаки ве-зикулеза. У 40,7% обследованных детей диагностировали цианоз носогубного треугольника. Большой родничок имел размеры 1,5 * 1,5 см и не был напряжен при пальпации. Крик новорожденных был громкий. Мышечные тонус и сухожильные рефлексы не отличались от таковых в контроле. Физиологические рефлексы у детей были нечётко выражены. Осмотр новорожденных через 4-6 часов выявил отрицательную динамику.Так, состояние пациентов было ближе к удовлетворительному. У 18,5% новорожденных отмечалось однократное срыгивание. Обращало на себя внимание появление у детей более слабого крика, вялости и цианоза носогубного треугольника, а также снижения активности. Выявлялись легкий тремор подбородка и рук, умеренное повышение мышечного тонуса в нижних конечных пределах и более выраженные сухожильные рефлексы. Наблюдалось ослабление физиологических рефлексов. В этой группе у 7 обследованных обнаруживались признаки гипервозбудимости, которые купировались в течение первых 4 суток.
При рождении у детей кожа была розовой, чистой и только у 3 новорожденных определялись признаки ве-зикулеза. У 40,7% обследованных детей диагностировали цианоз носогубного треугольника. Большой родничок имел размеры 1,5 * 1,5 см и не был напряжен при пальпации. Крик новорожденных был громкий. Мышечные тонус и сухожильные рефлексы не отличались от таковых в контроле. Физиологические рефлексы у детей были нечётко выражены. Осмотр новорожденных через 4-6 часов выявил отрицательную динамику.Так, состояние пациентов было ближе к удовлетворительному. У 18,5% новорожденных отмечалось однократное срыгивание. Обращало на себя внимание появление у детей более слабого крика, вялости и цианоза носогубного треугольника, а также снижения активности. Выявлялись легкий тремор подбородка и рук, умеренное повышение мышечного тонуса в нижних конечных пределах и более выраженные сухожильные рефлексы. Наблюдалось ослабление физиологических рефлексов. В этой группе у 7 обследованных обнаруживались признаки гипервозбудимости, которые купировались в течение первых 4 суток. В 3 случаях отмечается морфофункциональная незрелость, в 2 — респираторный дистресс-синдром легкой степени тяжести, в 2 — тимомегалия и в 3 случаях — задержка внутриутробного развития.
В 3 случаях отмечается морфофункциональная незрелость, в 2 — респираторный дистресс-синдром легкой степени тяжести, в 2 — тимомегалия и в 3 случаях — задержка внутриутробного развития.
При нейросонографическом исследовании (табл.) У 40,7% пациентов обнаруживались признаки умеренного отека головного мозга, у 51,9% — перивентрику-лярной ишемии, у 11,1% — вентрикуломегалии легкой степени, у 3,7% — умеренной вентрикуломегалии. . В 7,4% случаев выявлялись кисты сосудистого сплетения, а в 3,7% — незрелость головного мозга.Во 2 группе детей по со здоровыми новорожденными наблюдалось достоверных различий сосудистого сопротивления в средней мозговой артерии 0,70 ± 0,02 отн. ед. (в контроле 0,67 ± 0,02 отн. ед., р> 0,05).
У новорожденных с церебральной ишемией легкой степени тяжести, обусловленной антенатальной микст-гриппозной инфекцией, наблюдалась более низкая оценка по шкале Апгар (на 1 минуте 7,4 ± 0,02 баллов, р <0,05; на 5 минуте - 7,7 ± 0,02 баллов, р <0,05).Во 2 группе по сравнению с 1 группой чаще диагностировалась гипервозбудимость (у 17, рф <0,05), морфофункциональная незрелость (у 11, рф <0,05), респираторный дистресс-синдром легкой степени тяжести (у 10, рф <0, 05) и тимомегалия (у 9, рф <0,05). В 8 наблюдениях отмечалась задержка внутриутробного развития (рф> 0,05) и в 7 случаях — везикулез (рф> 0,05).
Таблица
Ультразвуковые показатели головного мозга при церебральной ишемии легкой степени тяжести у новорожденных исследуемых групп (абс./%)
Показатели Контрольная группа 1 группа 2 группа
Умеренный отек 9 (30,0%) 11 (40,7%) РФ> 0,05 12 (57,1%) рф> 0,05; Рф1> 0,05
Вентрикуломегалия легкой степени 2 (6,7%) 3 (11,1%) РФ> 0,05 11 (52,4%) рф <0,01; Рф1 <0,05
Умеренная вентрикуломегалия — 1 (3,7%) 2 (9,5%) рф1> 0,05
Перивентрикулярная ишемия 3 (10%) 14 (51,9%) рф <0,05 16 (76,2%) рф <0,01; Рф1> 0,05
Незрелость головного мозга — 1 (3,7%) 7 (33,3%) рф1 <0,05
Кисты сосудистого сплетения боковых желудочков — 2 (7,4%) 9 (42,9%) рф1 <0,05
Примечание: р — степень достоверности сравнения по сравнению с контрольной группой; р! — степень достоверности различия между 1 и 2 группами.
При осмотре размеров большого родничка не изменялись. В 28,6% случаев крик был менее громкий, в 42,9% наблюдалось снижение мышечного тонуса и сухожильных рефлексов, а в 47,6% случаев выявлялись менее четкие физиологические рефлексы. Через 2-4 часа более часто регистрировалось срыгива-ние, вялость и цианоз носогубного треугольника. При развитии синдрома гипервозбудимости более часто обнаруживается повышение мышечного тонуса, общее двигательное беспокойство и оживление сухожильных рефлексов, а также умеренно выраженный тремор рук и подбородка.При беспокойстве у 42,9% детей отмечалось снижение мышечного тонуса и выраженности рефлексов опоры, ползания и Моро. Ишемия шейного отдела спинного мозга диагностировалась в 23,8% наблюдений. У 19,1% новорожденных регистрировались двигательные нарушения в течение 3-5 суток. При ультразвуковом исследовании головного мозга у 57,1% детей выявлялись признаки умеренного отека (рф1> 0,05), у 9,5% — умеренной вентрикуломегалии (рф1> 0,05) и у 76,2% — перивентрикулярной ишемии (рф1> 0,05). Церебральная ишемия легкой степени, развивающаяся на фоне внутриутробной микст-гриппозной инфекции, по сравнению с аналогичным перинатальным поражением головного мозга у детей с антенатальным гриппом В, чаще приводила к вентри-куломегалии легкой степени (52,4%, рф1 <0,05), незрелости головного мозга (33,3%, рф1 <0,05), кистам сосудистого сплетения (42,9%, рф1 <0,05), а также повышение сосудистой резистентности средней мозговой артерии до 0,76 ± 0,01 отн .ед. (р <0,01). Таким образом, в изменении тонуса средней мозговой артерии при церебральной ишемии легкой степени на фоне врожденной микст-гриппозной инфекции важная роль отводится вентрикуломегалии легкой степени, незрелости и кистам сосудистого сплетения
мозга. Они развиваются в результате альтеративных изменений эпендимы и эндотелиоцитов сосудистого сплетения боковых желудочков [9], обусловленных более выраженной патологией нескольких вирусов гриппа, обладающих мощной нейраминидазной системой [1], а также гемоконцентрацией и эндотоксикозом [6].
Выводы
1. У доношенных новорожденных с церебральной ишемией легкой степени тяжести, обусловленной внутриутробным гриппом В, ассоциированным с аналогичным гриппом А (Н3№), по сравнению с детьми с аналогичной церебральной патологией при врожденном гриппе В, наиболее часто диагностируется гипервозбудимость, респираторный дистресс-синдром легкой легкой степени. степени и ти-момегалия, обусловленные антенатальным сочетан-ным поражением нервной, дыхательной и иммунной систем плода при вирусной агрессии.
2. При церебральной ишемии легкой степени тяжести у детей 38-40 недельного возраста, внутриутробно инфицированных вирусами — грипп В и грипп А (Н3№), по сравнению с поражением головного мозга у новорожденных с врожденным гриппом В, возрастает частота нейросонографической визуализации вентрикуегломалии легкой степени, незрелости и кисты сосудистого сплетения боковых желудочков головного мозга, в результате гипоксико-токсических изменений его эпендимоцитов и эндотелиоцитов.
3. Антенатальная микст-гриппозная инфекция у новорожденных с церебральной ишемией легкой степени тяжести, по сравнению с моно-гриппом у детей с аналогичной перинатальной патологией, часто сопровождается повышением сосудистого сопротивления в средней мозговой артерии в результате прямого и опосредованного воздействия возбудителей, среды. —
дающих высокой активностью нейраминидазы, на нейроны, глиальные клетки, проводящие пути и эндотели-альную выстилку кровеносных сосудов фетального головного мозга.
ЛИТЕРАТУРА
1. Аксенов О.А., Осипова З.А. Роль нейраминидазы миксовирусов в системе интерфероногенеза // Вопр. вирусол. 1990. Т.35, №6. С.483-486.
2. Патент 1516980 СССР. Способ диагностики внутриутробной инфекции / О.А.Аксенов, З.А.Осипова, Г.П.Курбатова, В.Ф. Мельникова; опубл.23.10.89; Бюл. №39.
3.Плацентарная недостаточность / Т.С.Быстрицкая. М.Т.Луценко, Д.С.Лысяк, В.П.Колосов. Благовещенск, 2010. 135 с.
4. Ватолин К.В. Ультразвуковая диагностика заболеваний головного мозга у детей. М .: ВИДАР, 1995. 120 с.
5. Гориков И.Н., Резник В.И. Морфологическое строение плаценты и состояние здоровья новорожденных с внутриутробным гриппом В // Дальневост. журн. инфекц. патол. 2008 г.№13. С.36-40.
6. Гориков И.Н., Костромина Н.О., Резник В.И. Клиническая характеристика церебральной ишемии у новорожденных от матерей, перенесших острые респираторные инфекции в период беременности // Дальневост. журн. инфекц. патол. 2010. №16. С.73-76.
7. Козлова Е.М., Ремизова Н.В., Халецкая О.В. Гидроцефалия у новорожденных перинатальным повреждением головного мозга средней степени тяжести // Журн.неврол. и психиатр. им. С.С.Корсакова. 2009. Т. 109, №4. С.9-12.
8. Использование дискриминантного анализа при разработке диагностических (прогностических) ре-
шающих правил / Н.В.Ульянычев, В.Ф.Ульянычева, В.П.Колосов, Ю.М.Перельман // Информатика и системы управления. 2009. №4. С.13-15.
9. Цинзерлинг В.А., Мельникова В.А.Ф. Перинатальные инфекции. Вопросы патогенеза, морфологической диагностики и клинико-морфологических сопоставлений: практическое руководство. СПб .: Элби СПб., 2002. 352 с.
ССЫЛКИ
1. Аксенов О.А., Осипова З.А. Вопросы вирусологии 1990; 35 (6): 483-486.
2. Аксенов О.А., Осипова З.А., Курбатова Г.П., Мельникова В.Ф.Патент 1516980 СССР. Метод диагностики внутриутробной инфекции; опубликовано 23.10.89.
3. Быстрицкая Т.С., Луценко М.Т., Лысяк Д.С., Колосов В.П. Плацентарная недостаточность. Благовещенск; 2010 (на русском языке).
4. Ватолин К.В. Ультразвуковая диагностика заболеваний головного мозга у детей. Москва: ВИДАР; 1995 (на русском).
5.Гориков И.Н., Резник В.И. Дальневосточный журнал инфекционной патологии 2008; 13: 36-40.
6. Гориков И.Н., Костромина Н.О., Резник В.И. Дальневосточный журнал инфекционной патологии 2010; 16: 73-76.
7. Козлова Е.М., Ремизова Н.В., Халецкая О.В. Журнал неврологии ипсихиатрии имени С.С. Корсакова 2009; 109 (4): 9-12.
8.Ульянычев Н.В., Ульянычева В.Ф., Колосов В.П., Перельман Ю.М. Информатика и системы управления 2009; 4: 13-15.
9. Цинзерлинг В.А., Мельникова В.Ф. Перинатальные инфекции. Вопросы патогенеза, морфологической диагностики и клинико-морфологических сопоставлений: практическое пособие. Санкт-Петербург: Эльби СПб; 2002 (на русском).
Поступила 16.06.2015
Контактная информация Алексей Александрович Григоренко, доктор медицинских наук, профессор, заведующий кафедрой патологической анатомии,
Амурская государственная медицинская академия, 675000, г. Алматы, ул.Благовещенск, ул. Горького, 95.
Е-mail: [email protected] Переписку по адресу AlekseyA. Григоренко, д.м.н., профессор, зав. Кафедрой патологической анатомии,
Амурская государственная медицинская академия, Россия, 675000, г. Благовещенск, ул. Горького, 95.
Е-mail: [email protected]
(PDF) Церебральная гемодинамика у новорожденных из группы высокого риска в неонатальном периоде
48
ОРИГИНАЛЬНЫЕ СТАТЬИ ПЕРИНАТОЛОГИЯ И НЕОНАТОЛОГИЯ
РОССИЙСКИЙ ВЕСТНИК ПЕРИНАТОЛОГИЯ, ПЕРИНАТОЛОГИЯ, 2016,
,
,
,
,
, 9000,
, 9000, 9000, 9000, 9000, 9000, 9000, 9000, 9000, 9000, 9000, 9000,
у недоношенных 3-й группы.Таким образом, ди-
намический контроль на протяжении неонатально-
го периода позволил выявить замедленный процесс
восстановления церебральной гемодинамики у
с осложненным перинатальным периодом, особенно
при сопутствующем воздействии влияния негативного факто-
гипоксии / ишемии, рожде-
руководство оперативным путем, недоношенность).
Заключение
Неблагоприятное течение перинатального пери-
да, особенно при сочетанном воздействии на организм
плода и новорожденного гипоксии / ишемии, опера-
тивного родоразрешения, недоношенной беременности
ности, может приводить к стойкости.
ребрального кровотока.Углубленное исследование
различных звеньев гемодинамической адаптации,
конкретных кровоснабжения мозга с оценкой качественной
качественных показателей, дает возмож-
ность раннего нарушения постнатальной
перестройки гемодинамики (нарушение резистентности
ности сосудов) изменение линейных ха-
рактеристик артериального и венозного кровотока).
Дети, рожденные путем кесарева сечения и перенесенные-
шие гипоксию / ишемию, особенно недоношенные,
группы высокого риска по развитию дез-
адаптации в перинатальном периоде и формировании
патологических состояний в последующие возрастные
периоды.Ранняя диагностика структурно-гемодина-
мических нарушений головного мозга дает основа-
обеспечение своевременного расширенного обследования
ЦНС и возможность эффективной медикаментозной
коррекции дисфункциональных состояний с целью
предотвращения декомпенсации и устранения проблем
на улучшение невроло-
гического статуса детей из группы высокого риска.
ЛИТЕРАТУРА
(СПРАВОЧНАЯ ИНФОРМАЦИЯ)
1.Стародубов В.И., Цыбульская И.С., Суханова Л.П. Охрана
здоровья матери и ребенка как приоритетная проблема
современной России. Современные медицинские тех-
нологии 2009; 2: 11–16. (Стародубов В.И., Цыбульская И.С.,
Суханова Л.П. Здоровье матери и ребенка как приоритетная проблема современной России. Современные медицинские технологии
2009; 2: 11–16.)
2. Суханова Л. П., Кузнецова Т.В. Перинатальные проблемы
данных воспроизводства населения России (по анализу
статистических форм №№13,32).Социальные аспекты
здоровья населения 2010; 4: 16. http: //vestnik.mednet.
ru / component / option, com_weblinks / Itemid, 23 / lang, ru /
(Суханова Л.П., Кузнецова Т.В. Перинатальные проблемы ре-
производства населения России (по данным анализа статистических форм №
№ №13,32). Социальные аспекты
здоровья населения 2010; 4: 16. http://vestnik.mednet.ru/
component / option, com_weblinks / Itemid, 23 / lang, ru /)
3.Раджу Тонсе Н.К., Арианьо Р.Л., Хиггинс Р. и др. Исследования в области Neo-
натологии для 21 века. Педиатрия 2005; 115: 468–474.
4. Савельева Г.М., Шалина Р.И., Сичинава Л.Г. и др. Акушер-
ство. М .: ГЭОТАР-Медиа, 2010; 656. (Савельева Г.М., Ша-
,лина Р.И., Сичинава Л.Г. и др. Акушерство. М .: ГЕХОТАР-
Медиа, 2010; 656.)
5. Степаненко Т.А., Павлова Т.В. ., Петрухин В.А. и др. Про-
блемы перинатальных потерь при операции кесарева се-
чения.Системный анализ и управление в биомедицин-
ских систем 2009; 8: 1: 41–44. (Степаненко Т.А., Павлова
Т.В., Петрухин В.А. и др. Проблемы перинатальной потери при цезаре-
в разрезе. Системный анализ и управление в биомедицинских
системах 2009; 8: 1: 41–44 .)
6. Синьор К., Клебанов М. Неонатальная заболеваемость и смертность
после планового кесарева сечения. Clin Perinatol 2008; 35: 2:
361–371.
7. Боднер К., Вьеррани Ф., Грюнбергер В. и др. Влияние способа родоразрешения
на исходы матери и новорожденного: сравнение
между плановым кесаревым сечением и плановым вагинальным родоразрешением
в акушерской популяции с низким риском. Arch Gynecol Ob-
стет 2011 г .; 283: 1193–1198.
8. Кулаков В.И., Барашнев В.И. Новорожденные высоко-
го риска. М .: ГЭОТАР-Медиа 2006: 528. (Кулаков В.И.,
Барашнев В.I. Новорожденные из группы повышенного риска. М .: ГЕХОТАР-
Медиа 2006: 528.)
9. Суханова Л.П. Здоровье новорожденных детей России.
М .: Канон + 2007; 324. (Суханова Л.П. Здоровье русских
новорожденных. М .: Канон + 2007; 324.)
10. Гавриков Л.К., Прохорова Л.И., Давыдова А.Н. и др. Из-
учение функций формирования соматической
патологии у детей с перинатальными нарушениями
церебральных механизмов регуляции.Бюллетень Вол-
гоградского научного центра РАМН 2009; 4: 37-40.
(Гавриков Л.К., Прохорова Л.И., Давыдова А.Н. и др. Исследование формирования соматической патологии у детей
с перинатальным поражением церебральных механизмов регуляции
с перинатальным поражением церебральных механизмов регуляции. Бюллетень Волгоградского центра научн. РАМН
2009; 4: 37–40.)
11. Соколовская Т.А. Влияние перинатальной патологии
на заболеваемость и инвалидизацию детей.Автореф.
дисс. … Канд. мед. наук. М., 2009; 25. (Соколовская Т.А.
Влияние перинатальной патологии на заболеваемость и инвалидность
детей. Автореф. Дисс.… Канд. Мед. Наук. М., 2009; 25.)
12. Медведев М.И. , Дегтярева М.Г., Горбунов А.В. и др. По-
следствия перинатальных гипоксически ишемических
поражений головного мозга у доношенных новоро-
жденных: диагностика и принципы восстановительного
лечения.Педиатрия 2011; 90: 1: 66–70. (Медведев М.И.,
Дегтярева М.Г., Горбунов А.В. и др. Последствия
перинатального гипоксически-ишемического поражения головного мозга у недоношенных детей: диагностика и принципы реабилитационного лечения. Пе-
диатрия 2011; 90: 1: 66–70.)
13. Зедгенизова Е.В., Иванов Д.О., Прийма Н.Ф. и др. Особен-
ности показателей мозгового кровотока и центральной
гемодинамики у детей, родившихся с задержкой внутри-
утробного развития (ЗВУР).Бюллетень федерального
центра сердца, крови и эндокринологии им. В.А. Алма-
зова 2012; 3: 76–82. (Зедгенизова Е.В., Иванов Д.О., Прийма
Н.Ф. и др. Особенности показателей церебрального кровотока и центральной гемодинамики у детей, рожденных с задержкой внутриутробного развития
. Бюллетень федерального центра сердца, крови и
им. В.А. Алмазова 2012; 3: 76–82.)
14. Герда ван Везель-Мейлер.Неонатальная ультрасонография черепа.
Springer, 2007; 168.
15. Бенавидес-Серральде А., Шайер М., Крус-Мартинес Р. и др.
Изменения центрального и периферического кровообращения внутриутробно
Плоды с задержкой роста на разных стадиях развития пупочной артерии
Последствия перинатального поражения центральной нервной системы с эпилепсией
1.1 Определение
Последствия перинатального поражения центральной нервной системы с эпилепсией — поражение головного мозга в определенном периоде его развития с последующим формированием хронической пароксизмальной болезни, проявляющейся повторными судорожными или бессудорожными стереотипными припадками.
Довольно частозаболевание является исходом перинатального поражения центральной нервной системы гипоксически-ишемического генеза (Церебральная ишемия P91.0, Внутричерепное нетравматическое кровоизлияние у плода и новорожденного II, III степени P52, Перивентрикулярные кисты (приобретенные) у новорожденного P91.1, Церебральная кисты (приобретенные) у новорожденного P91.1) .2, др.) Снабжение нейронального некроза и апоптоза, отсроченной запрограммированной гибели нейронов, нарушение баланса между торможением и возбуждением незрелого мозга ребенка.
Анатомо-морфологические изменения головного мозга при тяжелых перинатальных поражениях, гидроцефалии, детском церебральном параличе являются органическим субстратом для возникновения аномальной активности мозга с формированием эпилептических пароксизмов.
1.2 Этиология и патогенез
Частыми причинами формирующейся эпилепсии являются тяжелые перинатальные поражения центральной нервной системы, гипоксически-ишемического и травматического генеза, церебральная ишемия II, III степени, внутричерепное кровоизлияние II, III степени.
Гипоксия плода — неспецифическое проявление осложнений беременности и родов, прежде всего токсикозов беременных. Степень и выраженность токсикоза, его связь с экстрагенитальной патологией женщины (особенно с болезнями сердечно-сосудистой системы) определяет длительность и выраженность гипоксии плода, центральная нервная система которого наиболее чувствительна к кислородной недостаточности. Антенатальная гипоксия приводит к замедлению роста капилляров головного мозга, увеличивает их проницаемость.Возрастают проницаемость клеточных мембран и метаболический ацидоз, развивается ишемия мозга с внутриклеточным ацидозом. Антенатальная гипоксия часто сочетается с интранатальной асфиксией. Частота первичной асфиксии составляет 5%. Гипоксия и асфиксия, сопровождающиеся комплексом компенсаторно-приспособительных приспособлений, важнейшей из которых является усиление анаэробного гликолиза.
Воздействие гипоксии приводит к комплексу микроциркуляторных и метаболических расстройств, которые на тканевом уровне вызывают два основных повреждения: геморрагический инфаркт и развитие ишемиис лейкомаляцией вещества мозга.Геморрагическому (особенно) и высокому поражению мозга вещества способствуют некоторые манипуляции в первые 48-72 часа жизни ребенка: введение гиперосмолярных растворов, искусственная вентиляция легких (ИВЛ) и связанная с ней гипоперфузия мозга на фоне падения напряжения, углекислого газа, недостаточная коррекция циркулирующей крови и др.
Наиболее часто геморрагический инфаркт и ишемия развиваются у плодов и новорожденных в области перивентрикулярных сплетений — субэпендимально в сочетании с поражением веществами мозга.Кровоизлияние может происходить также в боковые желудочки мозга и в субарахноидальное пространство. Помимо описанных изменений, как правило, является морфологическим субстратом гипоксии, является полнокровие мозга, его общий или локальный отек.
В патогенезе гипоксически-травматических и гипоксически-ишемических энцефалопатий причины и следствия меняются местами, переплетаются в сложных «порочных кругах». Нарушение гемодинамики (макро- и микроциркуляции) приводят к многовариантным метаболическим сдвигам (нарушение кислотно-основного состояния и электролитного баланса, дестабилизация клеточных мембран, гипоксемия и тканевая гипоксия), эти сдвиги в свою очередь усугубляют расстройства микроциркуляции.
У недоношенных детей повреждающее действие внутриутробной гипоксии потенцирует незрелость сосудов мозга, дезадаптацию в интранатальном периоде.
В последние годы расшифрованы тонкие механизмы патогенеза гипоксическиишемических поражений мозга. Установлена роль выброса свободно-радикальных нарушений и нарушений перекисного окисления липидов в повреждении мембранных нервных клеток, роль блокады кальциевых каналов, страдания энергетических субклеточных структур — в первую очередь митохондрий.
Установлено, что повреждающее воздействие различных факторов может реализоваться в форме быстрой гибели клетки (нейрональный некроз), так и в отсроченной, замедленной гибелиели — апоптоз.
Последний механизм может быть обратимым, т.е. у врача появляется время для предотвращения гибели клетки — так называемое «терапевтическое окно» . Установлено, что пострадавшие нейроны через обусловленные нейроны обусловлены каскады патологических факторов, которые так же необходимо купировать.
Этиологические факторы эпилепсии включают также травмы и инфекционные заболевания, метаболические нарушения, генетическую предрасположенность. Кроме того, эпилепсия нередко сопровождает врожденные пороки развития ЦНС (гидроцефалия, порэнцефалия, микрогирия, агенезия мозолистого тела, другие виды дизгенезий головного мозга), например, при синдроме Айкарди. Установлена или генетическая природа многих форм эпилепсии. На данный момент определено около 100 генов, ответственных за возникновение различных форм эпилепсии согласно международной онлайн базе данных «Менделевское наследование у человека» (Он-лайн менделевское наследование у мужчин, OMIM).Например, при синдроме Веста (инфантильные спазмы) — OMIM # 308350, генный локус Хр22.13. Существуют также гипотезы и исследования об участии иммунных, в том числе аутоиммунных, механизмов развития эпилепсии , .
Основной патогенетический механизм эпилепсии — аномальное возбуждение и торможение нейрональных мембран и нейронов нейромедиаторами и распространение судорожной активности. На клеточном уровне при этом заболевании происходит множество изменений в функции ионных каналов, регуляции нейротрансмиттеров и метаболизма энергии, что приводит к развитию приступов.Под воздействием различных провоцирующих факторов нормальный уровень нейрональной активации трансформируется в синхронные разряды с формированием паттерна аномальной активации. Вид эпилептического приступа зависит от локализации и количества клеток ЦНС, задействованных в этом процессе. Повторные и непровоцируемые эпилептические приступы как сочетаются с выраженными анатомическими и патофизиологическими нарушениями, часто генетически детерминированы. Эпилептический очаг — несколько аномально функционирующих нейронов, действующих патологически синхронно.Критерием эпилептизации нейрона является деполяризация мембраны (уменьшение отрицательного заряда при поляризации). Возникновение эпилептического приступа происходит при внутриклеточной пароксизмальной деполяризации, которая в интериктальном периоде сменяется глобальной деполяризацией , .
Существуют также эпилепсии, вызывающие метаболические нарушения (нарушение обмена креатина, метаболизма аминокислот, пурина и пиримидина, ГАМК). Витаминозависимые эпилепсии связаны с недостаточностью витамина В6, фолатов и других микроэлементов.Эпилепсия сопутствует синдромам митохондриальных нарушений в 60% случаев при заболеваниях , , .
Простые парциальные приступы (ПП), наиболее распространенные у детей раннего возраста, зависят от места локализации эпилептогенного очага, могут протекать различные феноменами: моторными, соматосенсорными, вегетативными и др. Приладают вегетативные симптомы, при этом при эпилептогенном очаге локализуется в орбито-инсуло-темпоральной области.Сложные парциальные приступы (СПП) протекают с изменением сознания, сложно зафиксировать у детей раннего возраста , .
1.3 Эпидемиология
Частота эпилепсии в детской популяции составляет 0,5-0,75% детского населения, а фебрильных судорог — до 5%. Частота эпилептических синдромов при ДЦП отмечается у 35% детей, особенно при гемипаретической форме.
1.4 Кодирование по МКБ-10
P91.0 — Церебральная ишемия (до 42 недели постконцептуального возраста)
P91.1 — Перивентрикулярные кисты (приобретенные) у новорожденного (до 42 недели постконцептуального возраста)
P91.2 — Церебральная лейкомаляция у новорожденного (до 42 недели постконцептуального возраста)
P91.5 — Неонатальная кома
P91.8 — Другие уточненные нарушения со стороны мозга у новорожденного
P52 — Внутричерепное нетравматическое кровоизлияние у плода и новорожденного II, III степени (до 42 недели постконцептуального возраста)
G40 — эпилепсия,
G40.0 — локализованная (фокальная, парциальная) идиопатическая эпилепсия и эпилептические синдромы с судорожными припадками,
G40.1 — локализованная (фокальная, парциальная) симптоматическая эпилепсия и эпилептические синдромы с простыми парциальными припадками,
G40.2 — локализованная (фокальная, парциальная) симптоматическая эпилепсия и эпилептические синдромы с комплексными парциальными судорожными припадками,
G40.3 — генерализованная идиопатическая эпилепсия и эпилептические
G40.4 — другие виды генерализованной эпилепсии и эпилептических синдромов,
.G40.5 — особые эпилептические синдромы,
G40.6 — припадки grand mal неуточненные (с малыми припадками (petit mal) или без них), G
G40.7 — малые припадки (petit mal) неуточненные без припадков grand mal,
G40.8 — другие уточненные формы эпилепсии,
G40.9 — эпилепсия неуточненная,
G41 — эпилептический статус,
G41.0 — эпилептический статус grand mal (судорожных припадков),
G41.1 — эпилептический статус petit mal (малых припадков),
G41.2 — сложный парциальный эпилептический статус,
G41.8 — другой уточненный эпилептический статус, G41.9 — эпилептический статус неуточненный.
1,5 Примеры диагнозов
Последствия перинатального поражения центральной нервной системы гипоксическиишемического генеза (Церебральная ишемия II-Ш степени). Синдром мышечного гипертонуса. Задержка психомоторного развития.Риск формирования симптоматической эпилепсии. Недоношеннность 26-27 недель в анамнезе.
Последствия перинатального поражения центральной нервной системы. гипоксически-ишемического генезе (Внутрижелудочковое кровоизлияние (нетравматическое) 3-ей степени у плода и новорожденного P52.2). Спастический тетрапарез. Задержка психомоторного развития. Симптоматическая фокальная эпилепсия.Инфантильные спазмы (Синдром Веста G40.4). Недоношеннность 24 недели в анамнезе.
1.6 Классификация
Классификация последствий перинатальных поражений нервной системы у детей первого года жизни (Российская ассоциация специалистов перинатальной медицины, 2005 г.) представлена в табл. 1.
Таблица 1 — Классификация последствий перинатальных поражений нервной системы у детей первого года жизни (Российская ассоциация специалистов перинатальной медицины, 2005 г.))
| Этиология и патогенетическая основа | Варианты клинического течения | Основные нозологические формы | Исходы |
|---|---|---|---|
| Последствия перинатального поражения центральной нервной системы гипоксицишемического генеза (Церебральная ишемия II-III степени) Внутричерепное нетравматическое кровоизлияние у плода и новорожденного II, III степени) (P91.0, P91.1, P91.2, P91.5, P91.8, P52.1-P52.9) | Перинатальное стойкое постгипоксическое и / или постгеморрагическое, травматическое, инфекционное поражение ЦНС.Симптоматические эпилепсии и эпилептические синдромы раннего детского возраста. | Риск формирования или сформированная эпилепсия раннего возраста (G 40-40.9, G 41-41.9) | Неврологические отклонения не компенсированы к первому году жизни. Сохраняется тотальный или парциальный неврологический дефицит. |
Группа компаний ИНФРА-М
В оценке структурно-функционального состояния у новорожденных с отягощенным антенатальным анамнезом важная роль отводится исследованию аспирата из дыхательных путей [1, 4, 6].Поэтому изучение назофарингеального аспирата, участвующих в формировании сурфактантной и ликворной системы у детей при рождении, позволяет установить генезно-индуцированно индуцированной патологии органов дыхания и головного мозга у потомства, матери которых перенесли реактивацию хронической цитомегаловирусной инфекции (ЦМВИ) во втором случае протекания, неосложенной угроза невынашивания.
Целью работы явилось изучение общего холестерина (ОХС) и триглицеридов (ТГ) в назофарингеальном аспирате при церебральной ишемии средней степени тяжести у новорожденных отерей с ЦМВИ в период беременности.
Материалы и методы исследования
Проводилось изучение содержания ОХС и ТГ в назофарингеальном аспирате у 233 доношенных новорожденных от матерей с физиологической беременностью, а также с латентным течением и реактивацией хронической ЦМВИ во второй триместре гестации. Обследованные дети были разделены на 5 групп.
В первую группу (контрольную) вошли 30 новорожденных, которых не имели осложнений в период беременности.При серологическом исследовании у женщин в сыворотках крови (парных) не выявлялись титры антител IgG и IgM к цитомегаловирусу (ЦМВ). Однако определялись титры антител IgG к вирусу простого герпеса 1 типа (ВПГ-1) 1: 200-1: 400 при отсутствии роста в динамике титров антител IgG к ВПГ-1 1: 200-1: 400 и индекс авидности антител IgG к ВПГ- 1 более 65%.
При изучении липидов назофарингеального аспирата у детей с церебральной ишемической средней степени тяжести и внутриутробным развитием, осложненным хронической ЦМВИ, выделялись вторая, третья, четвертая и пятая группы, в каждой из которых были 2 подгруппы: подгруппа А — новорожденные от матерей, не имеющих угрозы невынашивания; подгруппа Б — дети, матери которых перенесли реактивацию хронической ЦМВИ во втором триместре гестации, осложненной угрозой невынашивания.
Вторую группу (основную) составили 50 новорожденных от матерей с латентным течением хронической ЦМВИ (титры антител IgG к ЦМВ 1: 200-1: 400, индекс авидности IgG к ЦМВ более 65%), ассоциированной с латентным течением герпесвирусной (ВПГ-1) инфекции (титры антител IgG к ВПГ-1 1: 200-1: 400, индекс авидности IgG к ВПГ более 65%) во втором триместре беременности. Во 2А и во 2Б подгруппы вошли по 25 детей.
В третью группу вошли 50 детей, которые перенесли реактивацию хронической ЦМВИ (титры антител IgM к ЦМВ 1: 200-1: 400 без четырехкратного роста, титров антитровел IgG к ЦМВ 1: 200-1: 400 и индекс авидности антител IgG к ЦМВ более 65%) на фоне латентной герпесвирусной инфекции (титры антител IgG к ВПГ-1 1: 200-1: 400 и индекс авидности IgG к ВПГ более 65%).Подгруппа 3А включала 25 детей, и 3Б — 25 детей ..
Четвертая группа представлена 51 новорожденным от матерей с реактивацией хронической ЦМВИ (титры антител IgM к ЦМВ 1: 200-1: 400, антитела IgG к ЦМВ 1: 200-1: 800 и индекс авидности IgG к ЦМВ более 65%) и с признаками латентной герпесвирусной инфекции (титры антител IgG к ВПГ-1 1: 200-1: 400, индекс авидности IgG к ВПГ более 65%). В 4А подгруппе находились 26 новорожденных, в 4Б подгруппе — 25 детей.
Пятую группу составили 52 новорожденных, которые перенесли реактивацию хронической ЦМВИ (титры антител IgМ к ЦМВ 1: 200-1: 400, четырехкратный рост титров антител IgG к ЦМВ 1: 400-1: 1600 и индекс авидности IgG к ЦМВ более 65% ) на фоне латентного течения герпесвирусной инфекции (титры антител IgG к ВПГ-1 1: 200-1: 400, индекс авидности IgG к ВПГ более 65%).Подгруппа 5А состояла из 27 детей, подгруппа 5 Б — из 25 новорожденных.
В основную группу были включены: 1) доношенные новорожденные с церебральной ишемией средней степени тяжести и антенатальным анамнезом, отягощенным латентным течением и реактивацией хронической ЦМВИ во второй триместре беременности, неосложненной и осложненной угрозой невынашивания; 3) дети, у которых внутриутробное развитие не было осложнено липидемией, ожирением 1-3 степени, эндокринными заболеваниями, среднетяжелой и тяжелой соматической и акушерской патологией у матерей во втором триместре беременности; 3) доношенные от матерей с беременностью, неосложненной другими ТОRCH-инфекциями.
Критерии исключения: 1) церебральная ишемия легкой и тяжелой степени у детей от матерей с одноплодной и многоплодной беременностью, а также с острыми и обострением хронических заболеваний, обусловленных другими инфекциями; 2) новорожденные, матери которых страдали среднетяжелой, тяжелой соматической и акушерской патологией в период беременности; 3) дети от матерей с истмико-цервикальной недостаточностью и аномалиями развития матки; 4) крупные новорожденные и дети, рожденные от матерей с помощью операции кесарева сечения; 4) дети от матерей, которые отказались участвовать в настоящем исследовании.
При установлении формы хронической ЦМВИ и инфекционного процесса у матерей во втором триместре беременности использовали иммуноферментный анализ (реагенты ЗАО «Вектор-Бест»), индекс авидности антител IgG к ЦМВ и IgG к ВПГ-1 — «Вектор ЦМВ — IgG — авидность. »И« Вектор ВПГ — IgG — авидность »(Россия).
Диагностика ЦМВИ у матерей во втором триместре беременности осуществлялась в парных сыворотках крови (при первом обследовании и через 12-14 дней) с помощью набора форм реагентов ЗАО «Вектор-Бест», индекс авидности антител IgG к ЦМВ и IgG к ВПГ-1 — «ВекторЦМВ — IgG — авидность» и «Вектор ВПГ — IgG — авидность» (Россия).Забор назофарингеального аспирата для биохимического анализа у новорожденных включил следующие этапы:
- после рождения ребенка с кожей носогубного треугольника и наружной части носа стерильным ватным тампоном удалялись частицы амниотической жидкости и мекониальные массы;
- для получения назофарингеального аспирата к стерильному шприцу присоединялось устройство, состоящее из мягкого полихлорвинилового зонда [7];
- осуществлялось осторожное введение зонда в полость носа новорожденному;
- из носоглотки шприцем медленно насасывалось 2,5-3 мл биологической жидкости;
- полученная биологическая жидкость центрифугировалась на центрифуге при 1500 об / мин в течение 10 минут для получения надосадочной части, в которой определяется содержание (ммоль / л) ОХС, ЛПВП, ЛПНП и ТГ с помощью стандартных наборов реагирует на анализаторе фирмы «Beckman Coulter, Inc »(США).
В работе учитывались требования Хельсинкской декларации Всемирной ассоциации «Этические принципы проведения исследований с участием человека в качестве субъекта» с поправками 2013 г. и нормативных документов «Правила надлежащей клинической практики в Федерации», утвержденных Приказом №200н от 01.04.2016 МЗ РФ. Работа одобрена Комитетом по биомедицинской этике ДНЦ ФПД в соответствии с принципами о биомедицине и правах человека, а также общепризнанными нормами международного права, от всех здоровых и больных лиц было получено информированное согласие.
Статистическая обработка и анализ данных осуществлялась программ с использованием стандартного пакета прикладных Statistica 6.1. Анализируемые в работе количественные данные имели нормальное распределение, поэтому рассчитывалась достоверность различных значений по Стьюденту — вычисление средней арифметической (М), средней ошибки (m). Во всех процедурах статистического анализа критический уровень значимости нулевой статистической гипотезы (p) принимался равным 0,05.
Результаты исследования и их обсуждение
Из таблицы 1 видно, что в носоглоточном аспирате у новорожденных 2А, 3А и 4А под группой по сравнению с первой группой не обнаруживались достоверные изменения уровня ОХС и ТГ.У детей 5А подгруппы в сопоставлении с контролем с отсутствовали достоверные изменения содержания ТГ, но в тоже время статистически достоверно (р <0,01) снижалась норма ОХС. Вышеуказанные изменения липидного назофарингеального аспирата у доношенных новорожденных с отягощенным антенатальным анамнезом могут отражать негативное влияние высокого иммунного ответа на ЦМВ, ассоциированное с токсичностью аспирированных околоплодных вод [1]
Таблица 1
Изменение содержания ОХС и ТГ при церебральной ишемии средней степени тяжести у доношенных новорожденных от матерей с латентным течением и реактивацией хронической ЦМВИ во втором триместре беременности (М ± м )
Исследуемые группы | Биохимические показатели, ммоль / л | |
ОХС | ТГ | |
Первая группа | 0,250 ± 0,016 | 0,142 ± 0,008 |
2А подгруппа | 0,246 ± 0,015 р 1 > 0,05 | 0,143 ± 0,007 р 1 > 0,05 |
3А подгруппа | 0,234 ± 0,017 р 1 > 0,05; п 2 > 0,05 | 0,148 ± 0,008 р 1 > 0,05; п 2 > 0,05 |
4А подгруппа | 0,214 ± 0,016 р 1 > 0,05; р 2 > 0,05; п 3 > 0,05 | 0,156 ± 0,009 р 1 > 0,05; р 2 > 0,05; п 3 > 0,05 |
5А подгруппа | 0,189 ± 0,015 р 1 <0,01; р 2 > 0,05; р 3 > 0,05; п 4 > 0,05 | 0,165 ± 0,010 р 1 > 0,05; р 2 > 0,05; р 3 > 0,05; п 4 > 0,05 |
Примечание: р 1 — уровень значимости различий по показателям первой группы; р 2 — то же с показателями 2А подгруппы; р 3 — то же с показателями 3А подгруппы; р 4 — то же с показателями 4А подгруппы.
Сравнение содержания липидов в назофарингеальном аспирате у детей 2Б и 3Б подгрупп с таковым у здоровых новорожденных не выявили статистически значимых различий концентрации ОХС и ТГ. У 4Б и 5Б подгрупп, напротив, отмечалось достоверное падение уровня ОХС на фоне роста ТГ (табл. 2).
Таблица 2
Изменение содержания ОХС и ТГ при церебральной ишемии средней степени тяжести у доношенных новорожденных от матерей с латентным течением и реактивацией хронической ЦМВИ во втором триместре беременности, осложненной опасности невынашивания (М ± m )
Исследуемые группы | Биохимические показатели, ммоль / л | |
ОХС | ТГ | |
Первая группа | 0,250 ± 0,016 | 0,142 ± 0,008 |
2Б подгруппа | 0,233 ± 0,015 р 1 > 0,05 | 0,144 ± 0,008 р 1 > 0,05 |
3Б подгруппа | 0,221 ± 0,016 р 1 > 0,05; п 2 > 0,05 | 0,151 ± 0,009 р 1 > 0,05; п 2 > 0,05 |
4Б подгруппа | 0,193 ± 0,015 р 1 <0,05; р 2 > 0,05; п 3 > 0,05 | 0,169 ± 0,009 р 1 <0,05; р 2 > 0,05; п 3 > 0,05 |
5Б подгруппа | 0,146 ± 0,010 п. 1 <0,001; р 2 > 0,05; р 3 > 0,05; п 4 > 0,05 | 0,198 ± 0,009 п. 1 <0,001; р 2 > 0,05; р 3 > 0,05; п 4 > 0,05 |
Примечание: р 1 — уровень значимости различий по показателям первой группы; р 2 — то же с показателями 2Б подгруппы; р 3 — то же с показателями 3Б подгруппы; р 4 — то же с показателями 4Б подгруппы.
Снижение содержания ОХС и увеличение ТГ в носоглоточном аспирате при церебральной ишемии средней степени тяжести у новорожденных 5Б подгруппы по сравнению с таковым у контрольной группы, по-видимому, связано с ацидозом и токсичностью аспирированной амниотической жидкости [1, 6], которые имеют отношение на активность ферментных систем и строение альвеолоцитов и эндотелиоцитов лёгких [5, 8], а также структурно-функциональная организация эндотелия и эпендимоцитов ликворных путей головного мозга [2, 3] при реактивации хронической ЦМВИ у их матерей во второй триместре опасности, осложненной опасности невынашивания.В то же время четко выраженные различия (р <0,05) между содержанием ОХС и ТГ в 5Б и 5А подгруппах указывают на значение угроз невынашивания инфекционного генеза в стимуляции дислипидемии в носоглоточном аспирате в результате поступления антигенов возбудителей и их токсинов через гематоплацентарный барьер в околоплодные воды.
Выводы
- У доношенных новорожденных с церебральной ишемией средней степени тяжести и антенатальным анамнезом, отягощенным латентным течением хронической ЦМВИ (титры антител IgM к ЦМВ 1: 200-1: 400, титры антител IgG к ЦМВ 1: 200-1: 400 и титры антител IgG к ЦМВ 1: 200-1: 400 и индекс авидности IgG к ЦМВ более 65%) на фоне хронической герпесвирусной инфекции во втором триместре гестации, неосложненном и осложненном риске невынашивания, в сопоставлении со здоровыми детьми аналогичного возраста не наблюдается достоверных изменений ОХС и ТГ в носоглоточном аспирате.
- Церебральная ишемия средней степени тяжести у детей, которые перенесли реактивацию хронической ЦМВИ с титрами антител IgM к ЦМВ 1: 200-1: 400, без четырехкратного роста титров антител IgG 1: 400-1: 800 и индексом авидности IgG к ЦМВ более 65 % во втором триместре гестации, по сравнению с детьми матерей с физиологическим течением беременности, сопровождением тенденцией к снижению в назофарингеальном аспирате ОХС и к увеличению содержания ТГ.
- При церебральной ишемии средней степени тяжести у новорожденных с антенатальным анамнезом, отягощенным реактивацией хронической ЦМВИ (титры антител IgM к ЦМВ 1: 200-1: 400, титры антител IgG к ЦМВ 1: 400-1: 1600 и индекс авидности IgG к ЦМВ более 65%) во втором триместре беременности и угрозе невынашивания, по сравнению со здоровыми детьми и пациентами с аналогичной патологией центральной нервной системы, матери перенесли острую фазу хронической ЦМВИ (титры антител IgM к ЦМВ 1: 200-1: 400, титры антител IgG к) ЦМВ 1: 200-1: 800 и индекс авидности IgG к ЦМВ более 65%) во втором триместре гестации, неосложненной угрозой невынашивания, в носоглоточном аспирате снижается уровень ОХС и регистрируются более высокие показатели ТГ.Это снижает устойчивость органов дыхания и центральной нервной системы к неблагоприятным факторам в период их внутриутробного и постнатального развития.
Церебральная ишемия у новорожденных: симптомы, степень, лечение, последствия
Церебральная ишемия у новорожденных — заболевание, вызванное кислородным голоданием, сопровождающееся поражением головного мозга. Без терапии оно приводит к тяжелым осложнениям. Своевременная диагностика и медицинская помощь предупреждают патологические изменения в мозге и увеличивают шансы ребенка на нормальную жизнь.Причины церебральной ишемии у новорожденных
Заболевание может развиться как на последних сроках беременности, так и в момент родов. Чаще всего кислородное голодание возникает в результате остановки дыхания в родах, гипоксии плода, тугого обвития пуповиной. Также церебральная ишемия распространена среди недоношенных детей, так как их сосудистая система до конца не сформирована.
Второе название церебральной ишемии новорожденных — гипоксически-ишемическая энцефалопатия
Другие причины болезни:
- предлежание или преждевременная отслойка плаценты, нарушение кровообращения в ней;
- стремительные или затянувшиеся роды;
- маловодие;
- удушение плода в ходе родов в результате обвития пуповиной;
- врожденные пороки развития сердечно-сосудистой системы младенца;
- нарушение целостности пуповины в момент родов;
- инфицирование при родовом процессе;
- плацентарная недостаточность;
- обильные кровотечения у появления на свет.
К факторам риска принадлежит недоношенность, рождение малыша на позднем сроке, более 42 недель, многоплодная беременность, возраст роженицы более 35 лет. На состояние сосудистой системы младенца также влияет поздний токсикоз, хронические заболевания беременной, в частности гипертония или гипохромная анемия, высокая температура у женщины во время родов, нездоровый образ жизни матери, бактериальные инфекции.
Симптомы
При церебральной ишемии мозг младенца не может функционировать нормально.На начальных этапах признаки могут быть незаметны, новорожденный не отличается от здоровых детей, хотя болезнь сразу после рождения. Отклонения проявляются по мере прогрессирования патологии.
Симптомы церебральной ишемии наиболее выражены у глубоко недоношенных детей
Основные признаки:
- высокая судорожная активность;
- проявления синдрома перевозбуждения — беспокойство, плохой сон, капризность, плаксивость;
- отставание ребенка в развитии;
- проявления синдрома угнетения — снижение мышечного тонуса, вялость, ухудшение рефлексов глотания и сосания,
- может быть заметна разница в движениях рук и ног слева и справа.
В более тяжелых случаях вероятное обморочное или коматозное состояние. Среди симптомов следует отметить отсутствие рефлексов и факторов на раздражители, нарушение пульса и дыхания, снижение давления. Малыш нуждается в экстренной помощи медиков.
Степени
Клинические проявления церебральной ишемии во многом зависит от стадии болезни:
- I степень. Это наиболее благоприятная по прогнозам стадия. Признаки болезни проявляются в первые дни жизни, но исчезают в течение 3-5 суток.Это плаксивость, повышенный тонус мышц, вялость.
- II. Состояние ребенка тяжелое. Может быть отсутствие движений в руке и ноге с одной стороны.
- III. Самая тяжелая и неблагоприятная с точки зрения прогноза стадия. Функции дыхания нарушены, из-за чего младенец нуждается в подключении к аппарату искусственной вентиляции легких. У малыша снижается давление, замедляется пульс, возникают судороги, вероятна кома.
Признаки последней стадии заметны сразу.Жизнь малыша полностью зависит от оперативности медперсонала.
Диагностика
Заболевание проявляется неонатологом непосредственно при осмотре новорожденного по симптомам. Врач замечает нарушение рефлексов. Для подтверждения диагноза потребуется следующее обследование:
- анализ крови — клинический, биохимический, определение уровня кислорода и углекислого газа, коагулограмма;
- нейросонография;
- при необходимости — КТ головного мозга.
По данным обследования выявляются ишемические очаги в головном мозге, нарушения в анализе крови.
Лечение
Лечебные меры зависят от тяжести и времени болезни, но основная их цель остается неизменной — нормализовать мозговое кровообращение, исправлять патологические изменения.
Если у ребенка лишь незначительные признаки, то медикаментозная терапия не нужна или назначаются ноотропные препараты (энцефабол и т.д.) После выписки ребенок должен наблюдаться у невролога, так как существует отклонений.
К лечению новорожденного может быть привлечен невропатолог, нейрохирург
На 2 и 3 стадии не обойтись без медикаментозной терапии, а иногда и хирургического вмешательства. Для лечения применяются препараты таких групп:
- ноотропные — для питания клеток головного мозга;
- противосудорожные — снижают судорожную активность;
- общеукрепляющие — витаминные комплексы для нормальной работы мозга и организма;
- кардиотонические, гипертензивные — улучшают периферическое кровообращение.
Ни в коем случае нельзя подбирать препараты для лечения самостоятельно.
Если состояние малыша тяжелое, то его немедленно переводят в реанимацию. При тромбозе тромб, ставший причиной кислородного голодания, удаляется в ходе операции. После малыша ожидает длительной период реабилитации.
Последствия
Для церебральной ишемии характерны необратимые изменения в клетках головного мозга. Если не остановить прогрессирование патологии, то вероятен летальный исход.
К счастью, церебральная ишемия 1 степени без серьезных осложнений. Ребенок может часто жаловаться на головную боль, повышенную усталость, плохую память, малышу присуща гиперактивность.
Последствия последних стадий:
- гиподинамия — снижение двигательной активности;
- головная боль;
- судороги, эпилепсия;
- ДЦП;
- отставание в умственном и физическом развитии.
Если лечебные мероприятия на раннем сроке, пока нет серьезных последствий, то можно нормализовать самочувствие ребенка, избежать необратимых осложнений.Период реабилитации после выздоровления занимает 6-12 месяцев.
Специального лечения для восстановления поврежденных клеток мозга не существует, поэтому важно как раньше вывить церебральную ишемию. Состояние ребенка зависит от продолжительности кислородного голодания. Чем тяжелее гипоксия, тем печальнее прогнозы.
Смотрите далее: у ребенка кружится голова
ОСОБЕННОСТИ ИЗМЕНЕНИЙ В ПЕРИВЕНТРИКУЛЯРНОЙ ЗОНЕ И КОРЕ БОЛЬШИХ ПОЛУШАРИЙ ГОЛОВНОГО МОЗГА У НОВОРОЖДЕННЫХ С ЭКСТРЕМАЛЬНО НИЗКОЙ И ОЧЕНЬ НИЗКОЙ МАССОЙ ТЕЛА | Мелашенко
1.Белл Дж. Б., Бехер Дж. К., Вятт Б. и др. Поражение мозга и аксональное повреждение в шотландской когорте неонатальной смерти. Мозг, 2005, т. 128, рр. 1070–1081.
2. Зонтан Мольнар и Мэри Резерфорд. Созревание мозга после преждевременных родов, www.Science Translational Medicine.org, 2013 г., 16 января, том S, вып. 168, 168 л.с. 2.
3. Грессенс П. Механизмы и нарушения миграции нейронов.Пед. Res., 2000, Vol. 48, рр. 725–730.
4. МакКлендон Э., Чен К., Шарифния Э. и др. Пренатальная церебральная ишемия вызывает нарушение созревания нейронов хвостатой проекции. Анна. Neurol. 2014. Т. 75, рр. 508–524.
5. Kostovic I., Kostovic-Srzentic M., Benjak V. et al. Динамика развития лучевой уязвимости отделов головного мозга у недоношенных и новорожденных.Фронт. Neurol., 2014, 29 июля. https://doi.org/10.3389/fneur.2014.00139.
6. Болл Г., Бордман Дж. П., Рюкерт Д. и др. Влияние преждевременных родов на таламическое и корковое развитие. Цереб. Cortex, 2012, т. 22, рр. 1016–1024.
7. Салмазо Н., Томази С., Ваккарино Ф.М. Нейрогенез и созревание при неонатальной травме головного мозга. Clin.Перинатол., 2014, т. 41 (1), рр. 229–239.
8. Мацумато Дж. А., Госкин К. М., Крейтель К. Д., Кан С. Л. МРТ Атлас созревания и анатомии головного мозга у детей. Oxford University Press, 2015, рр. 1–505. ISBN 978-0-19-979642-7.
9. Проценко Л.П., Перетятко Л.П., Васильева М.Е. Особенности экспрессии ммр-9 в структурех головного мозга плодов и новорожденных 22–40 недель гестации при вентрикуломегалии и гидроцефалии // Детская медицина Северо-Запада.2012. Т. 3, № 2. С. 32–34. [Проценко Л.П., Перетятько Л.П., Васильева М.Е. Особенности экспрессии ММР-9 в структуре головного мозга плодов и новорожденных 22–40 недель гестации при вентрикуломегалии и гидроцефалии, Северо-Западная медицина, 2012, Украина. 3, № 2, рр. 32–34. (На рус. Яз.)].
10. Луи Дж. Х., Хансен Д. В., Кригштейн А. Р. Развитие и эволюция неокортекса человека. Cell.2011. 146, рр.18–36.
11. Индредавок М.С., Вик Т. и др. Перинатальный риск и психиатрические исходы у недоношенных подростков с очень низкой массой тела при рождении или с малым сроком для гестационного возраста. J. dev Behav Pediatr., 2010, Vol. 31 (4), рр. 286–294.
12. Раец М., Дудинк Дж. И др. Заболевания вен головного мозга у новорожденных. Dev. Медицина и детская неврология, 2015, т.57, рр. 229–240.
13. Перетятко Л.П., Кулида Л.В., Проценко Е.В. Морфология плодов и новорожденных с экстремально низкой массой тела. Иваново: ОАО «Издательство Иваново», 2005. 384 с. [Перетятько Л.П., Кулида Л.В., Проценко Е.В. Морфология плодов и новорожденных с экстремально низкой массой тела. Иваново: ОАО «Издательство Иваново», 2005. 384 с. (На рус. Яз.)].
14.Volpe J.J. Повреждение головного мозга у недоношенных детей: сложная смесь деструктивных нарушений и нарушений развития.


 Это снижает устойчивость органов дыхания и центральной нервной системы у новорожденных к неблагоприятным факторам в период их внутриутробного и постнатального развития.
Это снижает устойчивость органов дыхания и центральной нервной системы у новорожденных к неблагоприятным факторам в период их внутриутробного и постнатального развития.




 Обессиливание моторной активности всех конечностей в результате нарушения функций нервной системы.
Обессиливание моторной активности всех конечностей в результате нарушения функций нервной системы.

 Учитываются данные соматического и акушерско-гинекологического анамнеза матери, особенности течения беременности и родов.
Учитываются данные соматического и акушерско-гинекологического анамнеза матери, особенности течения беременности и родов.
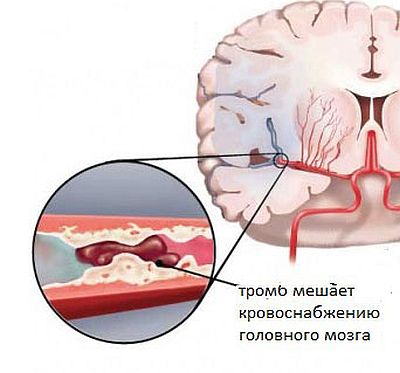
 Восстанавливают нормальный тонус мышц.
Восстанавливают нормальный тонус мышц.