Прививка АКДС+ХИБ | Tibbiyot Dunyosi — медицинский центр, лаборатория, центр вакцинации в Ташкенте, Узбекистан
Расшифруем АКДС: адсорбированная коклюшно-дифтерийно-столбнячная вакцина, а значит, действие прививки защищает сразу от трех страшных инфекционных заболеваний.
Чем опасны коклюш, дифтерия, столбняк для ребенка, и почему лучше сделать прививку и приобрести иммунитет искусственный, нежели переболеть и «заработать» естественную защиту?
- Дифтерия опасна тяжелыми токсическими осложнениями, такими, как инфекционно-токсический шок, полиневрит, нефроз, миокардит, блокирование дыхательных путей.
- Столбняк вызывает серьезные поражениями нервной системы, вплоть до появления генерализованных тетанических судорог.
- Коклюш, особенно в первый год жизни, может вызывать апноэ (остановку дыхания) и привести к летальному исходу. Для болезни характерны приступы спазматического кашля, грозящего состоянием тяжелой гипоксии, развитием судорожного синдрома и гипоксической энцефалопатией.

Побочные реакции могут возникнуть даже при вакцинировании современными качественными вакцинами и носят временный характер. Сравните статистику, от легких побочных реакций до тяжелых осложнений, с учетом того факта, что прививку поставили здоровому ребенку, не имеющему противопоказаний, после необходимых анализов и осмотра у врача:
- Среди легких побочных реакций у 1 из 4 малышей наблюдается повышение температуры тела, дискомфорт, отек и покраснение на месте укола. У 1 из 10 детей — отсутствует аппетит, наблюдаются рвота и понос, вялость и сонливость.
- Побочные реакции средней тяжести, такие, как судороги, встречаются у 1 ребенка на 14 500 детей, у 1 малыша из 15 000 детей — повышение температуры выше 39,5°.
- Серьезная аллергия на компоненты вакцины возможна у 1 ребенка на миллион детей, а тяжелые неврологические нарушения, возникшие непосредственно после прививки, чрезвычайно редки, поэтому невозможно установить их связь с побочным действием вакцины.

Все возможные легкие и среднетяжелые реакции организма на прививку — явление нормы, своего рода сигнал о формировании иммунитета. Тогда как полное отсутствие каких бы то ни было негативных проявлений — результат того, что вам вместе с врачом удалось свести к минимуму все негативные проявления. Главное — грамотно подготовиться к вакцинации: посоветуйтесь с лечащим врачом своего ребенка или с врачом-педиатром нашего Медицинского Центра, внимательно изучите Советы родителям и рекомендации по Подготовке к вакцинации, а также раздел Часто задаваемые вопросы, в котором вы найдете ответы на волнующие вас вопросы.
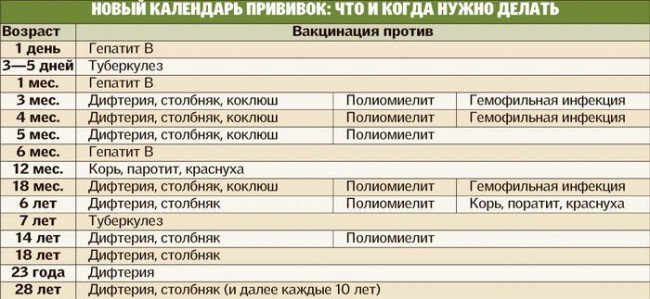
Комплексная вакцина АКДС вводится многократно со строго установленными интервалами (минимум 30 дней для в рамках первичного курса), которые необходимо соблюдать. Схема вакцинации АКДС согласно Национальному календарю прививок:
|
2 месяца |
АКДС-1 — Вакцинация против коклюша, дифтерии и столбняка |
|
3 месяца |
АКДС-2 — Вакцинация против коклюша, дифтерии и столбняка |
|
4 месяца |
АКДС-3 — Вакцинация против коклюша, дифтерии и столбняка |
|
16 месяцев |
АКДС-4 — Вакцинация против коклюша, дифтерии и столбняка |
|
7 лет |
АДС-М-5 — Ревакцинация против дифтерии и столбняка |
|
16 лет |
АДС-М-6 — Ревакцинация против дифтерии и столбняка |
Получить прививки вы можете по следующим адресам:
- г.
 Ташкент, Алмазарский р-н, ул. Тахтапуль, 341а.
Ташкент, Алмазарский р-н, ул. Тахтапуль, 341а.
Телефоны: +998 95 142-75-75, +998 95 143-75-75
- г.Ташкент, Чиланзар-2, ул. Гагарина, дом 11.
Телефоны: +998 71 277-99-90, +998 71 271-10-85
- г.Ташкент, ул. Карасарайская, дом 31
Телефоны: +998 71 248-01-07, +998 71 248-00-13
Вакцинопрофилактика
График работы процедурно-прививочного кабинета (каб.205)
| Пн | 10:00 – 13:00 | 14:00 – 19:30 |
|---|---|---|
| Вт | 08:00 – 13:00 | 14:00 – 19:30 |
| 10.00 – 13.00 | 14. 00 – 19.30 00 – 19.30 |
|
| Чт | 10:00 – 13:00 | 14:00 – 19:30 |
| Пт | 10:00 – 12:30 | 16:00 – 19:30 |
13.00 — 14.00 – уборка, кварцевание, проветривание.
Забор крови (из вены) по предварительной записи: понедельник, среда, четверг, пятница – 8:00 — 9:30
09.30 — 10.00 и 19.30 — 20.00 – текущая уборка помещения (ЕЖЕДНЕВНО) 13.00 — 16.00 – генеральная уборка помещения (ТОЛЬКО ПЯТНИЦА)
Вакцинопрофилактика для детей – наиболее удобный и распространенный способ защиты организма от инфекционных заболеваний. В настоящее время прививки успешно защищают людей от серьезных инфекционных заболеваний, способных вызвать тяжелые осложнения, сделать человека инвалидом или стать причиной смерти.
 При введении в организм ребенка, вакцины обеспечивают выработку специфической защиты (антител и специальных клеток). Когда организм встречается с настоящим возбудителем инфекции, то выработанная защита препятствует развитию болезни или смягчает тяжесть ее течения.
При введении в организм ребенка, вакцины обеспечивают выработку специфической защиты (антител и специальных клеток). Когда организм встречается с настоящим возбудителем инфекции, то выработанная защита препятствует развитию болезни или смягчает тяжесть ее течения.Если мама сама была защищена от всех инфекций, то через плаценту она передаст своему малышу специфические антитела. Они обеспечат защиту ребенка от опасных инфекций в первые месяцы жизни. Но с трех-пяти месяцев начинают разрушаться антитела, защищающие от дифтерии, столбняка и т. д. К 12 месяцам разрушаются антитела, защищающие против кори. Поэтому именно с этого возраста необходимо начать создавать защиту с помощью введения вакцин. Чтобы к тому времени, когда антитела, которые получены от мамы разрушатся, у малыша была уже собственная защита.
В каждой стране формируется свой Национальный календарь профилактических прививок: он включает перечень инфекционных заболеваний, против которых целесообразно сформировать защиту, возраст, в котором целесообразно сделать ту или иную прививку. В календарь прививок входят не все возможные инфекционные заболевания, против которых существуют эффективные вакцины, а только те инфекции, которые могут иметь массовое (активное) распространение на территории страны, которые могут протекать тяжело, давая осложнения и даже смертельные исходы.
В календарь прививок входят не все возможные инфекционные заболевания, против которых существуют эффективные вакцины, а только те инфекции, которые могут иметь массовое (активное) распространение на территории страны, которые могут протекать тяжело, давая осложнения и даже смертельные исходы.
В Национальном календаре прививок обозначены минимальные интервалы между прививками. Эти интервалы нельзя сокращать, но в случае необходимости можно увеличивать.
В календаре прививок используется два термина: «вакцинация» и «ревакцинация». Что это такое?
«Вакцинация» — это первичное (или несколько первичных) введений вакцины (анатоксина), которое обеспечивает формирование базового иммунитета против той или иной инфекции. Например, для того, чтобы сформировать базовый иммунитет против дифтерии необходимо трехкратное введение противодифтерийного анатоксина.
«Ревакцинация» — повторное (или повторные) введения вакцины (анатоксина), которые способствуют поддержанию (продлению) сформированного ранее базового иммунитета.
- Эупента — (АКДС+ВГВ+ХИБ(V-1-2-3) комбинированная вакцина для профилактики дифтерии, столбняка, коклюша (цельно-клеточный компонент), вирусного гепатита В и гемофильной инфекции. Страна производитель-Корея.
- Имовакс Полио – инактивированная вакцина для профилактики полиомиелита. Страна производитель-Франция.
- Приорикс – комбинированная живая вакцина для профилактики кори, эпидемического паротита и краснухи. Страна производитель-Бельгия.
- АДС-м (в возрасте 6 и 16 лет)-адсорбированная комбинированная вакцина с уменьшенным содержанием антигена против дифтерии и столбняка. Страна производитель-Россия.
- АД-м (в возрасте 11 лет) – адсорбированная вакцина с уменьшенным содержанием антигена против
 Страна производитель – Россия.
Страна производитель – Россия. - Эувакс В – рекомбинантная вакцина для профилактики гепатита В. Страна производитель – Корея.
- VERO CELL – вакцина против SARS CoV-2 инактивированная с 5 лет. Страна производитель – Китай.
- Гриппол плюс – вакцина для профилактики гриппа с 6 мес. Страна производитель – Россия.
Вакцина ЭУПЕНТА (LG Chem, Korea) предназначена для профилактики пяти инфекций: коклюша (цельноклеточный компонент), дифтерии, столбняка, вирусного гепатита В и гемофильной инфекции.
Плановая вакцинация 1-3 против коклюша, дифтерии и столбняка будет осуществляться с использованием вакцины ЭУПЕНТА. Вакцинация 2-3, начатая вакцинами АКДС или Тетраксим может, быть продолжена или завершена вакциной ЭУПЕНТА (основание письмо МЗ РБ от 04.01.2018 №6-18/58)
Вакцина прошла все необходимые испытания на безопасность и эффективность и рекомендована ВОЗ к широкому применению.
Вакцина ЭУПЕНТА (АКДС+ВГВ+ХИБ) является удобным вакцинным препаратом, позволяющим сократить количество инъекций для достижения иммунитета сразу к пяти инфекционным болезням. Вакцину получат все дети первого года жизни 3-кратно.
Согласно письму МЗ РБ от 26.01.2018 № 7-18/1212 вакцинация против коклюша, дифтерии, столбняка, гемофильной инфекции, вирусного гепатита В и полиомиелита по следующим схемам:
1. Детям, получившим вакцинацию-1 и вакцинацию-2 против вирусного гепатита В с использованием моновакцин и не получившим вакцинацию против коклюша, дифтерии, столбняка и полиомиелита проводить:
1.1. вакцинацию-1 против коклюша, дифтерии и столбняка с использованием вакцины ЭУПЕНТА (при этом ребенок получит вакцинацию-3 против вирусного гепатита В и вакцинацию-1 против гемофильной инфекции) и вакцинацию-1 против полиомиелита с использованием инактивированной полиомиелитной вакцины;
1.2. вакцинацию-2 против коклюша, дифтерии и столбняка с использованием вакцины ЭУПЕНТА (при этом ребенок получит вакцинацию-4 против вирусного гепатита В и вакцинацию-2 против гемофильной инфекции) и вакцинацию-2 против полиомиелита с использованием инактивированной полиомиелитной вакцины;
1. 3. вакцинацию-3 против коклюша, дифтерии и столбняка с использованием вакцины АКДС и вакцинацию-3 против полиомиелита с использованием инактивированной полиомиелитной вакцины;
3. вакцинацию-3 против коклюша, дифтерии и столбняка с использованием вакцины АКДС и вакцинацию-3 против полиомиелита с использованием инактивированной полиомиелитной вакцины;
2. Детям, получившим вакцинацию-1, вакцинацию-2 и вакцинацию-3 против вирусного гепатита В с использованием моновакцин и не получившим вакцинацию против коклюша, дифтерии, столбняка и полиомиелита проводить:
2.1. вакцинацию-1 против коклюша, дифтерии и столбняка с использованием вакцины ЭУПЕНТА (при этом ребенок получит вакцинацию-4 противовирусного гепатита В и вакцинацию-1 против гемофильной инфекции) и вакцинацию-1 против полиомиелита с использованием инактивированной полиомиелитной вакцины;
2.2. вакцинацию-2 против коклюша, дифтерии и столбняка с использованием вакцины АКДС и вакцинацию-2 против полиомиелита с использованием инактивированной полиомиелитной вакцины;
2.3. вакцинацию-3 против коклюша, дифтерии и столбняка с использованием инактивированной полиомиелитной вакцины.
С целью формирования полноценной защиты против гемофильной инфекции вакцинацию 1 и (или) 2, начатую вакциной ЭУПЕНТА целесообразно завершить с использованием монокомпонентной вакцины против гемофильной инфекции (при наличии иммунобиологического лекарственного средства против данного инфекционного заболевания).
Вышеуказанная тактика вакцинации рассмотрена на заседании экспертного совета по иммунизации Министерства здравоохранения Республики Беларусь 24.01.2018 г. и одобрена его членами.
Согласно письму МЗ РБ от 20.02.2018 № 7-10/2405 «О вакцинации против вирусного гепатита В» вакцинация против вирусного гепатита В может проводится по следующим схемам:
1. в 3-дозовом графике первая доза вакцины против гепатита В (моновакцины) вводится при рождении, а вторая и третья дозы (моновакцины или комбинированной вакцины) – одновременно с введением первой и третьей дозы АКДС-содержащий вакцины.
2. в 4-дозовом графике первая доза вакцины против гепатита В (моновакцины) вводится при рождении, далее вводится три дозы (моновакцины или комбинированной вакцины), одновременно с введением трех доз АКДС-содержащий вакцины. При этом дополнительная доза вводимой вакцины против гепатита В является безопасной. Интервал между дозами должен быть минимун четыре недели.
Внимание! Имеющиеся моновакцины или комбинированные вакцины, содержащие компонент против гепатитаВ, могут быть взаимозаменяемыми в рамках программ иммунизации».
Почему родители до сих пор не решаются вакцинировать своих детей от COVID-19 | Педиатрия | JAMA
По состоянию на начало декабря более 2,3 миллиона детей в возрасте от 5 до 11 лет заболели COVID-19, 209 человек умерли. Хотя вакцина, которая на 90,7% эффективна для предотвращения болезни, была одобрена для детей младшего возраста в конце октября, эти цифры, по-видимому, недостаточно убедительны, чтобы убедить многих родителей вакцинировать своих детей.
iStock.com/Ivan Pantic
Согласно недавнему опросу, проведенному Kaiser Family Foundation (KFF), только 27% родителей детей в возрасте от 5 до 11 лет заинтересованы в иммунизации своих детей от COVID-19. , тогда как 30% заявили, что точно не будут вакцинировать своих детей. Треть родителей сказали, что они «подождут и посмотрят», прежде чем решить, как действовать дальше. Педиатр Пол Оффит, доктор медицинских наук, член консультативной группы Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), которая рекомендовала разрешение на использование в чрезвычайных ситуациях (EUA), сказал, что он не удивлен.
, тогда как 30% заявили, что точно не будут вакцинировать своих детей. Треть родителей сказали, что они «подождут и посмотрят», прежде чем решить, как действовать дальше. Педиатр Пол Оффит, доктор медицинских наук, член консультативной группы Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), которая рекомендовала разрешение на использование в чрезвычайных ситуациях (EUA), сказал, что он не удивлен.
«Освоение будет медленным и низким», — сказал он в интервью.
Offit находится на переднем крае вакцинологии в течение десятилетий и является одним из изобретателей ротавирусной вакцины, продаваемой как RotaTeq, которую FDA одобрило для младенцев в 2006 году. Когда-то печально известная тем, что она вызывала сильную диарею и рвоту у маленьких детей, теперь ротавирус редко поражает иммунизированных людей. Хотя болезнь менее смертоносна, чем COVID-19., Офит не видел такой негативной реакции на ротавирусную вакцину, которую в настоящее время получает вакцина против COVID-19. «Это был небольшой шприц в рот, и я думаю, что это было просто более приятно, если можно так выразиться… чем вводить кому-то вакцину», — сказал он.
«Это был небольшой шприц в рот, и я думаю, что это было просто более приятно, если можно так выразиться… чем вводить кому-то вакцину», — сказал он.
Тем не менее, CDC сообщает, что более 90% детей в США в возрасте до 24 месяцев иммунизированы с помощью инъекций против нескольких заболеваний, включая корь, эпидемический паротит и краснуху; почти 93% получили как минимум 3 из 4 рекомендуемых инъекций вакцины против полиомиелита. И примерно 95% воспитанников получили государственные прививки на 2019-2020 учебный год.
Так почему же родители более нерешительны, когда дело доходит до прививки от COVID-19? Для многих ответ связан со знакомством с рассматриваемыми вакцинами. Прививки для защиты от кори, эпидемического паротита и краснухи существуют с 1960-х годов. Но первая вакцина против COVID-19 была создана в прошлом году; это все еще относительно неизведанная территория. И в отличие от родителей 1960-х годов, сегодняшние родители могут быть завалены социальными сетями и интернет-сообщениями, пропагандирующими дезинформацию о вакцинах или недоверие к ним.
Успокоит ли наука страхи?
Согласно опросу KFF, родители с детьми в возрасте от 5 до 11 лет слишком мало послужного списка с вакциной против COVID-19.
«Родители очень боятся сделать со своим ребенком что-то, что может иметь долгосрочные последствия», — сказала Габриэль Шапиро, доктор медицинских наук, председатель Совета Американской психиатрической ассоциации по делам детей, подростков и их семей. Когда дело доходит до отказа от вакцинации против COVID-19, «основная причина, по которой я слышу, заключается в том, что она слишком новая; это экспериментально », [и] как психиатр, я думаю, как любой врач, нам поручено прояснить дезинформацию».
Родители беспокоятся не только о том, как вакцина против COVID-19 может повлиять на их детей, но и о том, как она может повлиять на них самих.
«Наибольшие опасения вызывают потенциальные неизвестные долгосрочные эффекты и серьезные побочные эффекты вакцины», — сказала Лиз Хамел, директор группы программы исследования общественного мнения и опросов KFF и ведущий автор отчета об обзоре. «Это действительно согласуется с тем, что мы видели с точки зрения беспокойства родителей о подростках, и даже с опасениями, которые привели к тому, что вакцины стали доступны для взрослых».
«Это действительно согласуется с тем, что мы видели с точки зрения беспокойства родителей о подростках, и даже с опасениями, которые привели к тому, что вакцины стали доступны для взрослых».
Но результаты клинических испытаний демонстрируют безопасность вакцины для детей младшего возраста. Исследование, опубликованное в New England Journal of Medicine ( NEJM ) и финансируемое производителями BNT162b2 Pfizer и BioNTech, не выявило серьезных побочных эффектов, связанных с вакциной, среди 1517 полностью вакцинированных участников в возрасте от 5 до 11 лет. После медианного наблюдения в течение 2,3 месяца исследователи пришли к выводу, что BNT162b2 безопасен, иммуногенен и эффективен для изучаемой ими молодой возрастной группы.
Также растет объем данных о подростках. Поскольку FDA расширило EUA BNT162b2 в мае для детей в возрасте от 12 до 15 лет, примерно 15,6 миллиона человек в возрасте от 12 до 17 лет получили по крайней мере 1 дозу по состоянию на начало декабря. В ноябре Pfizer и BioNTech объявили, что их вакцина предотвращает COVID-19 в течение как минимум 4 месяцев среди привитых молодых людей при анализе 2228 участников клинических испытаний в возрасте от 12 до 15 лет. Хотя подростки имеют несколько повышенный риск миокардита — воспаления сердечной мышцы — от BNT162b2, вероятность развития заболевания в результате вакцинации редка. Фактически, Консультативный комитет CDC по практике иммунизации определил в июне, что преимущества мРНК COVID-19вакцины перевешивают их риски, включая риск поствакцинального миокардита, для всех подходящих возрастных групп. (В июне BNT162b2 еще не был разрешен для детей младше 12 лет.)
В ноябре Pfizer и BioNTech объявили, что их вакцина предотвращает COVID-19 в течение как минимум 4 месяцев среди привитых молодых людей при анализе 2228 участников клинических испытаний в возрасте от 12 до 15 лет. Хотя подростки имеют несколько повышенный риск миокардита — воспаления сердечной мышцы — от BNT162b2, вероятность развития заболевания в результате вакцинации редка. Фактически, Консультативный комитет CDC по практике иммунизации определил в июне, что преимущества мРНК COVID-19вакцины перевешивают их риски, включая риск поствакцинального миокардита, для всех подходящих возрастных групп. (В июне BNT162b2 еще не был разрешен для детей младше 12 лет.)
«Реальный риск заключается в реактогенности, поэтому в месте укола будет больно, и это продлится день или два». по словам Роберта Френка-младшего, доктора медицины, который является соавтором исследования NEJM и является директором Исследовательского центра вакцины Гэмбла в Медицинском центре детской больницы Цинциннати. Другие побочные эффекты у детей и подростков схожи: легкие или умеренные головные боли и усталость, которые проходят в течение нескольких дней. Иногда возникают гриппоподобные симптомы, такие как лихорадка и тошнота, но они, как правило, быстро проходят.
Другие побочные эффекты у детей и подростков схожи: легкие или умеренные головные боли и усталость, которые проходят в течение нескольких дней. Иногда возникают гриппоподобные симптомы, такие как лихорадка и тошнота, но они, как правило, быстро проходят.
Несмотря на это, родители все еще опасаются, что их ребенок будет исключением. «Вы просите родителей ввести своему ребенку биологический агент, и я думаю, что понятно отказаться от этого», — сказал Оффит, подчеркнув, как «наука может справиться с этими страхами».
Только факты
Сара «Салли» Гоза, доктор медицины, бывший президент Американской академии педиатрии, объясняет родительский страх отсутствием фактов. «Родители в замешательстве, потому что вокруг так много дезинформации», — сказал Гоза в интервью.
Это не обязательно имело место, когда в 1990-х годах стала доступна вакцина против ветряной оспы, продаваемая как Varivax. Оффит напомнил, что распространение вакцины было медленным, поэтому производитель запустил кампанию с категорическим сообщением о том, что некоторые родители потеряли ребенка из-за ветрянки. До вакцины болезнь редко считалась опасной, не говоря уже о летальном исходе.
До вакцины болезнь редко считалась опасной, не говоря уже о летальном исходе.
«Когда компания стала лучше распространять информацию о том, что каждый год от ветрянки умирает от 75 до 100 детей, — и они показывали фотографии геморрагической ветряной оспы, — я думаю, это разбудило не только родителей, я думаю, разбудил врачей к тому факту, что… если это можно предотвратить безопасно, это нужно предотвратить», — отметил Оффит.
«Они слышат, что вакцина против COVID-19 была сделана в спешке, что она все еще находится под разрешением на использование в чрезвычайных ситуациях, поэтому она не полностью лицензирована FDA, и они не понимают, что это значит», — добавил Гоза. «Вот почему я призываю всех родителей, у которых есть проблемы, поговорить со своими врачами».
Данные и исследования KFF в педиатрии показывают, что, когда речь идет о безопасности вакцин, педиатры являются одними из самых надежных источников информации.
«Я бы никогда не сказал родителям, что они не должны волноваться — это то, что делают родители», — сказал Гоза. «Но наша работа как педиатров состоит в том, чтобы помочь им преодолеть это беспокойство и узнать, что эта вакцина безопасна и эффективна».
«Но наша работа как педиатров состоит в том, чтобы помочь им преодолеть это беспокойство и узнать, что эта вакцина безопасна и эффективна».
Даже при заверении врача родители все еще боятся неизвестного. Например, отметил Гоза, многие люди считают технологию мРНК новой, хотя она существует уже почти 2 десятилетия. И мысли о новых технологиях часто приходят с трепетом перед будущим.
Согласно октябрьскому опросу KFF, основные опасения родителей по поводу вакцины против COVID-19 связаны с долгосрочными и серьезными побочными эффектами, включая проблемы с фертильностью в будущем. Проект COVID States Project, возглавляемый консорциумом исследователей из различных учреждений и областей, опубликовал аналогичные выводы о долгосрочных последствиях в одном из своих октябрьских отчетов об опросе. Но такие опасения были рассмотрены и во многих случаях опровергнуты. Основываясь на исторических данных о вакцинах, большинство побочных эффектов возникают в течение первых 6 недель после иммунизации, а негативные долгосрочные последствия маловероятны.
«Теперь у нас есть данные о введении этой вакцины за более чем год, и мы не видели никаких долгосрочных серьезных побочных эффектов от нее», — сказал Гоза.
Хотя серьезные побочные эффекты, такие как анафилаксия или тромбоз, возможны, они также редки. И исследователи не нашли никаких доказательств того, что вакцина против COVID-19 приводит к бесплодию. Несмотря на отсутствие тяжелых осложнений, связанных с вакциной против COVID-19, сомнения остаются высокими. Тем не менее, было время, когда вакцины были приняты общественностью — даже после фармацевтической катастрофы.
Время доверия
В конце 1940-х полиомиелит стал настолько распространенным в Соединенных Штатах, что многие люди практиковали социальное дистанцирование. Когда Джонас Солк, доктор медицины, изобрел вакцину против полиомиелита в 1950-х годах, публика благоговела перед ним. Полиомиелит в основном поражал детей, и больные часто становились парализованными. В 1955 году — в том же году, когда вакцина стала доступной — Cutter Laboratories произвела партии, содержащие живой вирус, а не неактивный. В результате примерно у 40 000 детей от вакцины развился абортивный полиомиелит; 164 человека были навсегда парализованы, 10 умерли. Но это не помешало большинству родителей тогда — или сейчас — сделать своим детям прививки от этой болезни. После временной приостановки вакцинационная кампания пошла полным ходом.
В результате примерно у 40 000 детей от вакцины развился абортивный полиомиелит; 164 человека были навсегда парализованы, 10 умерли. Но это не помешало большинству родителей тогда — или сейчас — сделать своим детям прививки от этой болезни. После временной приостановки вакцинационная кампания пошла полным ходом.
«Тот факт, что родители все еще были готовы сделать прививку от полиомиелита после инцидента с Каттером, можно объяснить тем фактом, что в то время люди больше доверяли правительству, компаниям и медицинскому сообществу», — сказал Оффит, который написал книгу об этом инциденте. «Если представители общественного здравоохранения говорили, что вакцину против полиомиелита теперь можно безопасно вводить, люди им верили».
Мать всех забот
Сегодня антипрививочное движение растет и сильно политизируется. Данные KFF 2020 показывают, что доверие к официальным источникам, таким как CDC, ослабло, особенно среди консерваторов. Исследования, опубликованные в American Politics Research и Socius: Sociological Research for a Dynamic World показывают, что по сравнению с демократами республиканцы с большей вероятностью одобряют дезинформацию о детской вакцине и с меньшей вероятностью делают прививку от COVID-19. Но Оффит не считает, что политические дебаты о COVID-19 играют ведущую роль в принятии родителями решений о том, следует ли иммунизировать своих детей.
Но Оффит не считает, что политические дебаты о COVID-19 играют ведущую роль в принятии родителями решений о том, следует ли иммунизировать своих детей.
«Конечно, вакцины против COVID-19 носят политический характер, и в прошлом этого не было», — сказал Оффит. «Я не знаю, относится ли это к детям от 5 до 11 лет. Я думаю, что здесь вы просто наблюдаете общую нерешительность в отношении вакцин, которая возникает при прививке вашему ребенку биологического агента, в котором вы не очень хорошо разбираетесь».
Особенно это беспокоит матерей. В октябрьском отчете проекта COVID States Project отмечается, что по сравнению с отцами в возрасте 18 лет и старше и матерями в возрасте 36 лет и старше, матери в возрасте от 18 до 35 лет значительно больше обеспокоены вакциной против COVID-19. Согласно предыдущим результатам проекта, матери остались непоколебимыми в своих сомнениях, хотя никаких причинно-следственных выводов сделано не было.
«Отсутствие движений у молодых матерей особенно бросается в глаза», — сказал Мэтью Симонсон, доктор философии, научный сотрудник Пенсильванского университета, соавтор обоих отчетов об исследовании COVID States Project. «Независимо от причины, если мамы больше обеспокоены и ведут своих детей к врачу, то мнение мамы будет иметь большее значение для уровня вакцинации в нашей стране, чем мнение отца».
«Независимо от причины, если мамы больше обеспокоены и ведут своих детей к врачу, то мнение мамы будет иметь большее значение для уровня вакцинации в нашей стране, чем мнение отца».
Френк соглашается, так как он чаще всего встречается с матерями во время приема пациентов. «Мамы принимают решение [о вакцинации], и если вы посмотрите, кто приводит детей в кабинеты врачей, в подавляющем большинстве случаев это будут мамы».
Как это ни парадоксально, некоторые обеспокоенные родители детей в возрасте от 5 до 11 лет сами вакцинируются. «Среди тех родителей, которые вакцинированы, 39% говорят, что подождут и увидят, как это работает, а 13% говорят, что они определенно не будут вакцинировать своего ребенка», — сказал Хамель, ссылаясь на статистическую разбивку, не представленную в публичном октябрьском отчете KFF. .
По словам Шапиро, такие опасения проистекают из защитного инстинкта. «Родители готовы рискнуть своими побочными эффектами», — сказала она. «Такова природа родителей, которые думают: «Пусть у меня будет плохой результат от вакцины, я не хочу, чтобы она была у вас».
Но что, если ребенок хочет вакцину? Зачастую для несовершеннолетних все сводится к согласию родителей, хотя и это зависит от законов штата. Тем не менее, Френк надеется, что родители удовлетворят просьбу. «Мой друг, местный педиатр, сказал, что не раз к ним приходил подросток, чтобы сделать прививку, а мама не была привита, и поэтому подросток уговорил маму сделать прививку. перед отъездом, — сказал он.
У Гозы был похожий опыт. «На самом деле не так давно у меня был родитель, чей ребенок получил вакцину, потому что они действительно этого хотели, а родитель все еще не был вакцинирован», — сказала она. «Это случается».
Эксперты надеются, что разработка вакцины сохранится, особенно с приближением зимы.
«Медицинские работники должны поддерживать родителей и семьи, помогать им в обучении и стараться вакцинировать как можно больше детей», — сказал Шапиро. «Мы должны работать вместе, чтобы преодолеть эту пандемию».
Наверх
Информация о статье
Конфликт интересов Раскрытие информации: Д-р Френк сообщил о получении грантов на исследования от производителей вакцин Pfizer и Moderna. Он также входит в консультативные советы Pfizer, Merck и Johnson & Johnson. Г-жа Хамель и д-р Гоза, Оффит, Шапиро и Симонсон не сообщили о раскрытии информации.
Он также входит в консультативные советы Pfizer, Merck и Johnson & Johnson. Г-жа Хамель и д-р Гоза, Оффит, Шапиро и Симонсон не сообщили о раскрытии информации.
К этой статье прилагается сводка медицинских новостей JAMA, звуковой обзор содержания новостей, появившихся в выпусках этого месяца от ДЖАМА . Чтобы послушать этот и другие эпизоды, посетите подкаст медицинских новостей JAMA.
Влияние пандемии COVID-19 на охват плановой вакцинацией детей и подростков: систематический обзор
1. Dinleyici EC, Borrow R, Safadi MAP, van Damme P, Munoz FM. Вакцины и стратегии плановой иммунизации во время пандемии COVID-19. Hum Вакцина Иммунотер. 2021;17(2):400-477. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2. Ву Дж, Ю В, Цао Л и др. Эффективность наверстывающих прививок после COVID-19сдерживание — Китай, 2020 г. China CDC Wkly. 2020;2(50):968‐974. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3.
Макдональд Н., Комо Дж., Дьюб Э., Буччи Л. COVID-19 и пропущенные плановые прививки: разработка эффективных мер наверстывания в Канаде. Может J Общественное здравоохранение. 2020;111(4):469-472. [Бесплатная статья PMC] [PubMed] [Google Scholar]
COVID-19 и пропущенные плановые прививки: разработка эффективных мер наверстывания в Канаде. Может J Общественное здравоохранение. 2020;111(4):469-472. [Бесплатная статья PMC] [PubMed] [Google Scholar]
4. Бечини А., Гарамелла Г., Джаммарко Б. и др. Педиатрическая деятельность и приверженность вакцинации в период эпидемии COVID-19 в Тоскане, Италия: опрос педиатров. J Prev Med Hyg. 2020;61(2):E125‐E129. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Хашеми-Шахри С.М., Барфар Э., Ансари-Могаддам А., Хаммарния М., Сетоодехзаде Ф., Окати-Алиабад Х. Экономические последствия COVID-19 в странах региона Ближнего Востока и Северной Африки. J Adv Med Biomed Res. 2020;28(131):304-306. [Google Scholar]
6. СейедАлинаги С., Мертак М., МохсениПур М. и др. Генетическая восприимчивость к COVID-19: систематический обзор текущих данных. Евр J Med Res. 2021;26(1):46. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7.
СейедАлинаги С., Мирзапур П., Дадрас О. и др. Характеристика различных вариантов SARS-CoV-2 и связанных с ними заболеваемости и смертности: систематический обзор. Евр J Med Res. 2021;26(1):51. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Характеристика различных вариантов SARS-CoV-2 и связанных с ними заболеваемости и смертности: систематический обзор. Евр J Med Res. 2021;26(1):51. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Огунделе О.А., Омотосо А.А., Фагбеми А.Т. Вспышка COVID-19: потенциальная угроза деятельности программы плановой вакцинации в Нигерии. Hum Вакцина Иммунотер. 2021;17(3):661-663. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Дадрас О., Алинаги С.А.С., Карими А. и др. Последствия COVID-19процедуры профилактики других распространенных инфекций: систематический обзор. Евр J Med Res. 2021;26(1):67. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. СейедАлинаги С., Афсахи А.М., МохсениПур М. и др. Поздние осложнения COVID-19; систематический обзор имеющихся данных. Arch Acad Emerg Med. 2021;9(1):e14. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11.
Чандир С., Сиддики Д., Мехмуд М. и др. Влияние ответных мер на пандемию COVID-19 на использование плановой иммунизации в Синде, Пакистан: анализ провинциального электронного регистра иммунизации. вакцина. 2020;38(45):7146-7155. [Бесплатная статья PMC] [PubMed] [Google Scholar]
вакцина. 2020;38(45):7146-7155. [Бесплатная статья PMC] [PubMed] [Google Scholar]
12. Алдахил Х., Альбеда Н., Алтураики Н., Аладжлан Р., Абусалих Х. Нерешительность в отношении вакцинации детей как предиктор намерения матерей вакцинировать своих детей против COVID-19 в Саудовской Аравии. J заразить общественное здравоохранение. 2021;14(10):1497-1504. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Олорунсайе Ч.З., Юсуф К.К., Рейнхарт К., Салиху Х.М. COVID-19 и вакцинация детей: системный подход к устранению пробелов в иммунизации. Int J MCH AIDS. 2020;9(3):381-385. [Бесплатная статья PMC] [PubMed] [Google Scholar]
14. Сато АПС. Пандемия и охват вакцинацией: проблемы возвращения в школы. Преподобный Сауд Публика. 2020;54:115. [Бесплатная статья PMC] [PubMed] [Google Scholar]
15.
Лэнгдон-Эмбри М., Пападука В., Ченг И., Альмашхадани М., Тернье А., Цукер Дж. Заметки с мест: восстановление рутинной вакцинации детей после снижения во время пандемии COVID-19 — Нью-Йорк, 1 марта — 27 июня, 2020. MMWR Morb Mortal Wkly Rep. 2020; 69: 999-1001. [Бесплатная статья PMC] [PubMed] [Google Scholar]
MMWR Morb Mortal Wkly Rep. 2020; 69: 999-1001. [Бесплатная статья PMC] [PubMed] [Google Scholar]
16. Кэш Р., Патель В. Подорвал ли COVID-19 глобальное здравоохранение? Ланцет. 2020;395(10238):1687‐1688. [Бесплатная статья PMC] [PubMed] [Google Scholar]
17. Ранабхат С.Л., Яковлевич М., Ким С.Б., Симхада П. Пандемия COVID-19: возможность для всеобщего охвата услугами здравоохранения. Фронт Паб Здоровье. 2021;9:673542. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Сантоли Дж. М., Линдли М. С., ДеСильва М. Б. и др. Последствия пандемии COVID-19 для рутинного заказа и введения педиатрических вакцин — США, 2020 г. MMWR Morb Mortal Wkly Rep. 2020;69(19):591-593. [PubMed] [Google Scholar]
19. Селл Х., Асси А., Драйджер С.М. и др. Непрерывность программ плановой иммунизации в Канаде во время пандемии COVID-19. вакцина. 2021;39(39):5532-5537. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20.
Прадхан Х.С., Мохакуд Н.К., Кавита А., Наяк М.К. , Сатпати С.К. Наличные расходы на здравоохранение в связи с диареей среди детей в возрасте до пяти лет в клинической больнице в Одише, Индия. Индийское Дж. Общественное здравоохранение. 2020;64(3):252. [PubMed] [Академия Google]
, Сатпати С.К. Наличные расходы на здравоохранение в связи с диареей среди детей в возрасте до пяти лет в клинической больнице в Одише, Индия. Индийское Дж. Общественное здравоохранение. 2020;64(3):252. [PubMed] [Академия Google]
21. Прадхан Х.С., Мохакуд Н.К., Пугалия Р., Сатпати С.К. Стоимость лихорадочных заболеваний среди детей в возрасте до пяти лет, исследование в учебной больнице третичной помощи в Одише. Индия J Glob Infect Dis. 2019;11(4):135-139. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Seiler M, Goldman RD, Staubli G, et al. Намерение родителей сделать прививку от гриппа во время пандемии COVID-19 в двух регионах Швейцарии. Swiss Med Wkly. 2021;151:w20508. [PubMed] [Google Scholar]
23. Сокол Р.Л., Груммон А.Х. COVID-19и намерение родителей вакцинировать своих детей от гриппа. Педиатрия. 2020;146(6):e2020022871. [Бесплатная статья PMC] [PubMed] [Google Scholar]
24.
Хоу Зи, Сонг С, Ду Ф и др. Влияние эпидемии COVID-19 на поведение китайских детей и подростков в отношении профилактики и вакцинации: результаты онлайн-опроса. JMIR Надзор за общественным здравоохранением. 2021;7(5):e26372. [Бесплатная статья PMC] [PubMed] [Google Scholar]
JMIR Надзор за общественным здравоохранением. 2021;7(5):e26372. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Алвес Дж.Г., Фигейроа Дж.Н., Уркиа М.Л. Влияние COVID-19по иммунизации бразильских младенцев. Int J Infect Dis. 2021;107:252-253. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Фалькенштейн Хагандер, К. , Аронссон Б., Даниэльссон М., Лепп Т., Кулане А., Шоллин А.Л. Национальное шведское исследование показало, что службы охраны здоровья детей и программы плановой иммунизации были устойчивыми во время ранней пандемии COVID-19. Акта Педиатр. 2021;110(9):2559-2566. [Бесплатная статья PMC] [PubMed] [Google Scholar]
27. Ахмед Т., Рахман А.Е., Амоле Т.Г. и др. Эффект COVID-19на услуги по охране здоровья матери, новорожденного и ребенка (ЗМНД) в Бангладеш, Нигерии и Южной Африке: призыв к контекстуальным ответным мерам на пандемию в СНСД. Int J Equity Health. 2021;20(1):77. [Бесплатная статья PMC] [PubMed] [Google Scholar]
28.
Алмуса З. , Алхамуд Х.Х., Алхалаф А.Б. и др. Влияние пандемии коронавирусной болезни 2019 (COVID-19) на плановую педиатрическую вакцинацию в восточном регионе. Медицинские науки Саудовской Аравии. 2020;24(106):4672-4681. [Google Scholar]
, Алхамуд Х.Х., Алхалаф А.Б. и др. Влияние пандемии коронавирусной болезни 2019 (COVID-19) на плановую педиатрическую вакцинацию в восточном регионе. Медицинские науки Саудовской Аравии. 2020;24(106):4672-4681. [Google Scholar]
29. Alrabiaah AA, Alshaer AH, Estrella SMC, et al. Последствия коронавирусной болезни 2019пандемии на показатели охвата плановой детской иммунизацией в главной университетской больнице в Саудовской Аравии. Saudi Med J. 2020;41(11):1197-1203. [Бесплатная статья PMC] [PubMed] [Google Scholar]
30. Алсухайбани М., Алакил А. Влияние пандемии COVID-19 на плановую иммунизацию детей в Саудовской Аравии. Вакцины (Базель). 2020;8(4):581. [Бесплатная статья PMC] [PubMed] [Google Scholar]
31. Брамер К.А., Кимминс Л.М., Суонсон Р. и соавт. Снижение охвата вакцинацией детей во время COVID-19пандемия – реестр улучшения ухода за больными штата Мичиган, май 2016 г. – май 2020 г. MMWR Morb Mortal Wkly Rep. 2020;69(20):630-631. [PubMed] [Google Scholar]
32. Буонсенсо Д., Чиникола Б., Каллон М.Н., Йодис Ф. Детское здравоохранение и иммунизация в странах Африки к югу от Сахары во время пандемии COVID-19. Фронт Педиатр. 2020;8:517. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Буонсенсо Д., Чиникола Б., Каллон М.Н., Йодис Ф. Детское здравоохранение и иммунизация в странах Африки к югу от Сахары во время пандемии COVID-19. Фронт Педиатр. 2020;8:517. [Бесплатная статья PMC] [PubMed] [Google Scholar]
33. Кариас С., Паваскар М., Ньяку М. и др. Потенциальное влияние пандемии COVID-19 на охват вакцинацией детей: тематическое исследование введения противокоревой вакцины в Соединенных Штатах (США). вакцина. 2021;39(8):1201-1204. [Бесплатная статья PMC] [PubMed] [Google Scholar]
34. Чандир С., Сиддики Д.А., Мехмуд М. и др. Влияние ответных мер на пандемию COVID-19 на плановую иммунизацию в Синде, Пакистан: анализ данных провинциального электронного регистра иммунизации. вакцина. 2020;38(45):7146-7155. [Бесплатная статья PMC] [PubMed] [Google Scholar]
35.
Руссо Р., Боццола Э., Пальма П., Корселло Г., Виллани А. Плановые детские прививки в период изоляции от COVID-19: опрос Итальянского педиатрического общества. Ital J Pediatr. 2021;47(1):72. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
36. Silveira MF, Tonial CT, Goretti KMA и др. Пропущенные детские прививки во время пандемии COVID-19 в Бразилии: анализ обычной статистики и национального обследования домохозяйств. вакцина. 2021;39(25):3404-3409. [PubMed] [Google Scholar]
37. Тегегне А.В., Гидафи А.К., Мамо Д.Г., Васси С.Т., Менги З.А. Статус иммунизации и проблемы во время COVID-19 и связанные с ним факторы среди детей в возрасте 10–23 месяцев в южном регионе, Эфиопия, 2020 г. Pediatr Health Med Ther. 2021;12:101-109. [Бесплатная статья PMC] [PubMed] [Google Scholar]
38. Ю Дж. Х., Чон Х. Дж., Ким С. Дж. и др. Устойчивый охват вакцинацией во время эпидемии коронавирусной болезни 2019 года в Республике Корея. вакцина. 2020;9(1):2. [Бесплатная статья PMC] [PubMed] [Google Scholar]
39. Чжун И, Клэпхэм Х.Е., Айшвория Р. и др. Детские прививки: скрытое влияние COVID-19 на детей в Сингапуре. вакцина. 2021;39(5):780-785. [Бесплатная статья PMC] [PubMed] [Google Scholar]
40. Чехлаби Н., Арраб Р., Эттаир С., Дини Н. Последствия COVID-19пандемия по иммунизации детей в Марокко: электронный опрос 103 педиатров. Pan Afr Med J. 2021; 38:134. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Чехлаби Н., Арраб Р., Эттаир С., Дини Н. Последствия COVID-19пандемия по иммунизации детей в Марокко: электронный опрос 103 педиатров. Pan Afr Med J. 2021; 38:134. [Бесплатная статья PMC] [PubMed] [Google Scholar]
41. Кара А., Ильбай С., Топач О. и др. Изменение показателей вакцинации и оценка восприятия врачами возможного влияния пандемии SARS-CoV-2 на вакцинацию детей в Анкаре, Турция. Hum Вакцина Иммунотер. 2021;17(10):3457-3462. [Бесплатная статья PMC] [PubMed] [Google Scholar]
42. Китано Т., Аоки Х. Модель возрастающего бремени инвазивных Haemophilus influenzae типа b из-за снижения вакцинации детей во время вспышки COVID-19: динамическая модель передачи в Японии. вакцина. 2021;39(2):343-349. [PubMed] [Google Scholar]
43.
Китано Т., Аоки Х. Увеличение бремени инвазивной пневмококковой инфекции, связанное со снижением вакцинации детей с использованием модели динамической передачи в Японии: вторичное воздействие COVID-19. Компьютер Биол Мед. 2021;133:104429. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
44. Масреша Б.Г., Люс Р. мл., Шибеши М.Е. и др. Проведение плановой иммунизации в отдельных африканских странах в течение первых шести месяцев пандемии COVID-19. Pan Afr Med J. 2020; 37 (Приложение 1): 12. [Бесплатная статья PMC] [PubMed] [Google Scholar]
45. Мирету Д.Г., Асфав З.А., Аддис С.Г. Влияние пандемии COVID-19 на охват вакцинацией детей в возрасте от 15 до 23 месяцев в городе Десси, северо-восточная Эфиопия. Hum Вакцина Иммунотер. 2020;2021:1-9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
46. О’Лири С.Т., Трефрен Л., Рот Х., Мосс А., Северсон Р., Кемпе А. Количество вакцинаций детей и подростков, проведенных до и после вспышки COVID-19 в Колорадо. JAMA Педиатр. 2021;175(3):305-307. [Бесплатная статья PMC] [PubMed] [Google Scholar]
47.
Джайн Р., Чопра А., Фалезан С., Патель М., Дюпас П. Сбои в иммунизации, связанные с COVID-19, в Раджастане, Индия: ретроспективное обсервационное исследование. вакцина. 2021;39(31):4343-4350. [Бесплатная статья PMC] [PubMed] [Google Scholar]
вакцина. 2021;39(31):4343-4350. [Бесплатная статья PMC] [PubMed] [Google Scholar]
48. McDonald HI, Tessier E, White JM и др. Раннее влияние пандемии коронавирусной болезни (COVID-19) и мер физического дистанцирования на плановые детские прививки в Англии, январь-апрель 2020 г. Euro Surveill. 2020;25(19):2000848. [Бесплатная статья PMC] [PubMed] [Google Scholar]
49. Ахмед С., Аджисола М., Азим К. и др. Влияние реакции общества на COVID-19 на доступ к медицинской помощи для решения проблем со здоровьем, не связанных с COVID-19, в трущобах Бангладеш, Кении, Нигерии и Пакистана: результаты до COVID-19 и COVID-19Взаимодействие с заинтересованными сторонами в режиме самоизоляции. BMJ Глоб Здоровье. 2020;5(8):e003042. [Бесплатная статья PMC] [PubMed] [Google Scholar]
50.
Chang HJ, Huang N, Lee CH, Hsu YJ, Hsieh CJ, Chou YJ. Влияние эпидемии атипичной пневмонии на использование медицинских услуг: атипичная пневмония и боязнь атипичной пневмонии. Am J Общественное здравоохранение.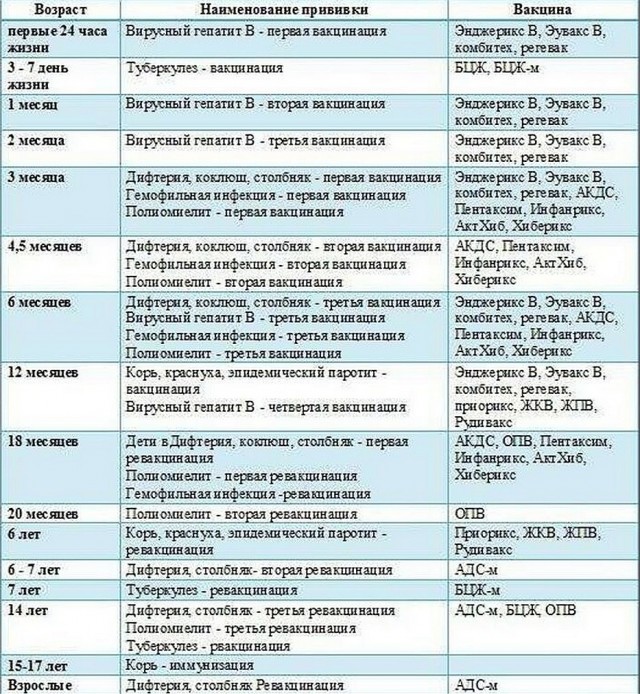 2004;94(4):562-564. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2004;94(4):562-564. [Бесплатная статья PMC] [PubMed] [Google Scholar]
51. Lanzi S, Pousaz A, Buso G, Mazzolai L, Calanca L. Частичное домашнее заключение во время пандемии COVID-19, физические функции и физическая активность у пациентов с симптоматическим заболеванием периферических артерий нижних конечностей. Васк Мед. 2021;26(4):437-439. [Бесплатная статья PMC] [PubMed] [Google Scholar]
52. Брамер К.А., Кимминс Л.М., Суонсон Р. и соавт. Снижение охвата вакцинацией детей во время пандемии COVID-19 — Реестр улучшения медицинского обслуживания штата Мичиган, май 2016 г. — май 2020 г. Am J Transplant. 2020;20(7):1930–1931. [Бесплатная статья PMC] [PubMed] [Google Scholar]
53. Хоу Зи, Сонг С, Ду Ф и др. Влияние эпидемии COVID-19 на поведение китайских детей и подростков в отношении профилактики и вакцинации: поперечное онлайн-исследование. JMIR Надзор за общественным здравоохранением. 2021;7(5):e26372. [Бесплатная статья PMC] [PubMed] [Google Scholar]
54. Гранди Дж., Биггс Б.А. Влияние конфликта на охват иммунизацией в 16 странах. Int J Health Policy Manag. 2019;8(4):211-221. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Гранди Дж., Биггс Б.А. Влияние конфликта на охват иммунизацией в 16 странах. Int J Health Policy Manag. 2019;8(4):211-221. [Бесплатная статья PMC] [PubMed] [Google Scholar]
55. Пагио Дж. А., Яо Дж. С., Ди EC. Положительная сторона COVID-19: повышенный глобальный интерес к вакцинам против пневмококка и гриппа, инфодемиологическое исследование. вакцина. 2020;38(34):5430-5435. [Бесплатная статья PMC] [PubMed] [Google Scholar]
56. Всемирная организация здравоохранения . Руководство по услугам плановой иммунизации во время COVID-19пандемия в Европейском регионе ВОЗ, 20 марта 2020 г. Всемирная организация здравоохранения. Региональное бюро для Европы; 2020. Доступно по адресу: https://apps.who.int/iris/bitstream/handle/10665/334123/WHO-EURO-2020-1059-40805-55114-eng.pdf
57. Патель М., Ли А.Д., Редд С.Б. и др. Увеличение числа случаев кори — США, 1 января — 26 апреля 2019 г. MMWR Morb Mortal Wkly Rep. 2019; 68:402-404. doi: 10.15585/mmwr.mm6817e1 [PubMed] [CrossRef] [Google Scholar]
58.

 Ташкент, Алмазарский р-н, ул. Тахтапуль, 341а.
Ташкент, Алмазарский р-н, ул. Тахтапуль, 341а. Страна производитель – Россия.
Страна производитель – Россия.