Лучшие противовирусные средства у взрослых и детей
Борьба с вирусными заболеваниями разного рода всегда будет актуальной. Российская и зарубежная фармацевтическая промышленность производит большое количество препаратов, помогающих в кратчайшие сроки избавиться и от симптомов, и от причин болезни. На рынке представлено большое количество лекарственных средств, которые значительно отличаются друг от друга по принципу действия, стоимости.
Мы постарались облегчить вам проблему выбора подобной продукции и составили рейтинг лучших противовирусных препаратов. Когда мы выбирали лекарства для включения в этот обзор, то предварительно провели тщательный мониторинг рынка подобных препаратов, выбрав наиболее эффективные и при этом приемлемые по цене. Опирались мы во многом на отзывы пользователей и на соотношение цены и качества лекарства. Надеемся, что после внимательного изучения рейтинга вы сумеете подобрать для себя наиболее эффективную продукцию. Однако необходимо помнить, что обзор представляет собой рекомендательную статью, которая не является призывом к покупке той или иной продукции. Перед применением любого лекарства обязательно нужно проконсультироваться с лечащим врачом, так как у каждого состава имеются противопоказания и побочные эффекты.
Перед применением любого лекарства обязательно нужно проконсультироваться с лечащим врачом, так как у каждого состава имеются противопоказания и побочные эффекты.
Профилактические средства
3. Цитовир-3
Данная продукция отечественного производства разрабатывалась специально для того, чтобы снизить риск возможного инфицирования вирусными заболеваниями, однако ее зачастую используют и для лечения болезней. Лекарство подходит как взрослым, так и детям. Активные соединения хорошо борются с вирусами гриппа, а также прочими патогенными микроорганизмами, которые являются причиной возникновения ОРВИ. Препарат нужно пить курсами, причем после принятия средства удается в значительной степени минимизировать вероятность заболевания. Если же человек уже успел подхватить инфекцию, то с помощью этого лекарства можно снять многие симптомы и облегчить состояние болеющего человека. В качестве активных действующих соединений здесь используются три вещества – гидрохлорид бендазола, дипептид глутамил-триптофана и аскорбиновая кислота. Первое вещество предназначено для питания и дополнительного укрепления иммунной системы, второе отличается аналогичным действием, а вот аскорбиновая кислота или витамин С помогает также и восстановить ткани. В составе еще есть несколько вспомогательных компонентов, которые позволяют усилить терапевтический эффект.
Первое вещество предназначено для питания и дополнительного укрепления иммунной системы, второе отличается аналогичным действием, а вот аскорбиновая кислота или витамин С помогает также и восстановить ткани. В составе еще есть несколько вспомогательных компонентов, которые позволяют усилить терапевтический эффект.
Лекарство выпускается в нескольких вариантах – сироп, порошок, капсулы, ароматизированный порошок. Препарат запускает активный синтез интерферона в теле человека – данное соединение предназначено для быстрого подавления инфекции. Интерферон вступает в контакт с клетками и не допускает сборки вирусных частиц. Патологические процессы локализуются и нейтрализуются в кратчайшие сроки. Аскорбиновая кислота обеспечивает лучшую проницаемость капиллярных сосудов, снимая тем самым отечность и избавляя от воспалительного процесса. Препарат также хорошо защищает ткани от окислительного стресса.
Преимущества:
- Универсальное средство, которое может использоваться как для профилактики, так и для лечения;
- Относится к среднему ценовому диапазону;
- Можно давать детям в возрасте от 6 лет;
- Минимальное количество противопоказаний.

Недостатки:
- Полностью синтетическое средство;
- Справляется не со всеми формами гриппа и ОРВИ.
Цитовир-3
2. Дибазол-убф таблетки
Лекарство выпускается еще с советских времен и вплоть до сегодняшнего дня не потеряло своей актуальности, причем оно характеризуется вполне приемлемой стоимостью. В продаже встречается в виде таблеток, обладает превосходными иммуностимулирующими характеристиками. Содержащиеся здесь активные компоненты в значительной степени активизируют выработку макрофагов, также позволяют увеличить количество интерферона в организме. Состав предназначен для пациентов любых возрастов, обладает незначительным количеством противопоказаний, его назначают при различных простудных заболеваниях и некоторых формах гриппа. Основной активный компонент характеризуется обезболивающим, сосудорасширяющим и гипотоническим действием. С его помощью удается также понизить артериальное давление, активизировать приток дополнительного количества крови к участкам миокарда, страдающим от ишемической болезни и гипоксии.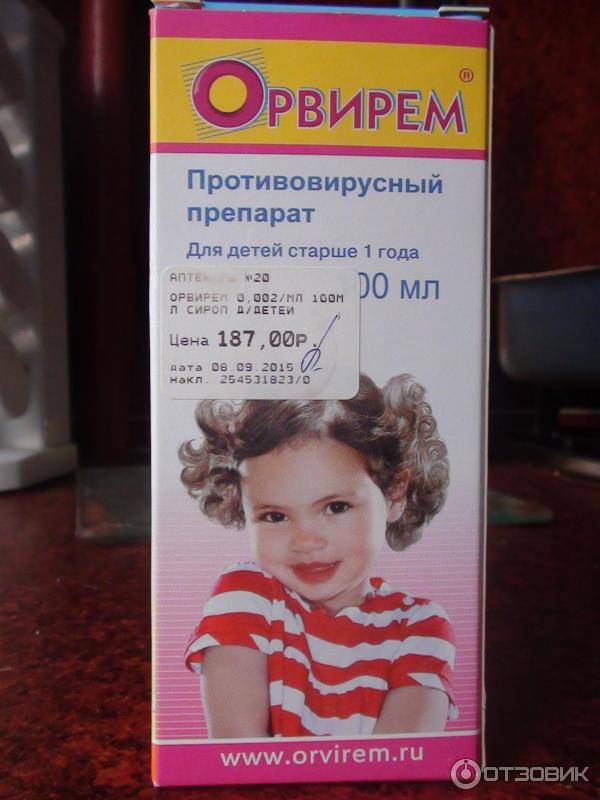 Как уже говорилось ранее, препарат отличается невысокой стоимостью, но помогает бороться с многими заболеваниями и патологиями, поэтому он до сих пор достаточно популярен.
Как уже говорилось ранее, препарат отличается невысокой стоимостью, но помогает бороться с многими заболеваниями и патологиями, поэтому он до сих пор достаточно популярен.
У лекарства есть ряд противопоказаний. В частности, препарат не подойдет пациентам, у которых наблюдается хотя бы незначительная непереносимость бендазола – активного вещества в лекарстве. Специалисты с осторожностью назначают его людям пожилого возраста, а также тем, которым приходится постоянно быть внимательными или сосредоточенными. Категорически лекарство противопоказано людям с артериальной гипотонией, язвами желудка или кишечника, особенно, если последние характеризуются кровотечениями. Болезни почек и мочевыводящих путей также будут препятствием по отношению к приему препарата – подобные заболевания могут сильно обостриться. Принимают таблетки по одной за два часа до или через два часа после еды.
Преимущества:
- Одно из самых дешевых профилактических средств на российском фармакологическом рынке;
- Расширенное положительное действие;
- Довольно хорошо переносится;
- Позволяет справиться с головной болью и повышенным артериальным давлением.

Недостатки:
- Достаточно много противопоказаний;
- Натуральных компонентов в составе нет.
Дибазол-убф таблетки
1. Амиксин
Позволяет активизировать внутренние ресурсы человеческого организма, усилить иммунитет и не допустить развития патологических процессов. В клинических условиях была доказана эффективность этого препарата в борьбе с вирусными, бактериальными и грибковыми заболеваниями. Медикамент является абсолютно безопасным. Как правило, лечащие врачи назначают это лекарство для профилактики острых респираторных инфекций, однако оно подходит и для борьбы с ними. В качестве ключевого действующего компонента здесь выступает тилорон. Это вещество низкомолекулярного типа, получают его исключительно в лабораторных условиях. Оно активно воздействует на иммунную систему человека, способствуя выработке необходимых для борьбы с заболеванием соединений. В качестве вспомогательных веществ здесь используются диоксид титана, полисорбат, гипромеллоза, макрогол и так далее.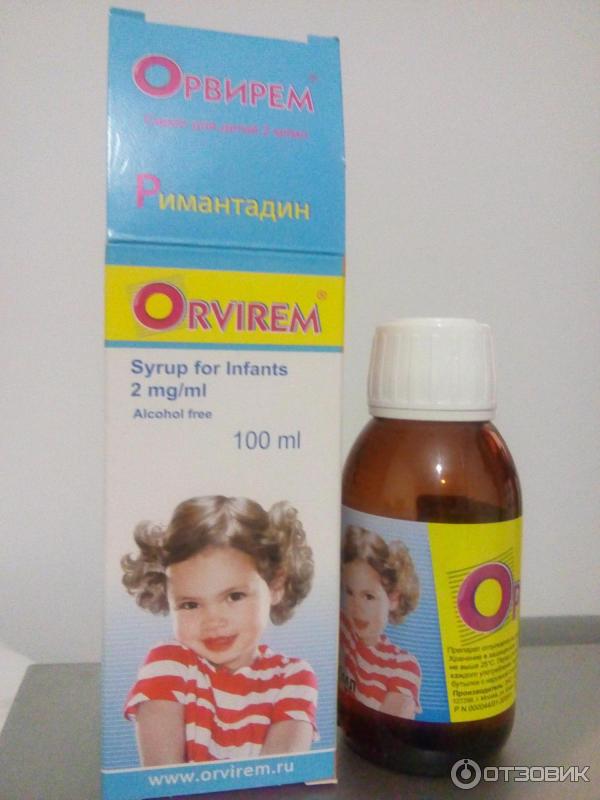 Все эти соединения позволяют стабилизировать лекарство, облегчить его всасывание. Выпускается препарат исключительно в виде таблеток. Он оказывает активное воздействие на ткани и органы. усваивается лекарство быстро.
Все эти соединения позволяют стабилизировать лекарство, облегчить его всасывание. Выпускается препарат исключительно в виде таблеток. Он оказывает активное воздействие на ткани и органы. усваивается лекарство быстро.
Оно относится к группе иммуномодуляторов и противовирусных препаратов. С его помощью удается быстро локализовать попавшую в организм инфекцию, не допустить последующего развития болезни. Всасывание происходит в пищеварительном тракте, все активные соединения с кровотоком распространяются по организму. Тилорон хорошо воздействует на клетки эпителия кишечника, стимулирует выработку лейкоцитов и гепатоцитов. Несмотря на то, что этот препарат не является антибиотиком, он хорошо борется с различными бактериальными и грибковыми заболеваниями, зачастую назначается людям, болеющим туберкулезом. Лекарство надежно защищает от воздействия рентгеновского излучения – при попадании в организм за несколько часов до проникновения лучей в ткани, оно в значительной степени улучшает радиопротекторные качества органов.
Преимущества:
- Хорошо борется с вирусными и инфекционными заболеваниями;
- Отличное профилактическое средство;
- Стимулирует работу иммунной системы;
- Минимальное количество противопоказаний.
Недостатки:
- Нередки аллергические реакции на этот препарат;
- Стоит дороже аналогичных лекарств.
Амиксин
Гомеопатическая продукция
4. Оциллококцинум
Хорошо справляется с болезнетворными вирусными инфекциями, в том числе с большинством форм гриппа. Выпускается в небольших запакованных колбочках, которые следует высыпать под язык за 15 минут до еды либо через час после принятия пищи. Держат под языком вплоть до полного растворения. Разрешается применять такой препарат вне зависимости от стадии болезни. Передозировка не случается практически никогда, а количество препарата нисколько не зависит от возраста пациента. На наиболее острой стадии болезни, когда наблюдается высокая температура, принимают лекарство дважды в день – по одной дозе утром и вечером. В такой дозировке можно пить средство максимум трое суток. Препарат наиболее эффективно действует в случае, если принимают его на начальной стадии болезни. Если инфекция еще не успела поразить весь организм, то разрешается сделать так: употребляют сначала одну дозу, потом еще две или три с промежутком в 6 часов.
В такой дозировке можно пить средство максимум трое суток. Препарат наиболее эффективно действует в случае, если принимают его на начальной стадии болезни. Если инфекция еще не успела поразить весь организм, то разрешается сделать так: употребляют сначала одну дозу, потом еще две или три с промежутком в 6 часов.
Может выступать в качестве профилактического средства в период эпидемий. В этом случае нужно будет пить по одной дозе в неделю – в это случае вероятность заболевания снижается в несколько раз. Разрешается давать препарат даже грудным детям – для этого гранулы растворяют в очищенной воде и дают малышу с ложечки или же наливают в бутылочку с соской. Противопоказаний практически нет за исключением индивидуальной непереносимости отдельных компонентов, что встречается очень редко. Согласно клиническим исследованиям, которые проводили независимые лаборатории разных стран, препарат представляет собой очень эффективное средство при борьбе с вирусными инфекциями и гриппом. Состояние больных становится лучше буквально через пару часов. В полной мере удается побороть инфекцию в течение двух-трех дней. Лекарство борется со всеми симптомами вирусов.
В полной мере удается побороть инфекцию в течение двух-трех дней. Лекарство борется со всеми симптомами вирусов.
Преимущества:
- Очень быстро справляется с инфекцией любого рода;
- Подавляет симптомы и причины заболевания;
- Противопоказаний практически нет;
- Можно давать даже грудным детям.
Недостатки:
- Высокая стоимость;
- При регулярном применении у организма возникает привыкание к препарату, из-за чего его эффективность сильно снижается.
Оциллококцинум
2. Гипорамин таблетки сублингв.
Первое в нашем обзоре лучших противовирусных препаратов исключительно натуральное средство, которое производится на основе растительных компонентов. В качестве основного действующего вещества используется высушенный и полностью очищенный экстракт листьев крушиновидной облепихи. В одной таблетки содержится 20 мг этого продукта. В экстракте облепихи содержится полифенольный комплекс галлоэллаготанинов, которые отличаются ярко выраженным противовирусным эффектом по отношению к штаммам гриппа, а также целому ряду других заболеваний, в том числе герпесу. Механизм действия препарата базируется на ингибирующем воздействии на РНК патологической среды. Иными словами, лекарство блокирует процессы размножения и деления клеток вируса. Кроме того, оно способствует выработке интерферона. Токсичность минимальная, средство не является причиной мутагенного, аллергенного, канцерогенного и тератогенного эффекта, не подавляет естественный иммунитет.
Механизм действия препарата базируется на ингибирующем воздействии на РНК патологической среды. Иными словами, лекарство блокирует процессы размножения и деления клеток вируса. Кроме того, оно способствует выработке интерферона. Токсичность минимальная, средство не является причиной мутагенного, аллергенного, канцерогенного и тератогенного эффекта, не подавляет естественный иммунитет.
Препарат подходит для взрослых и детей в возрасте от двух месяцев, выступает в качестве профилактического и терапевтического средства. Согласно проведенным клиническим исследованиям, это лекарство может назначаться даже беременным и кормящим женщинам, однако делается это с осторожностью и под наблюдением специалиста. Из противопоказаний здесь есть только возможная индивидуальная непереносимость отдельных компонентов препарата. Желательно принимать данное средство на ранних стадиях заболевания – таблетку держат под языком вплоть до полного рассасывания. Стоит отметить, что продукция хорошо помогает и при ветряной оспе – она облегчает общее состояние пациента, снижает зуд и убирает излишнее покраснение._sirop_d_detey_02_fl_100ml_rnd12024S.gif) Случаев передозировки во время тестирования обнаружено не было.
Случаев передозировки во время тестирования обнаружено не было.
Преимущества:
- Изготавливается на базе натуральных экстрактов;
- Приемлемая стоимость;
- Помогает не только при простуде или гриппе, но и при борьбе с рядом других заболеваний;
- Способствует выработке естественного иммунитета.
Недостатки:
- Врачи назначают далеко не всегда – непонятно почему.
Гипорамин таблетки сублингв.
1. Кагоцел
Лекарство представляет собой гомеопатическое средство, использующееся в борьбе с острыми респираторными вирусными инфекциями, зачастую оно применяется для понижения риска инфицирования. С его помощью удается улучшить работу иммунной системы организма. Его используют как в терапевтической, так и в педиатрической практике, так как он подходит для пациентов в возрасте от трех лет и старше. На патогенную микрофлору самостоятельно препарат не влияет, зато помогает организму бороться с инфекцией своими силами. Он безопасен, хорошо переносится даже ослабленным иммунитетом. В качестве основного активного средства здесь используется вещество кагоцел, которое в комплексе с кальциевой солью стеариновой кислоты, крахмалом, молочным сахаром и кросповидоном запускает работу иммунной системы. После применения быстро всасывается в кровь и распределяется по всему организму.
Он безопасен, хорошо переносится даже ослабленным иммунитетом. В качестве основного активного средства здесь используется вещество кагоцел, которое в комплексе с кальциевой солью стеариновой кислоты, крахмалом, молочным сахаром и кросповидоном запускает работу иммунной системы. После применения быстро всасывается в кровь и распределяется по всему организму.
Препарат помогает синтезировать интерферон, который хорошо борется с болезнью. При применении данного лекарства вырабатывается большее количество лимфоцитов, гранулоцитов, а также многих других клеток, отвечающих за формирование иммунитета. Даже однократное применение средства позволяет повысить содержание интерферона в крови на четыре-пять дней. Если соблюдать указанную в аннотации дозировку, то препарат не будет вредить тканям, не накапливается в организме. С осторожностью можно применять даже во время беременности, так как активные вещества не оказывают вредоносного воздействия на плод. Можно использовать в качестве профилактического средства. Лекарство безопасное, хорошо переносится организмом, непереносимость наблюдается чрезвычайно редко.
Лекарство безопасное, хорошо переносится организмом, непереносимость наблюдается чрезвычайно редко.
Преимущества:
- Довольно удобная форма выпуска – маленькие таблетки с легкостью проглатываются;
- Положительный эффект достигается быстро;
- Приемлемая стоимость;
- Продолжительное действие;
- Противопоказаний и побочных эффектов минимальное количество.
Недостатки:
- Для прохождения курса лечения нужно две неполных упаковки.
Кагоцел
Наиболее эффективные лекарства
4. Арбидол
Выпускается в виде небольших таблеток с пленочной оболочкой, препарат имеет белую или кремовую окраску. Является очень популярным лекарственным средством, предназначенным для профилактики и лечения простудных заболеваний дыхательных путей, помогает справиться с повышенной температурой, кашлем и прочими проявлениями вирусных инфекций. Действующий компонент не дает вирусам размножаться, избавляет от симптомов недуга, а также повышает возможности иммунитета человека. Вероятность возникновения побочных эффектов при приеме этого лекарства минимальная. Арбидол используется для симптоматического и этиологического лечения. В качестве главного действующего компонента используется умифеновир. Это искусственно синтезированное соединение обладает ярко выраженными противовирусными и иммуномодулирующими качествами.
Вероятность возникновения побочных эффектов при приеме этого лекарства минимальная. Арбидол используется для симптоматического и этиологического лечения. В качестве главного действующего компонента используется умифеновир. Это искусственно синтезированное соединение обладает ярко выраженными противовирусными и иммуномодулирующими качествами.
Здесь также есть стеарат кальция, повидон, крахмал, диоксид титана и несколько прочих стабилизирующих компонентов. Пленочная оболочка довольно плотная, поэтому растворяться и всасываться лекарство будет в требуемом отделе желудочно-кишечного тракта. Форма выпуска разная – порошок, капсулы и таблетки. Активное вещество средства помогает организму синтезировать повышенное количество интерферона, предусмотрен антиоксидантный эффект, не допускающий повреждения тканей под воздействием агрессивных форм кислорода. Из организма лекарство выводит токсины, не допуская их накапливания в почках и печени.
Преимущества:
- Небольшой размер таблеток облегчает проглатывание;
- Выпускается в нескольких формах;
- Эффективность препарата заметна в течение ближайшего часа;
- Продолжительность действия достигает 3-4 часов.

Недостатки:
- Высокая стоимость.
Арбидол
3. Ингавирин
Возможности этого препарата позволяют использовать его для профилактики или борьбы с инфекциями дыхательной системы, минимизируют вероятность инфицирования даже на самых ранних стадиях. Активно борется с самыми разными возбудителями болезней. При помощи средства удается быстро очистить организм пациента от патогенной микрофлоры, ускорить выздоровление, можно давать лекарство даже маленьким детям. Функцию активного вещества выполняет имидазолилэтанамид пентандиовой кислоты. Концентрация соединения находится в непосредственной зависимости от формы выпуска препарата. Здесь также содержится ряд дополнительных компонентов, которые стабилизируют формулу самого лекарства, а также помогают облегчить усвоение препарата в пищеварительном тракте.
Состав борется с грибковыми и вирусными инфекциями, в том числе с гриппом формата А или В. После прохождения курса лечения инфекционные агенты полностью выводятся из организма пациента, иммунная система начинает правильно и стабильно работать. При своевременном применении риск заражения снижается примерно на 70%. После всасывания средство быстро распространяется по кровотоку, моментально запуская внутриклеточные механизмы борьбы с болезнью. Кроме того, нарушается клеточный транспорт, что приводит к замедлению образования клеток патогенной микрофлоры. Выраженность воспалительного процесса также снижается, равно как и вероятность возникновения осложнений.
При своевременном применении риск заражения снижается примерно на 70%. После всасывания средство быстро распространяется по кровотоку, моментально запуская внутриклеточные механизмы борьбы с болезнью. Кроме того, нарушается клеточный транспорт, что приводит к замедлению образования клеток патогенной микрофлоры. Выраженность воспалительного процесса также снижается, равно как и вероятность возникновения осложнений.
Преимущества:
- Побочные эффекты практически отсутствуют;
- Лекарство не просто стимулирует работу иммунной системы, но и справляется с патогенной микрофлорой, в кратчайшее время выводя ее из организма;
- Удобная форма;
- Одна упаковка рассчитана на полноценный курс.
Недостатки:
- Довольно дорого стоит;
- Иногда вызывает аллергические реакции.
Ингавирин
2. Циклоферон
Достаточно эффективное лекарственное средство, которое может использоваться не только для лечения, но и для профилактики вирусных и простудных заболеваний. Препарат характеризуется активными противовирусными и иммуномодулирующими качествами. После курса иммунитет становится значительно выше, а риск формирования патологий вирусного или бактериального типа сводится практически к нулю. Для того, чтобы побороть инфекционный процесс, можно использовать лекарство в рамках комплексной терапии. Оно подходит для взрослых и детей в возрасте от 4 лет и старше. Побочные эффекты проявляются, но довольно редко. Это лекарство относится к новому классу препаратов, которые обладают способностью регулировать работу иммунных систем всего организма. Средство по безопасности и эффективности гораздо лучше нежели антибиотики – оно не причиняет организму ни малейшего вреда, выводится в течение нескольких дней, не накапливается в почках или печени.
Препарат характеризуется активными противовирусными и иммуномодулирующими качествами. После курса иммунитет становится значительно выше, а риск формирования патологий вирусного или бактериального типа сводится практически к нулю. Для того, чтобы побороть инфекционный процесс, можно использовать лекарство в рамках комплексной терапии. Оно подходит для взрослых и детей в возрасте от 4 лет и старше. Побочные эффекты проявляются, но довольно редко. Это лекарство относится к новому классу препаратов, которые обладают способностью регулировать работу иммунных систем всего организма. Средство по безопасности и эффективности гораздо лучше нежели антибиотики – оно не причиняет организму ни малейшего вреда, выводится в течение нескольких дней, не накапливается в почках или печени.
В качестве основного действующего средства здесь используется акридонуксусная кислота. Если лекарство выпускается в форме таблеток, то в нем в качестве дополнительных веществ будут содержаться полисорбат, полимер метакриловой кислоты, пропиленгликоль и стеарат кальция. Вырабатываемые под действием препарата интерфероны концентрируются в легких, селезенке, печени и некоторых других органах, не допуская развития бактерий. Лекарство не просто помогает организму вырабатывать вещества для борьбы с болезнью, но и само тоже угнетающе воздействует на микробы и вирусы, помогая справиться с ними в кратчайшие сроки.
Вырабатываемые под действием препарата интерфероны концентрируются в легких, селезенке, печени и некоторых других органах, не допуская развития бактерий. Лекарство не просто помогает организму вырабатывать вещества для борьбы с болезнью, но и само тоже угнетающе воздействует на микробы и вирусы, помогая справиться с ними в кратчайшие сроки.
Преимущества:
- Помогает выздороветь в течение всего лишь пары дней;
- Хорошее профилактическое средство;
- Не просто стимулирует иммунитет, но и само борется с заболеванием;
- Справляется с вирусными и бактериальными инфекциями.
Недостатки:
- Цена высоковата;
- Полностью искусственно синтезированное средство.
Циклоферон
1. Эргоферон
Разрабатывался специально для борьбы с гриппом и рядом других инфекционных заболеваний. Согласно аннотации, отличается противовирусными и иммуномодулирующими характеристиками. В составе есть специально подготовленные антитела, которые позволяют улучшить работу иммунитета, помочь организму справиться с патогенной микрофлорой любого типа. Как отмечают специалисты, курс терапии следует начинать за несколько дней до начала сезона простуд. Зачастую продукцию используют в рамках комплексной терапии. В качестве основного действующего средства здесь используется комплекс иммуноглобулинов. Подобные химические вещества помогают добиться превосходного терапевтического эффекта при борьбе с простудными заболеваниями. В качестве вспомогательных компонентов здесь выступает лактоза, вода, целлюлоза и стеарат магния.
Активные соединения попадают в кровоток и соединяются с интерфероном, за счет чего естественная защита организма становится значительно лучше. Препарат помогает бороться в том числе и с грибковыми инфекциями. Все вещества, имеющиеся в составе данного лекарства, помогают справиться с патологией и избавиться от негативных изменений в тканях. Побочных реакций и противопоказаний при приеме средства здесь практически не встречается. Вероятность возникновения осложнений зависит от индивидуальных особенностей человеческого организма.
Преимущества:
- Продукция отличается приятным вкусом;
- Можно использовать в терапевтических целях;
- Стимулируют работу иммунной системы и выработку интерферона;
- Быстро подавляют патогенную микрофлору.
Недостатки:
- Относительно дорого стоит.
Эргоферон
В заключении полезное видео
Вот и подошел к концу наш обзор лучших противовирусных препаратов самых разных ценовых категорий и принципов действия. Если вы уже пользовались какими-то аналогичными лекарствами, расскажите нам и другим читателям об этом – будет очень интересно узнать о вашем опыте борьбы с простудными заболеваниями.
ТОП!6 дешевых лекарств от простуды, которые заменят дорогие
Watch this video on YouTube
10 лучших противовирусных средств для детей в рейтинге 2020 года
Авторы рейтинга: Матвеева Виктория
Ценность противовирусных препаратов для детей заключается в их эффективности при лечении и профилактике. Каждое лекарство разработано с учётом безопасности для ребёнка. Рейтинг лучших средств 2020 года поможет разобраться в их разнообразии.
Когда нужно давать ребенку противовирусные средства
Вирусами называют микроорганизмы, состоящие из генетического материала и белковой оболочки. Но у них отсутствуют компоненты, отвечающие за обмен веществ (органеллы). Поэтому вирусы вне организма не размножаются. Им необходима человеческая клетка и её собственные органеллы. Внедрившись туда, они заставляют клетку работать на себя. В итоге та гибнет.
Организм имеет собственные механизмы и вещества, которые противостоят распространению вирусов. Кроме общеизвестных антител есть также макрофаги, лимфоциты, интерфероны и некоторые другие. Но часто организму необходима помощь в борьбе с вирусами, для чего и были разработаны противовирусные препараты.
Выделяют следующие типы таких средств:
- вакцины – позволяют организму отреагировать на вирус соответствующим иммунным ответом;
- интерферон и его индукторы – либо восполняют запасы интерферона (белка с противовирусными свойствами), либо стимулируют его выработку;
- этиотропные средства – блокируют активность вирусов.
Один из достоинств противовирусных препаратов – возможность лечить ими ребёнка до того, как температура достигнет 38°C. После этого уже можно начинать лечение медикаментами. Лекарства выпускают в разных формах – таблетки, сиропы, свечи и т.п.
Когда встаёт вопрос о непосредственном приёме препарата, лучше всего смотреть на самочувствие детей. Если ребёнок не стал вялым, не отказывается от еды, а температура невысокая – возможно, удастся обойтись без противовирусных.
Обязательно воспользуйтесь консультацией врача. Он выпишет самый подходящий и, главное, безопасный вариант. Самолечение при помощи даже самого простого средства может иметь непредвиденные последствия.
Существуют строгие правила относительно того, когда принимать интерфероносодержащие препараты.
- Естественные интерфероны вырабатываются в организме на 4-й день. Поэтому подобные препараты нужно давать ребёнку в первые 2-3 суток болезни.
- Интерфероносодержащие лекарства можно принимать максимум раз в полгода. В противном случае иммунная система слабеет, т.к. вместо неё с вирусами слишком часто борется лекарство.
По мнению некоторых специалистов, противовирусные подходят только для случаев, когда собственный иммунитет слишком слабый. Также некоторые средства (в первую очередь гомеопатические и растительные) можно использовать для профилактики.
Противовирусные препараты с рождения
Средства, которые помогут при болезнях даже самых маленьких. Полностью безопасны и могут применяться в возрасте до года.
1. Виферон свечи
Препарат выпускается в виде ректальных суппозиторий (свечей) пулевидной формы белого и желтоватого цвета. Цвет может быть неоднородным, с вкраплением или мраморными узорами. Один из главных плюсов средства – возможность приёма сразу после рождения. Подходит для женщин в период беременности и лактации. Виферон применяется при ОРВИ, гриппе (в том числе с осложнением), инфекционно-воспалительных заболеваниях разных видов, герпетической инфекции, хронических вирусных гепатитах. Препарат регулирует иммунную систему, усиливая её сопротивление болезни, и обладает противовирусным эффектом. В составе есть вещества, которые также снимают воспаление и имеют регенерирующие свойства.
Есть варианты средства в различных дозировках. При выборе нужно ориентироваться на заболевание, возраст ребёнка, особенности здоровья. Средство применяется ректально. Использование противовирусных свечей для детей поможет избежать побочных эффектов, которые возникают при парентеральном введение интерферона подобного рода.
Преимущества:
- эффективные;
- удобство применения;
- не вызывает рвоту;
- реже возникают заболевания;
- подходит для новорожденных.
Недостатки:
- возможна аллергия;
- возможны проблемы со стулом.
Отзывы покупателей
Наталия Т. Когда ребенок маленький, лечить можно оказывается не всем. У нас из-за сиропов ужасно болит животик, врач сказала, скорее всего реакция на подсластители, которые в составе. Выписала свечи Виферон от простуды. И как-то нам они очень хорошо сразу стали помогать и ничего не болело. Нашла хорошее лечение для ребенка, это важно дорогого стоит.
Надежда С.
Когда очередной раз ребенок заболел врач назначила с каплями в нос и спреем в горло свечи виферон. Я сначала отнеслась к ним с недоверием, но изучив состав купила их и теперь этот препарат всегда лежит у меня в холодильнике. Виферон быстро помогает дать ответ иммунитету на болезнь, соответственно выздоровление происходит намного быстрее, а сама простуда протекает легче. Моя подруга тоже всегда ставит их дочери, когда она болеет и считает их эффективными.
2. Оцилококцинум
Гомеопатическое средство с достаточно быстрым эффектом. Действующее вещество – экстракт печени и сердца утки барбарийской. Также в качестве вспомогательных компонентов используется сахароза и лактоза. Поэтому препарат не подойдёт при непереносимости лактозы и дефиците лактазы. Оцилококцинум применяется при гриппе средней и лёгкой степени тяжести, а также ОРВИ. Уменьшает симптомы заболеваний в течение 24 часов. В данном случае частота приёма зависит не от возраста, а от стадии заболевания. Также средство подходит для профилактики болезней. При его применении в слюне и на слизистых оболочках повышается уровень секреторного иммуноглобулина, что уменьшает риск проникновения вирусов в организм.
Препарат необходимо принимать внутрь, за 15 минут до еды или через час после. Содержимое тубы кладут под язык и рассасывают. Средство удобно тем, что его можно легко растворить в воде, чтобы затем дать ребёнку с ложечки или через бутылочку.
Преимущества:
- приятный вкус;
- быстрый результат при первых признаках болезни;
- подходит для профилактики;
- удобная упаковка.
Недостатки:
- высокая цена;
- слабый эффект, если стадия заболевания не начальная.
Отзывы покупателей
Татьяна Д. Очень хочется оставить отзыв о единственном препарате, который я могу себе позволить давать детям. Почему только его? Потому что другие либо в сиропах, либо в свечках. Сиропы слишком сладкие, а свечи малоэффективные. А здесь маленькие, очень вкусные и не слишком приторно-сладкие гранулы. Совсем маленьким деткам можно растворить в воде. Пила его во время беременности и какое-то время после родов.
Елена Д. «Оциллококцинум» считаю препаратом первой помощи при начинающейся простуде. Применяла его многократно сама, принимал супруг, советую его своим знакомым. Мне он прекрасно помогает справиться с заболеванием, мне нравится способ применения. А главное, что препарат гомеопатический, значит — не только эффективный, но и безопасный.
3. Афлубин капли
Ещё один гомеопатический препарат, который может применяться и для лечения, и для профилактики. Помогает при гриппе, ОРВИ, парагриппозных заболеваниях. Афлубин может сократить срок выздоровления вдвое. При профилактике значительно сокращает риск заболеваний. По инструкции, детям его можно давать с 12 месяцев. Однако многие педиатры выписывают его малышам до года, так как его состав практически безопасен. Эффект достигается за счёт целого комплекса активных веществ, в том числе трав. Среди них горечавка, аконит, бриония. Однако такой состав повышается риск возникновения аллергии на компоненты.
Средство снимает воспаления, регулирует иммунную систему, обладает жаропонижающим и дезинтоксикационным эффектом. Его можно использовать для экстренной профилактики ОРВИ или гриппа в случае, если был контакт с больным или после длительного переохлаждения. Капли нужно принимать внутрь за полчаса до еды или через час после. При этом их необходимо держат около полуминуты во рту. Можно использовать в чистом виде или разведённом.
Преимущества:
- не вредит иммунитету;
- подходит для профилактики;
- безопасный состав;
- эффективен при ОРВИ и гриппе;
- улучшение самочувствия.
Недостатки:
- возможна аллергия;
- спирт в составе;
- специфический вкус.
Отзывы покупателей
Helene Pavlova Афлубин знаю уже много лет. в этом году ребенок пошел в сад и стал болеть часто, ну и я с ним за компанию. Стала принимать Афлубин для профилактики и ребенку даю. Болеем гораздо реже, а если ребенок все же заболел, то я уже не заражаюсь. Радует безопасный состав и что нет побочки.
Имя скрыто Если вы побывали в больнице в большом торговом центре не важно,но если прорезается насморк,ослабление и.т.д «Афлубин» поможет,но если уже сильный кашель, температура НЕ НАДЕЙТЕСЬ на чудо! Афлубин предотвращает болезнь ,но ни как не вылечивает! (Средство хорошее !!!) рекомендую
Противовирусные средства детям 1-3 лет
Рейтинг продолжают препараты для более старшего возраста. Новорожденным они не подойдут, но хорошо справляются с заболеваниями у детей 1-3 лет.
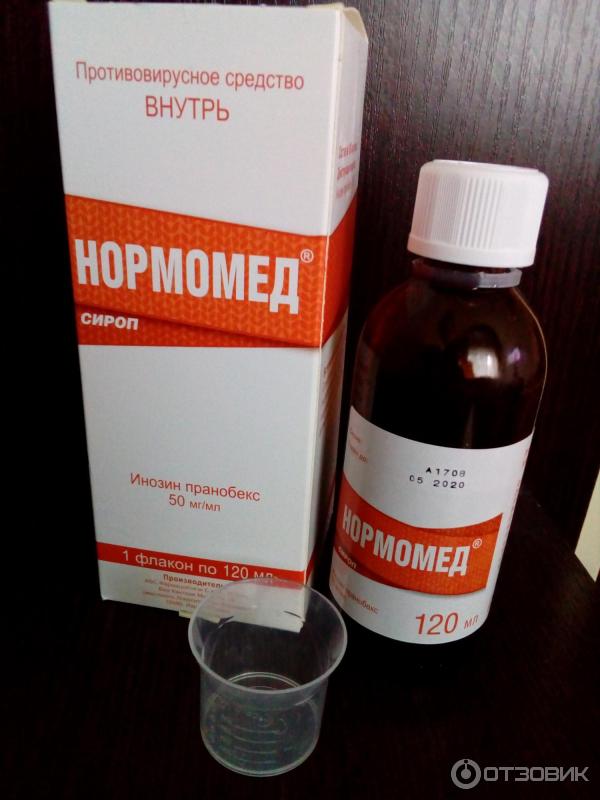
1. Цитовир-3 сироп
Лучшее противовирусное средство для детей от 1 года. Выпускается в виде сиропа белого или желтоватого цвета. Комплексно воздействует на организм, обладает иммуностимулирующим эффектом. При применении значительно повышает сопротивляемость организма к любым респираторным заболеваниям. Цитовир-3 воздействует на слизистую дыхательных путей, через которую чаще всего проникают вирусы, усиливает барьерную функцию. Если пациент уже заболел, препарат обеспечивает быстрое выздоровление или помогает перенести болезнь в лёгкой форме. Также снижается риск развития осложнений. Сироп также повышает выработку интерферонов, уничтожает клетки, мутировавшие под воздействием вирусов, и способствует выведению последних.
Сироп нужно принимать за полчаса до еды. Доза для детей 1-3 лет — 2 мл. 3 раза в сутки. Также Цитовир-3 подходит для профилактических курсов при контакте с больными. Курс длится 4 дня, через 3 недели можно повторить, пока не улучшится эпидемическая обстановка.
Преимущества:
- эффективный;
- подходит для профилактики;
- доступная цена;
- помогает при первых симптомах.
Недостатки:
- возможна аллергия.
Отзывы покупателей
Марина А. Как профилактическое средство использую несколько лет для детей, можно применять от 1 года. Старшему 6 лет, ему даже нравится. Курс повторяю в середине осени, в декабре и марте. Считаю, что лучше потратиться на профилактику, чем потом ребенок будет болеть. Да, и на лечение и потратить придется еще больше. Как лечение не использовала, не было необходимости. Максимум небольшая сопливость.
София А. Давать его нужно было 3 раза в день, за полчаса до еды. В принципе, мне не сложно было подстроить график ребенка, чтобы так давать. Принимать сироп Цитовир-3 нужно было всего 4 дня, вне зависимости от того лечение это или профилактика. Ребенок переносил препарат очень хорошо, никаких побочек не было. Вкус сладкий, приятный. Заметила что после него стали болеть намного меньше, хотя придерживаемся того же ритма жизни что и раньше.
2. Орвирем
Эффект этого средства основывается на ингибировании (замедлении) репродукции вируса после его попадания в клетку. В отличие от предыдущих препаратов, при приёме Орвирема может наблюдаться достаточно обширный список побочных явлений. Они касаются пищеварительной и центральной нервной систем. Также не исключена аллергическая реакция. При употреблении важно обратить внимание на ряд противопоказаний.
Орвирем помогает не только при гриппе, но также и в случае клещевого энцефалита, что особенно важно в летнее время, особенно если планируются частые выезды на природу. Главное действующее вещество –римантадин. В случае заболевания гриппом B оказывает антитоксический эффект. Средство будет полезно в профилактических целях, если был контакт с заражённым. Также снизит риск заболевания при распространении инфекции в замкнутой группе или при неблагоприятной эпидемической обстановке. Принимать сироп необходимо после еды. Каждый последующий день доза отличается.
Преимущества:
- эффективный;
- низкая цена;
- приятный вкус;
- снимает температуру;
- эффективен при профилактике.
Недостатки:
- возможны побочные реакции, аллергия.
Отзывы покупателей
Helene Pavlova Брала ребенку от ОРВИ. Обычно болеем недели 2, а тут поправились за 5 дней. Давала по схеме, а вот это неудобно, тк ребенка каждый раз нужно уговаривать открыть рот. В целом я довольна, читала, можно давать для профилактики в сезон простуд. Буду пробовать.
Rustam Agaev Прием по схеме — разобрался быстро. Сироп не противный, ребенок пил на ура. Обычно воротит нос от сиропов, а этот понравился. Вылечили быстро ОРВи и в сад)
3. Ликопид
Препарат в виде таблеток, обладающий достаточно широким воздействием на организм. Ликопид усиливает защитные функции организма, а в случае заболевания значительно сокращает срок его течения. Помогает против простудных заболеваний, вирусов, хронических инфекций, грибков. Показан при гнойно-воспалительных процессах на коже и мягких тканях, герписе. Главный плюс лекарства заключается в том, что его воздействие максимально близко к естественному процессу регуляции иммунитета. Также препарат будет полезен при профилактике заболеваний, в том числе хронических.
Средство принимается внутрь или путём рассасывания под языком. Если приём был пропущен, всё равно есть возможность употребить нужную дозу, если от запланированного времени не прошло 12 часов. Побочные явления включают в себя аллергию, кратковременное повышение температуры, диарею. Противовирусные таблетки для детей не токсичны, также не требуют специального хранения в прохладных местах.
Преимущества:
- быстрый эффект даже при ярко выраженных симпатомах;
- удобен в применении;
- нейтральный вкус;
- поддержка иммунитета;
- хорошо переносится.
Недостатки:
- возможна аллергия.
Отзывы покупателей
Вика К. От меня только положительные эмоции. После лечения несколькими курсами Ликопид 1 мг, мой ребенок перестал болеть. До этого было невыносимо ходить в садик. Три недели болеем, одну ходим, и так на протяжении полу года. А таблетки все-таки помогли побороть эту черную полосу. Наступила белая, здоровая и активная.
Вероника Н. Проявил себя очень хорошо. Два курса пропил ребенок и пока больше не болел. Достаточно внушительный срок прошел, пол года будет в ноябре. До этого сын постоянно простужался, сопли вообще не проходили, постоянно пузырями, а тут такой перерыв между болезнями, мечта.
Противовирусные препараты для детей старше 3-х лет
Эти препараты уже более эффективные. Ведь зачастую они должны помогать бороться с вирусом, когда ребёнок уже ходит в садик или школу.
1. Циклоферон
Достаточно известный препарат, который комплексно воздействует на организм и обладает широким спектром активности. Меглюмина акридонацетат, активное вещество, является индуктором интерферона, а потому эффективен в борьбе с вирусами, также регулирует работу иммунной системы и снимает воспаление. Циклоферон помогает в случае респираторных заболеваний различного рода, в т.ч. гриппа и герпеса. Он подавляет размножение вирусов в начале болезни, в первые 1-5 суток. Средство хорошо подходит для профилактики заболеваний у детей.
Циклоферон нужно употреблять раз в сутки за полчаса до еды, при этом его не разжёвывают, а сразу запивают водой. Детям 4-6 лет необходимо выпивать одну таблетку, 7-11 лет – 2-3 таблетки, для более старших доза возрастает до 3-4. Препарат хорошо переносится, побочные явления и аллергия возникают очень редко. К тому же, он совместим с другими лекарствами, которые применяются при подобных заболеваниях.
Преимущества:
- эффективный;
- хорошо помогает при первых симптомах;
- быстрый результат;
- усиливает иммунитет;
- подходит для комплексного лечения с другими препаратами.
Недостатки:
- высокая цена;
- влияние на пищеварительную систему.
Отзывы покупателей
Мари У нас был вирусный стоматит, помог только циклоферон. Назначали тоже виферон и полоскать, нифига не помогало. Перестала полоскать и дала циклоферон-температура почти сразу спала.
Настя Я при гриппе и орви принимаю циклоферон, он как раз помогает организму с вирусами справиться, с ним быстрее в норму прихожу, не выпадаю из жизни на неделю. Упаковка стоит недорого, неделю назад в нашей аптеке за 361 рубль брала пачку 20 таблеток. Детям своим его кстати тоже даю и для лечения, и для экстренной профилактики от гриппа, его с четырех лет принимать можно.
2. Полиоксидоний
Средство выпускается в виде суппозиторий для ректального и интравагинального введения. Раз в сутки можно применять 1 суппозиторию. Допускается применение каждый день, раз в два дня или 2 раза в неделю. Средство имеет торпедообразную форму, окрашено в светло-жёлтый цвет. Должно быть неоднородным. Обладает характерным запахом какао-масла. Активное вещество, азоксимера бромид, оказывает комплексное воздействие на организм, регулирует иммунитет, обладает детоксицирующим и антиоксидантным воздействием, поддерживает защитные силы организма и снимает воспаление.
Полиоксидоний применяется для комплексной терапии в случае инфекционно-воспалительных болезней в период ремиссии и обострения. Подходит для детей от 6 лет, но иногда назначается врачами и в более раннем возрасте. Помогает при туберкулёзе, аллергических заболеваниях, при проведении химио- и лучевой терапии. Также активирует процессы регенерации, а значит, будет полезен при переломах и ожогах.
Преимущества:
- нет дискомфорта;
- быстрый эффект;
- снижается риск заболеваний;
- хорошо подходят для детей;
- помогает при аллергии.
Недостатки:
- высокая цена;
- быстро тают.
Отзывы покупателей
Мини М. Как выяснилось, ставить свечи на ночь совсем не смертельно) Они без запаха практически, свечи как свечи, ничего особенного или необычного. Я на результат больше смотрела. Вот как мы их полностью проставили, стала отслеживать состояние своего чада. Больше месяца прошло, полет нормальный. Хотя и в дождь попадали и из бассейна на даче не вылезаем. Было где переохладиться.
Светлана В. У дочери частые простуды и бронхиальная астма, от цветения нам совсем плохо весной, приступы очень часто. У нас во дворе сплошные тополь да береза, ребенок задыхается постоянно. Мы у врача наблюдаемся, полиоксидоний нам сравнительно недавно добавили к бронхолитикам. Полиоксидоний в свечах, так меньше всего что отреагирует, но вообще как врач говорит, этот препарат почти не аллергенный. Ребенок очень хорошо свечи перенесла, приступы у нас реже стали.
3. Изопринозин
Средство выпускается в форме таблеток продолговатой формы. Принимать необходимо после еды, после запить водой. Изопринозин хорошо всасывается из ЖКТ, а после практически сразу подвергается метаболизму. Для детей суточная доза составляет 50 мг. на кг массы тела. Это количество разделяется на 3-4 приёма.
Средство будет полезно при многих заболеваниях. В список входят грипп, ОРВИ, герпес, лишай, ветряная оспа и некоторые другие. Средство достаточно негативно влияет на ЖКТ, также может вызывать аллергические реакции, боль в суставах. Побочные явления могут затрагивать нервную систему, мочеполовую систему. Основной эффект лекарства основывается на регулировании работы иммунной системы. Также оказывается противовирусное действие. Изопринозин относится к средствам достаточно широкого спектра действия. Например, он восстанавливает функции лимфоцитов в случае, когда иммунная система угнетена по какой-либо причине.
Преимущества:
- эффективный;
- снижает риск заболевания;
- укрепляет иммунитет;
- широкий спектр действия;
- хорошо всасывается.
Недостатки:
- высокая цена;
- возможны побочные явления и аллергия.
Отзывы покупателей
Елена Кривенко Классные таблетки, нам посоветовала знакомая врач, только ими и смогли вылечить мононуклеоз, до них ничего не помогало, 2 месяца мучились, их еще можно использовать при гриппе и как профилактику ОРЗ, у меня двое маленьких детей, раньше когда один заболевает и второй сразу паровозиком, теперь один за болел, начинаю поить обоих, и прокатывает… И первый более 1-2 дня и второй не заболевает…
Анна И. Где-то год назад дочку обсыпало бородавками ни с того, ни с сего. Видимо подцепила какой-то вирус. Причем они вылезли в самых видных местах — на руках и на лице, что для девочки вообще кошмар. Мы их и прижигали, и замораживали — всё бесполезно. В итоге, на мое счастье, попали к хорошему врачу, которая выписала именно «Изопринозин». Пропили курс этих таблеток, и бородавки стали исчезать одна за другой. Я даже не ожидала такого результата.
4. Реаферон-Липинт
Достаточно эффективный биотехнологический препарат. Подходит как для лечения, так и для профилактики. В первом случае применяется трёхдневный курс, в течение которого необходимо принимать дозу по 500 000 МЕ 2 раза в день за полчаса до еды. При профилактике достаточно принимать такую же дозу 1 раз в день дважды в неделю. Курс длится уже месяц. Действующее вещество препарата — интерферон альфа-2b. Поэтому Реаферон-Липинт оказывает противовирусный эффект. Регулирует работу иммунной системы.
Лекарство значительно улучшает состояние при болезни, облегчает симптомы. Выздоровление наступает быстрее. Также снижается риск развития осложнений. Препарат хорошо усваивается и длительное время циркулирует в крови. Одной упаковки хватает надолго, к тому же, нужная доза легко рассчитывается. Средство разработано таким образом, чтобы не вызывать аллергию. Хорошо совмещается с другими препаратами.
Преимущества:
- эффективный;
- снижает частоту возникновения заболеваний;
- хорошо регулирует иммунную систему;
- подходит для комплексного лечения.
Недостатки:
Отзывы покупателей
Ольга Т. Решила давать ребёнку Реаферон липинт, результат есть: насморк стал уходить, температура упала, ну и сама повеселела. Доча курс пропила и уже пару месяцев мы не болеем. Был момент когда вдруг появились сопли и чихи, но доза реаферона и на след утро ничего нет! Вот так, хотите верьте, а хотите проверьте!
Ирина П. Реаферон — Липинт — эффективный препарат. Моему сыну назначает детский врач при ОРВИ. Значительно облегчает протекание болезни и сокращает период заболевания. Когда высокая температура, препарат является отличным жаропонижающим, сразу чувствуется облегчение. Важно, пропит весь курс, не забрасывать. Так же используем и в качестве профилактики.
Противовирусные препараты для детей от 3 лет: инструкция по применению, лечение и профилактика :: Статьи
В особой группе риска находятся те, кто посещают детский сад и начальную школу. Дети этого возраста болеют около 6-8 раз в год, причем продолжительность заболевания в среднем составляет около 7-10 дней 4. Дети, которых педиатры относят к категории часто болеющих, переносят ещё большее число острых респираторных заболеваний.
Вот почему так важно в преддверии сезона высокой вирусной активности быть готовыми к всплеску заболеваний и знать, какие противовирусные препараты эффективно могут помочь ребёнку.
Что такое противовирусные препараты?
Противовирусные препараты — это группа лекарственных средств на основе веществ, обладающих особой избирательной активностью, направленной либо на ингибицию возбудителя болезни 5, либо на стимулирование иммунной системы организма.
Существует множество противовирусных препаратов. По механизму действия среди них выделяют 6:
-
препараты прямого действия, или специфические химиопрепараты: воздействуют непосредственно на сам вирус, подавляя возможность размножаться в клетках организма, либо препятствуя проникновению вируса в клетку или высвобождению из нее;
-
препараты опосредованного действия: стимулируют собственный клеточный иммунный ответ организма, повышая сопротивляемость вирусным агентам (интерфероны, индукторы интерферонов, иммуноглобулины).
Вирусы многообразны, подвержены разного рода мутациям, что формирует их устойчивость к лекарственным препаратам 7. Это осложняет поиск противовирусных средств прямого действия. На сегодняшний день всего для нескольких возбудителей вирусных инфекций разработаны противовирусные препараты. Это вирусы герпеса, гепатита В и С, папилломы человека, аденовируса, лихорадки Ласса, вируса иммунодефицита человека и некоторых других 8. А из респираторных вирусных инфекций прямые противовирусные препараты существуют только для вирусов гриппа. Поэтому в лечении респираторных вирусных инфекций большое распространение получили интерфероны и их индукторы.
К группе индукторов интерферона относится и Кагоцел. Он стимулирует активность образования интерферонов практически во всех клетках, участвующих в формировании иммунного ответа организма на проникновение инфекции 9. Действие интерферона направлено на обнаружение и уничтожение генетической информации вируса, который пытается реплицироваться (размножаться) в клетках организма, пораженного ОРВИ 10.
Уже после приёма внутрь одной дозы Кагоцела количество интерферона в крови достигает максимальных значений всего в течение 48 часов. После этого интерфероны циркулируют в крови ещё на протяжении 4-5 суток 11.
Противовирусные препараты для детей от 3 лет
В силу различных особенностей организма ребёнка, в том числе незрелости систем органов, несовершенства иммунной системы и других физиологических факторов, к лекарственным средствам, которые применяются для лечения детей младшего возраста, предъявляются особые требования 12. Например, у детей до 3-4 лет активность ферментов печени снижена, а значит многие лекарственные препараты медленно разрушаются и долго циркулируют в организме 13.
Индукторы интерферона в отличие от препаратов на основе синтезированных интерферонов обладают рядом преимуществ. Они слабоаллергенны и стимулируют выработку интерферонов в физиологических дозах 14 — то есть в таком количестве, которое воспринимается организмом как естественное. А также практически не вызывают побочных эффектов 15.
Кагоцел относится к наиболее изученным противовирусным препаратам этой группы. Он обладает выраженным терапевтическим эффектом и рекомендован как для лечения, так и для профилактики. А главное, его эффективность в отношении различных возбудителей вирусной инфекции доказана в ходе клинических и наблюдательных исследований 16.
Специальные научные исследования с участием детей разного возраста проводились на клинических базах НИИ вирусологии им. Д.И. Ивановского РАМН, ГОУ ВПО РГМУ Росздрава, ГНЦ «Институт иммунологии ФМБА», ФГУ «Московский НИИ педиатрии и детской хирургии Росмедтехнологий». В результате были получены данные о безопасности Кагоцела, его хорошей переносимости и отсутствии побочных реакций для детей старше 2 лет 17.
В соответствии с российским законодательством применение лекарственной формы «таблетка» разрешено только для детей старше 3 лет 18. Поэтому и Кагоцел, который выпускается в таблетированной форме, рекомендован к применению в возрасте от трех лет.
Противовирусные препараты для детей от 5 лет
У детей старше 5 лет по мере взросления происходит постепенное созревание организма и внутренних органов. Но число факторов, которые влияют на выбор лекарственных средств при ОРВИ, всё ещё очень велико. Следует помнить, что правильно назначить их может только педиатр.
Например, если ребёнок часто болеет и имеет сопутствующую аллергопатологию (например, атопический дерматит), специалисты рекомендуют применять для лечения ОРВИ индукторы интерферона, которые почти не вызывают аллергии 19. Кагоцел относится к препаратам именно этой группы и рекомендован к применению детям старше 3 лет 20.
Противовирусные препараты от простуды и гриппа для детей
Приём противовирусных препаратов в период эпидемиологического подъема заболеваемости желателен не зависимо от этиологии респираторно-вирусного заболевания, т.е. не зависимо от вида возбудителя, каким оно было вызвано 21. Ведь часто спрогнозировать тяжесть течения болезни и развитие осложнений у детей достаточно затруднительно 22.
Приём противовирусных препаратов может привести к сокращению выраженности (ослаблению) и продолжительности симптомов заболевания, к ускорению выздоровления 23, а также может предупредить развитие более серьёзных осложнений, например, таких, как отит, бронхит или пневмония.
Очень важно, чтобы противовирусные препараты принимали дети, у которых вероятность развития осложнений достаточно высока. В первую очередь это касается пациентов в возрасте до 5 лет, часто болеющих детей (более 5-6 раз в год) и детей любого возраста с хроническими заболеваниями.
Во время клинических испытаний было доказано, что Кагоцел 24 снижает продолжительность:
При этом приём препарата приводит к сокращению длительности курса лечения антибиотиками при развитии бактериальных осложнений ОРВИ у детей 25.
Противовирусные препараты детям при первых признаках простуды или гриппа
Из-за того, что прогнозировать развитие простуды и гриппа у маленьких пациентов сложно, вне зависимости от тяжести первоначального состояния в эпидемиологический сезон часто болеющим детям или детям с хроническими заболеваниями рекомендуется начать приём противовирусных препаратов при ОРВИ как можно раньше 26.
Применение этих лекарств в течение двух дней после появления первых симптомов значительно облегчает течение болезни и снижает частоту развития бактериальных осложнений, например, острого отита, и частоту назначений системных антибиотиков в дальнейшем 27.
Тем не менее, если в первые дни после появления симптомов противовирусное лечение начать не удалось, отказываться от него не стоит. Препараты группы индукторов интерферона могут помочь в любом случае. В первую очередь это касается Кагоцела, ведь он эффективен и при позднем старте противовирусной терапии.
Противовирусные препараты детям для профилактики гриппа и простуды
Вирус гриппа вызывает острое респираторное заболевание у людей любого возраста. Однако существуют группы риска, для которых эта инфекция особенно опасна тяжёлым течением болезни и осложнениями. По данным ВОЗ, к данной группе, в том числе, относятся дети в возрасте до 59 месяцев (то есть до 4 лет и 9 месяцев) 28. Российские специалисты относят к группам риска детей с 6 месяцев, учащихся 1-11 классов, а также обучающихся в профессиональных образовательных организациях 29.
В качестве основного средства профилактики гриппа для детей в возрасте от 6 месяцев до 5 лет ВОЗ рекомендует специальную ежегодную вакцинацию 30. Также возможным средством профилактики, по мнению специалистов ВОЗ, могут выступать противовирусные препараты 31.
С особой тщательностью и ответственностью к профилактическим мерам необходимо отнестись, если ребенок посещает сад или школу, а также в период высокой активности вируса гриппа (в эпидемиологический сезон) 32. В российских регионах с умеренным климатом он продолжается с ноября по май 33.
Для профилактики ОРВИ противовирусные препараты рекомендуется давать ребенку как до контакта с носителем вируса, так и после него (в качестве экстренной профилактики), даже если заболевание ещё не вступило в активную фазу 34. Кроме того, необходимо помнить об экстренной профилактике членов семьи в случае, если кто-то заболел, и прерывании цепи передачи инфекции другим людям, в том числе одноклассникам, одногруппникам, коллегам. В первую очередь это касается семей, в которых есть несколько детей. Для этих целей, благодаря универсальности, особенно подходит Кагоцел. Он рекомендован к применению как детям в возрасте старше 3-х лет, так и взрослыми.
Детям старше 3 лет для профилактики гриппа и других ОРВИ рекомендуется принимать по 1 таблетке препарата Кагоцел 1 раз в день на протяжении 2 дней. Затем необходимо сделать пятидневный перерыв и повторить цикл 35.
Кагоцел для детей: терапевтическая схема приёма (для лечения ОРВИ и гриппа):
Для лечения ОРВИ или гриппа у детей препарат Кагоцел применяется по схемам: 36- по 1 таблетке 2 раза в день на протяжении 2 дней;
- в последующие 2 дня по 1 таблетке 1 раз в день.
- по 1 таблетке 3 раза в день на протяжении 2 дней;
- в последующие 2 дня по 1 таблетке 1 раз в день
Дети в возрасте от 3 до 6 лет:
Дети старше 6 лет:
Общая длительность курса лечения для детей обеих возрастных групп составляет 4 дня.
Детские лекарства от простуды и гриппа
Простуда представляет собой ничто иное как острую респираторную вирусную инфекцию (ОРВИ). ОРВИ – это острое заболевание, которое сопровождается болью в горле, насморком, кашлем, слабостью, вялостью, лихорадкой.
ОРВИ и иммунитетПо данным всемирной организации здравоохранения, ОРВИ занимают первое место в структуре заболеваемости детей раннего возраста. Вирусов, которые вызывают ОРВИ, существует большое количество. К ним относятся: вирусы гриппа, парагрипп, респираторно-синцитиальные вирусы, аденовирус, вирусы ECHO, Коксаки, риновирусы, реовирусы, коронавирусы. Высокий уровень заболеваемостью ОРВИ связан с нестойким иммунитетом у детей после перенесенной ранее ОРВИ, а также высокой распространенностью указанных вирусов. В условиях неблагоприятной экологии ОРВИ предопределяют еще большие изменения в иммунитете, особенно у детей раннего возраста. Это может приводить к значительным изменениям в формировании иммунитета у малыша, а также способствовать развитию хронических заболеваний различных систем детского организма в более старшем возрасте. Учитывая высокую распространенность ОРВИ, остается актуальным вопрос лечения детей с данной патологией. Мы подойдем к лечению простуды с точки зрения современных протоколов по лечению ОРВИ у детей, которые были разработаны союзом педиатров России. Прежде, чем перейти к рассмотрению детских лекарств от простуды и гриппа, необходимо разобраться в основных проявлениях ОРВИ у детей.
Важно следить за состоянием ребенка и обратиться к педиатру при первых симптомах простуды.
Симптомы ОРВИ у детейРебенок или родители ребенка могут обратить внимание на появление таких признаков, как:
- Острое начало заболевания, сопровождающееся подъемом температуры тела. Обычно температура тела колеблется в пределах 37,5-38,0 градусов. Обычно температурная реакция исчезает через 2-3 дня. Более длительное повышение температуры может указывать на грипп или аденовирусную инфекцию. Родители должны помнить, что нарастание температуры с течением времени, усиление интоксикации у малыша (слабости, вялости, недомогания) может указывать на присоединение бактериальной инфекции. Повторное повышение температуры у малютки после ее купирования может указывать на развитие острого среднего отита на фоне продолжительного насморка.
- Заложенность носа, выделения из носа.
- Жжение, боль, покалывание, сухость в горле. Нередко скопление слизи, стекая по задней стенки глотки, может приводить к появлению кашля.
- Шум и боль в ушах, снижение слуха, пощелкивание. Указанные симптомы развиваются при распространении воспаления на слуховые трубы.
- У грудных детей появляется беспокойство, трудности при кормлении и засыпании.
- Может появиться осиплость голоса.
- Покраснение глаз.
Признаки ОРВИ сохраняются в течении 5-7 дней, в некоторых случаях достигая 10-14 дней.
Лекарства от простуды для детейНе стесняйтесь задавать вопросы вашему педиатру или любому другому врачу.
На приеме у педиатра родители малыша часто задают такие вопросы: «При простуде какие лекарства принимать ребенку? Какое лучшее средство от простуды у детей?». Простуда является наиболее частой причиной использования различных медикаментозных средств, которые чаще всего вовсе не нужны. Большинство данных препаратов не обладают доказательной базой, то есть их эффект достоверно не доказан. Более того, многие из них обладают также и побочными эффектами. Очень важно понимать, что данное заболевание протекает доброкачественно и требует от себя лишь минимальных вмешательств. Имеется ввиду малое количество используемых лекарственных средств. Ниже рассмотрим основные лекарства от гриппа и простуды у детей:
- Антивирусные препараты от простуды детям. Являются препаратами, влияющими на причину заболевания. Противовирусное лечение применяется только при гриппе А и В, и только в первые два дня болезни. Используются ингибиторы нейраминидазы: осельтамивир, занамивир. Пациентам с бронхиальной астмой при лечении занамивиром очень важно иметь под рукой бронхорасширяющие препараты. На другие вирусы указанные препараты не действуют. То есть они являются основными препаратами от гриппа для детей. Доказательная база противовирусной эффективности других лекарственных средств у детей остается крайне ограниченной.
- Иммунотропные препараты. Указанная группа препаратов не обладает выраженным действием, их назначение нецелесообразно. Возможно использование не позднее первых двух дней интерферона альфа, однако и его эффект достоверно не доказан. Для понимания, интерферон – это белок, который выделяется клетками организма при проникновении вируса. Он помогает бороться с ним. Существуют также интерфероногены. Интерфероногены – это вещества, которые способны вызывать образование интерферонов. Согласно протоколу лечения, данная группа препаратов у детей старше 7 лет не оказывает выраженного эффекта. Единственное, на что способны они, это уменьшение длительности лихорадочного периода (периода повышения температуры) на один день. К препаратам данной группы относят: тилорон, неовир, циклоферон, полудан, кагоцел и др.
- Антибиотики. Использовать антибактериальные препараты при неосложненной ОРВИ не рекомендуется. Более того, использование антибиотиков в данном случае может способствовать присоединению бактерии. Это обусловлено тем, что антибиотик будет подавлять нормальную флору верхних дыхательных путей. Данная флора является барьером между организмом человека и болезнетворными бактериями. Оправдано использование антибиотиков лишь у детей с хроническими заболеваниями органов дыхания (например, муковисцидоз), иммунодефицитом.
Важно, чтобы ребенок получал достаточно жидкости во время простуды.
- Симптоматическое лечение. Является основным лечением при ОРВИ. Заключается в использовании таких методов и лекарственных средств, как:
- Адекватная гидратация. Иными словами – достаточный питьевой режим. Данный метод способствует разжижению секрета, что улучшает его отхождение.
- Элиминационная терапия. Ее суть заключается в введении в нос физиологического раствора 2-3 раза в день. Это способствует удалению слизи и восстановлению работы эпителия, который выстилает полость носа. Вводить физраствор необходимо в положении лежа на спине с запрокинутой назад головой. У грудных детей можно также использовать специальный ручной отсос для отсасывания слизи, а затем вводить физраствор. У старших детей оправдано использование солевых растворов в виде спрея. Элиминационная терапия может использоваться не только для лечения, но и для профилактики простуды у детей. По факту, адекватная гидратация и элиминационная терапия являются вспомогательными средствами для лечения простуды у ребенка.
- Сосудосуживающие капли в нос. Длительность применения не более 5 дней. Устраняют быстро заложенность носа, а также восстанавливают функцию слуховой трубы. Используют: фенилэфрин, оксиметазолин, ксилометазолин.
- Жаропонижающие средства. Для того, чтобы снизить температуру тела, можно использовать и физические методы. Малыша нужно раскрыть и обтереть водой 25-30 градусов. В педиатрии с целью снижения температуры тела ребенка используют только два препарата – парацетамол и ибупрофен. Являются недорогими лекарствами от простуды детям. Снижать температуру тела необходимо при 39-39,5 градусов. Более раннее снижение температуры рекомендовано в таких случаях: детям до 3-х месяцев, пациентам с хронической патологией, при развитии дискомфорта на фоне температуры. Регулярно принимать жаропонижающие средства не стоит. Повторную дозу принимают лишь после нового повышения температуры. В качестве жаропонижающего средства у детей ацетилсалициловую кислоту и нимесулид не используют. Не рекомендуется также использовать метамизол (анальгин). Во многих странах европы данный препарат запрещен к применению уже более 50 лет назад.
- Борьба с кашлем. В борьбе с кашлем поможет регулярный туалет носа, что уменьшает степень выраженности стекания слизи по задней стенки глотки. Также может помочь теплое питье, использование леденцов и пастилок, содержащих антисептики. Это обусловлено тем, что кашель может быть связан и с першением в горле на фоне фарингита. Антисептики позволяют купировать воспалительный процесс в горле и, соответственно, уменьшают степень выраженности кашля.
- Противокашлевые, отхаркивающие препараты, муколитики при ОРВИ использовать не рекомендуется.
- Согласно рекомендациям ВОЗ, использовать паровые и аэрозольные ингаляции для лечения ОРВИ не рекомендуется.
- Не рекомендуется использование аскорбиновой кислоты (витамина С). Данное лекарственное средство никак не влияет на течение заболевания. Таким образом, использование различных народных средств лечения детей, богатых витамином С не всегда целесообразно.
Указанные утверждения несут за собой доказательный характер и согласуются с современным протоколом лечения ОРВИ у детей, разработанный союзом педиатров России.
ОРВИ является довольно распространенным заболеванием, требующим особого внимания со стороны родителей. При лечении очень важно использовать лишь те препараты, которые несут за собой доказательный характер и рекомендованы современными протоколами для лечения. Не занимайтесь самолечением, при развитии симптомов заболевания проконсультируйтесь с врачом.
Ротавирусная инфекция
Ротавирусную инфекцию нередко называют еще ротавирусным гастроэнтеритом или кишечным гриппом, хотя к семейству вирусов гриппа ротавирус не относится. Путь передачи возбудителя – фекально-оральный, т.е. через грязные руки, хотя возможен и воздушно-капельный. Может поражать людей в любом возрасте.
Опасность самолечения при ротавирусных инфекциях
Не у всех заразившихся ротавирусом болезнь протекает одинаково. Ее тяжесть и продолжительность зависят не только от возраста, но и от общего состояния человека. Что же делать в случае, если заболели? Необходимо помнить, что иногда под маской ОРВИ могут скрываться очень серьезные заболевания, поэтому необходимо проявить осторожность и при первых же признаках болезни (рвота, жидкий стул, подъем температуры) немедленно обратиться к врачу. А при сильных болях в животе ни в коем случае не принимать обезболивающие средства, и немедленно вызвать скорую помощь.
Терапия ротавирусной инфекции требует комплексного подхода, поэтому не следует заниматься самолечением. Врач сможет оценить состояние пациента, и, учитывая тяжесть заболевания, подберет необходимые препараты, в том числе и противовирусные (например, АРБИДОЛ®).
Признаки ротавирусной инфекции
Это заболевание с коротким инкубационным периодом (1–5 дней) и острым началом с симптомами гастроэнтерита (в среднем 3-7 суток, а при тяжелом течении более 7 суток). Часто к симптомам гастроэнтерита может присоединяться и респираторный синдром. Период выздоровления занимает 4-5 суток.
У детей это заболевание зачастую проявляется более остро, чем у взрослых: резким, вплоть до 39 градусов, подъемом температуры, рвотой и обильным жидким водянистым стулом. В рвотных массах обычно содержится слизь, а тошнота начинается даже от небольших порций еды и питья. При обильной рвоте и диарее может разиться обезвоживание, представляющее реальную опасность для ребенка (Опасной для жизни является потеря с жидкостью 8%), а возможность восполнения потерь жидкости с питьем осложнена повышенным рвотным рефлексом.
У взрослых тошнота и рвота наблюдаются редко, проявления ротавирусной инфекции обычно ограничиваются умеренной диареей, общей слабостью и небольшим повышением температуры.
Помимо симптомов энтерита, заболевание сопровождают проявления, присущие ОРВИ: насморк, боль и покраснения в горле, слабость, отсутствие или снижение аппетита.
Дети относятся к группе высокого риска по тяжелому и осложненному течению ОРВИ и гриппа. Их иммунная система еще несовершенна и не всегда может дать адекватный отпор инфекции. Поэтому риск тяжелого течения и осложнений даже при обычной простуде у детей гораздо выше, чем у взрослых людей, следовательно, им чаще требуется лечение противовирусными средствами. Противовирусные препараты, используемые в детской практике, должны быть хорошо изучены в доклинических и клинических исследованиях, а также должны обладать высокой эффективностью и благоприятным профилем безопасности.
АРБИДОЛ® порошок для приготовления суспензии и таблетки 50 мг рекомендованы для лечения и профилактики гриппа А и В, и других ОРВИ у маленьких пациентов старше 2 лет, а также в комплексной терапии ротавирусной инфекции.
Эффективное противовирусное средство для детей
Вирусные заболевания являются самыми распространенными, особенно когда речь идет о детях. Эффективное противовирусное средство для детей — обязательный препарат, который должен всегда находиться в аптечке, об этом знает каждый хороший родитель.
Среди широчайшего выбора фармацевтических продуктов порой сложно определить самое эффективное противовирусное средство для детей. Первое требование, которому должно соответствовать хорошее эффективное противовирусное для детей — это безопасность. То есть, противовирусное средство для детей должно эффективно воздействовать на сам вирус или оказывать активное профилактическое действие, но при этом, ни в коем случае не влиять на естественную работу клеток организма детей.
Эффективное противовирусное для детей должно соответствовать всем требованиям и стандартам относительно качества сырья и технологического процесса производства препарата.
Типы противовирусных средств для детей
Противовирусные средства для детей делятся на 2 типа:
Иммуномодуляторы направлены на укрепление иммунной системы, поскольку именно она распознает инфицированные вирусом клетки и атакует их. ПППД — это препараты, которые нацелены непосредственно на уничтожение вирусов — их структуру и размножение.
Самые эффективные и хорошие современные противовирусные средства для детей объединяют в себе оба этих воздействия.
Детское противовирусное: как выбирать хорошее противовирусное средство для детей?
Итак, чтобы выбрать самое хорошее противовирусное средство для детей, нужно, следовать принципу «не навреди». Не любое детское противовирусное средство можно, например, давать грудничкам, поэтому подбирая медикамент для малыша стоит ориентироваться на его возраст.
Хорошее противовирусное средство для детей должно отличаться быстрым эффектом подавления обострений симптомов простуды и сокращать период болезни, при этом не давать побочных эффектов. Кроме того, хорошее детское противовирусное средство должно быть приятным на вкус, чтобы малыш не противился его принимать, но при этом, не содержать красителей, а также искусственных ароматизаторов.
Самое лучшее противовирусное средство для детей
Лучшие противовирусные средства для детей имеют самый высокий профиль безопасности.
Также лучшее противовирусное средство для детей не должно вызывать аллергических реакций и хорошо сочетаться с другими препаратами. Кроме того лучшие противовирусные средства для детей имеют широкий спектр действия они подавляют не только вирусы различных форм гриппа, но и герпесвирусы, респираторные вирусы и др.
Самыми эффективными и хорошими по праву считаются препараты, которые не только подавляют вирусы, но и стимулируют организм, вырабатывая естественный иммунитет, чтобы организм ребенка был готов самостоятельно противостоять проникновению вирусов в будущем.
«Анаферон» является примером фармакологического препарата, который претендует на звание самое лучшее противовирусное средство для детей.
Поскольку, его можно принимать детям возрастом от 1 месяца, профиль безопасности медикамента настолько высок, что позволяет назначать его детям, которые страдают астматическими и аллергическими реакциями.
Препарат «Анаферон» эффективно воздействует на вирусы гриппа А и В, парагриппа, аденовирусы, герпесвирусы и др., а также минимизирует риски развития осложнений после них. Длительный профилактический курс этим препаратом усиливает потенциал организма производить интерфероны — белки, которые борются с вирусами на внутриклеточном уровне, а также активирует запуск механизмов наращивания хорошей иммунной неспецифической системы (то есть, той, которая борется не с определенным вирусом, а направлена на разрушительное действие любого типа инфекции).
Вовремя данное малышу самое лучшее противовирусное средство для детей позволяет предотвратить всевозможные негативные воздействия простуды на работу различных систем детского организма. Также стоит помнить, что лучший способ обезопасить своего ребенка в любом возрасте заключается в обеспечении условий для формирования максимально сильного естественного иммунитета и применение профилактический мер.
Средства от насморка для детей: какие препараты можно использовать у ребенка от 2 лет
Соавтор, редактор и медицинский эксперт – Максимов Александр Алексеевич.
Дата последнего обновления: 28.04.2021 г.
Количество просмотров: 123 098.
Среднее время прочтения: 6 минут.
Содержание:
Первая помощь
Немедикаментозные методы лечения
Лекарственные средства
Правила применения препаратов для лечения насморка
О насморке (рините) говорят, когда у ребенка из-за воспаления слизистой оболочки носа появляются выделения и ощущение заложенности. Это может быть следствием общего переохлаждения, резких перепадов температуры окружающей среды, инфекции, аллергии или продолжительного механического воздействия.1 А в период новорожденности и при прорезывании зубов возможен физиологический насморк.
При подборе способов лечения учитывается не только причина ринита, но и возраст ребенка. Чем младше малыш, тем тщательнее нужно выбирать средства от насморка для детей. Можно использовать как немедикаментозные методы, так и специальные препараты. Лечение в любом случае назначает врач.
Наверх к содержанию
Первая помощь
Насморк причиняет ребенку дискомфорт, нарушает сон, повышает риск осложнений со стороны нижележащих отделов дыхательных путей, например тонзиллита и бронхолегочных заболеваний. У младенцев при заложенности носа затрудняется сосание. К счастью, детский насморк излечим, начинать оказывать ребенку помощь нужно уже при первых симптомах заболевания.
В первую очередь нужно очистить носовую полость. Грудным детям слизь удаляют аспиратором, предварительно закапав в каждую ноздрю солевой раствор для разжижения секрета. Подросшему ребенку желательно при насморке регулярно промывать нос специальными средствами2, даже если он уже умеет сморкаться.
При рините слизистая оболочка носа раздражена, отечна. Для уменьшения неприятных ощущений ее желательно смягчать при помощи масляных растворов витаминов А и Е (если у ребенка нет непереносимости). Для снижения отечности слизистой оболочки можно нанести на крылья носа специальную мазь с эфирными маслами.
Наверх к содержанию
Немедикаментозные методы лечения
Ингаляции. Во время паровых ингаляций частички лекарственного средства равномерно распределяются внутри носовой полости, оказывая противовоспалительное, увлажняющее и противомикробное действие. С этой целью используются щелочные минеральные воды, отвары и настои лекарственных растений (календулы, ромашки, шалфея, липового цвета, сосновых игл, можжевельника).
Прогревания околоносовых пазух. Эту процедуру можно начинать в первые дни насморка, если у ребенка нет нарастающей лихорадки, сильной интоксикации и гайморита. Могут применяться завернутые в хлопковую ткань теплое вареное яйцо, отварное пшено, нагретая на сковороде соль или песок. Прогревания способствуют уменьшению воспаления и отека слизистой оболочки, улучшают носовое дыхание.
Обильное питье. Частое обильное питье помогает восполнить потери жидкости, предупреждает пересыхание слизистой носа, стимулирует организм на борьбу с интоксикацией. Можно давать обычную и минеральную воду, компоты, отвары, травяные чаи, морсы, натуральные соки.
Наверх к содержанию
Лекарственные средства
Не всегда при насморке удается обойтись без лекарств. Но использовать их можно по назначению врача, выяснив точную причину ринита. Для детей лекарства от насморка выпускаются в виде капель и спреев, для облегчения симптомов могут использоваться средства разного действия.
Сосудосуживающие препараты. Сужая поверхностные мелкие сосуды, они снижают секрецию слизи и отек, улучшают носовое дыхание. Они не лечат насморк, а лишь уменьшают его основные симптомы.
Увлажняющие средства. Применение увлажняющих средств позволяет улучшить состояние слизистой оболочки носа и облегчить ее очищение. Обычно в состав входят солевые растворы определенной концентрации или стерильная морская вода.
Противовоспалительные и антисептические препараты. Содержат ионы серебра или эфирные масла эвкалипта, сосны, мяты. Обычно они назначаются ребенку при затянувшемся насморке, когда из-за размножающихся бактерий выделения из носа становятся густыми и желто-зелеными.
Противовирусные лекарства. Эти средства от насморка для детей содержат интерфероны, которые подавляют дальнейшее размножение вирусных частиц. Могут применяться по назначению врача на начальном этапе вирусной инфекции, сопровождающейся насморком.3
Топические антигистаминные препараты. ТИЗИН® Алерджи и другие средства из этой группы действуют местно, помогая быстро уменьшить отек слизистой оболочки носа при аллергическом насморке у ребенка.
Топические глюкокортикостероиды. Могут использоваться по назначению врача при поллинозах. Оказывают влияние на выраженность основных симптомов ринита.
Наверх к содержанию
Правила применения препаратов для лечения насморка
Большинство препаратов от насморка для детей противопоказаны в первый год жизни ребенка. Можно использовать только капли, концентрация которых зависит от возраста младенца. Их закапывают в каждую ноздрю после очищения носа, слегка наклоняя приподнятую голову ребенка в противоположную сторону. А с 2 лет детям можно использовать спреи. Сосудосуживающие препараты применяют 2–3 раза в день не более недели.
Информация в данной статье носит справочный характер и не заменяет профессиональной консультации врача. Для постановки диагноза и назначения лечения обратитесь к квалифицированному специалисту.
Список литературы:
- Кириченко И.М. Роль тонических деконгестантов в лечении острых ринитов у детей. Российский университет дружбы народов. Научно-клинический центр оториноларингологии Федерального медико-биологического агентства России, Москва. Медицинский совет, 2018 (2): 118-121.
- Chia-Ling Li, Hsiao-Chuan Lin, Chien-Yu Lin, Teh-Fu Hsu. Effectiveness of hypertonic saline nasal irrigation for alleviating allergic rhinitis in children: a systematic review and meta-analysis. Journal of Clinical Medicine. 2019 Jan; 8(1): 64.
- Крюков А.И., Кунельская Н.Л., Изотова Г.Н. и др. Подходы к терапии острого ринита. Научно-исследовательский клинический институт оториноларингологии им. Л.И. Свержевского Департамента здравоохранения г. Москвы. Медицинский совет, 2016 (9): 45-47.
Читайте также:
Лечение детского насморка
Насморк у новорожденного
Противовирусные препараты для детей и гриппа
Противовирусные препараты
Хотя CDC рекомендует ежегодно делать прививку от гриппа (гриппа) в качестве первого и наиболее важного шага в защите от гриппа, существуют также лекарства, которые могут лечить грипп. Эти «противовирусные препараты от гриппа» являются важным вариантом лечения детей с подозрением на грипп или подтвержденным диагнозом.
Противовирусные препараты для детей выпускаются в форме таблеток, жидкости, порошка для ингаляций или раствора для внутривенного введения.Они борются с гриппом, не давая вирусам гриппа размножаться в организме. Противовирусные препараты должны быть прописаны врачом — они не продаются без рецепта. В идеале противовирусные препараты для лечения гриппа следует начинать в течение 2 дней после заболевания, но детям с высоким риском осложнений гриппа или госпитализации все же может быть полезно, если противовирусное лечение начнется через 2 или более дней после заболевания. Если ребенок болеет гриппом, противовирусные препараты предлагают безопасный и эффективный вариант лечения.
Противовирусные препараты против гриппа работают только против вирусов гриппа — они не помогут против других вирусов, которые могут вызывать симптомы заболевания, похожие на грипп.
Преимущества противовирусного лечения гриппа
Противовирусные препараты против гриппа могут облегчить симптомы гриппа и сократить продолжительность заболевания. Противовирусные препараты работают лучше всего, если их начать сразу после болезни (в течение двух дней после появления симптомов). Раннее лечение гриппа противовирусными препаратами также снижает частоту инфекций уха и снижает потребность в лечении антибиотиками у детей в возрасте от 1 до 12 лет.Лечение противовирусными препаратами также может уменьшить более серьезные осложнения, связанные с гриппом, такие как пневмония и госпитализации. Исследования как взрослых, так и детей показывают, что лечение госпитализированных пациентов может быть полезным для предотвращения дыхательной недостаточности и смерти.
CDC и Американская академия педиатрии (AAP) рекомендуют противовирусные препараты для лечения подтвержденного или подозреваемого гриппа у детей с тяжелым, осложненным или прогрессирующим заболеванием или у детей, госпитализированных с подтвержденным или подозреваемым гриппом, как можно раньше.Незамедлительное начало противовирусного лечения также рекомендуется для детей, которые подвержены высокому риску серьезных осложнений гриппа и у которых есть подтвержденный или подозреваемый грипп любой степени тяжести. Дети с высоким риском осложнений, связанных с гриппом, включают детей младше 5 лет (особенно младше 2 лет) и детей любого возраста с определенными хроническими заболеваниями, такими как астма, диабет, болезни сердца или легких. Для получения дополнительной информации о рекомендациях AAP посетите веб-страницу ресурсов по гриппу Красной книги AAP Externalexternal.
Начало страницы
Противовирусные препараты, разрешенные для использования у детей
Если поставщик вашего ребенка прописывает вашему ребенку капсулы осельтамивира, а ваш ребенок не может проглотить капсулы, предписанные капсулы можно открыть, смешать с густой подслащенной жидкостью и дать таким образом.
Существует четыре противовирусных препарата от гриппа, одобренных Управлением по контролю за продуктами и лекарствами США (FDA) для использования в Соединенных Штатах, которые CDC рекомендуют для использования у детей в этот сезон гриппа:
- Осельтамивир (доступный в виде дженерика или под торговым названием Тамифлю®) одобрен для лечения гриппа у детей от 2 недель и старше.Осельтамивир для перорального применения выпускается в форме таблеток и жидкости. Хотя это не является частью утвержденных FDA показаний, пероральное применение осельтамивира для лечения гриппа у детей младше 14 дней.
- Занамивир (торговое название Relenza®) одобрен для лечения гриппа у детей от 7 лет и старше. Не рекомендуется применять детям с основным респираторным заболеванием, в том числе с астмой и другими хроническими заболеваниями легких. Ингаляционный занамивир вводится через специальный ингалятор (Diskhaler®).
- Перамивир (торговое название Rapivab®) вводится внутривенно и рекомендуется для детей от 2 лет и старше.
- Балоксавир (торговое название Xofluza®) — это таблетка, которая назначается однократно внутрь и одобрена для раннего амбулаторного лечения детей с гриппом в возрасте от 12 лет и старше.
Начало страницы
Побочные эффекты противовирусных препаратов
Побочные эффекты различаются для каждого лекарства. Наиболее частыми побочными эффектами осельтамивира являются тошнота и рвота.Занамивир может вызвать затруднение дыхания у людей с основным заболеванием легких, а перамивир может вызвать диарею. Сообщалось также о других менее распространенных побочных эффектах. Ваш лечащий врач может предоставить вам дополнительную информацию об этих препаратах, или вы можете посетить веб-сайт с внешним значком Управления по контролю за продуктами и лекарствами (FDA), чтобы получить конкретную информацию о противовирусных препаратах, включая листок-вкладыш от производителя.
Если ваш ребенок заболел гриппом
Лечащий врач вашего ребенка может помочь решить, следует ли вашему ребенку принимать противовирусные препараты, если он заболел гриппом в этом сезоне.Признаки и симптомы гриппа включают жар, головную боль, сильную усталость, сухой кашель, боль в горле, насморк или заложенность носа и мышечные боли. Важно отметить, что у некоторых детей, заболевших гриппом, не бывает температуры.
Для получения дополнительной информации о противовирусных препаратах от гриппа посетите раздел «Лечение — противовирусные препараты».
Начало страницы
Использование противовирусных препаратов в неонатальном периоде
Clin Perinatol. Авторская рукопись; доступно в PMC 1 марта 2013 г.
Опубликован в окончательной редакции как:
PMCID: PMC32
NIHMSID: NIHMS351802
Ричард Дж.Whitley
Заслуженный профессор, стипендиат Леба в области педиатрии, профессор педиатрии, микробиологии, медицины и нейрохирургии, Университет Алабамы в Бирмингеме, Бирмингем, AL
Ричард Дж. Уитли, заслуженный профессор, стипендиат Леба в педиатрии, профессор педиатрии, Микробиология, медицина и нейрохирургия, Университет Алабамы в Бирмингеме, Бирмингем, Алабама;
Окончательная отредактированная версия этой статьи издателем доступна в Clin Perinatol. См. Другие статьи в PMC, в которых цитируется опубликованная статья.Введение
Парентеральная терапия вирусных инфекций новорожденных и младенцев стала реальностью с появлением видарабина (аденин арабинозида) для лечения инфекций, вызванных вирусом простого герпеса (ВПГ) у новорожденных в начале 1980-х годов. С тех пор ацикловир стал препаратом выбора для лечения неонатальных инфекций HSV, а также множества других герпесвирусных инфекций. Аналогичным образом было установлено, что ганцикловир полезен для лечения врожденных цитомегаловирусных (ЦМВ) инфекций, поражающих центральную нервную систему (ЦНС).В этой главе будут рассмотрены уроки, извлеченные из лечения неонатального ВПГ и врожденных ЦМВ-инфекций в связи с применением ацикловира и ганцикловира. Хотя естественная история этих заболеваний рассматривается в другом месте в этом тексте, краткое изложение будет предшествовать подробному обсуждению имеющихся установленных и альтернативных методов лечения. Отсылаем читателя к более обширным обзорам противовирусной терапии у детей и взрослых [1, 2].
Терапия инфекций, вызванных вирусом простого герпеса
Неонатальные инфекции ВПГ встречаются примерно у 1 из 3200 родов в США [3], и примерно у двух третей из них развивается какая-либо форма заболевания ЦНС [4].Большинство случаев вызвано ВПГ-2 [5]. Риск передачи увеличивается при первичной материнской инфекции в третьем триместре, составляет 30–50%, и может быть снижен путем кесарева сечения, если HSV был изолирован из шейки матки или наружных половых органов незадолго до родов [3]. Согласно обзору Кимберлина, 85% случаев неонатального ВПГ происходят из-за передачи в период беременности и родов, в то время как 10% происходят в результате послеродовой передачи, и только 5% связаны с передачей in utero [6].
Младенцы с внутриутробной инфекцией ВПГ характеризуются тремя кожными признаками (активные поражения, рубцы), неврологическими признаками (микроцефалия, гидранэнцефалия) и данными глаз (хориоретинит, микрофтальмия), присутствующими при рождении.Было обнаружено, что внутриутробная инфекция HSV возникает как при первичной, так и при рецидивирующей материнской HSV-инфекции [7], хотя риск повторной инфекции меньше.
Инфекция HSV, приобретенная в послеродовом или послеродовом периоде, может быть классифицирована как заболевание кожи, глаз и / или рта (SEM), заболевание ЦНС или диссеминированное заболевание. По определению, болезнь SEM не затрагивает ЦНС. Распространенное заболевание может поражать ЦНС (75% случаев) вместе с множеством других систем органов, включая печень, надпочечники, желудочно-кишечный тракт, кожу, глаза или рот [8].Заболевание ЦНС также может иметь компонент вовлечения SEM, но не затрагивает другие системы органов. Из всех младенцев с неонатальной инфекцией ВПГ около 33% имеют заболевание ЦНС, а около 25% имеют диссеминированное заболевание [9]. Таким образом, около 50% младенцев с неонатальной инфекцией ВПГ имеют заболевание ЦНС.
Патогенез поражения ЦНС при неонатальных инфекциях ВПГ различается в зависимости от того, является ли инфекция диссеминированной. Энцефалит, связанный с диссеминацией, происходит из-за гематогенного распространения, тогда как изолированный энцефалит или энцефалит, связанный только с вовлечением SEM, вероятно, возникает из-за ретроградного внутринейронального транспорта HSV [4].Это различие соответствует клиническим проявлениям диссеминированного заболевания по сравнению с заболеванием ЦНС в том смысле, что распространение диссеминированного заболевания через кровь проявляется раньше (в среднем от 9 до 11 дней жизни) и вызывает более диффузное поражение мозга с множественными участками геморрагического некроза, в то время как заболевание ЦНС происходящий через более медленный аксональный транспорт, проявляется позже (примерно от 16 до 17 дней жизни) и обычно вызывает более очаговое поражение ЦНС [10].
Ранняя эра противовирусной терапии неонатальной инфекции ВПГ была отмечена повышением смертности при внутривенном введении видарабина, а также при внутривенном введении стандартной дозы (SD) ацикловира (30 мг / кг / день в 3 приема).Годовая смертность от диссеминированного заболевания снизилась с 85% при отсутствии терапии до 50% при использовании видарабина и 61% при использовании ацикловира SD, в то время как смертность за 1 год от заболевания ЦНС снизилась с 35% без лечения до 14% как для видарабина, так и для ацикловира SD [11]. Совсем недавно было показано, что ацикловир в высоких дозах (HD) дополнительно улучшает эти показатели смертности. При внутривенном введении ацикловира на HD (60 мг / кг / день в 3 приема в течение 21 дня) летальность в течение одного года составила 29% и 4% от диссеминированных заболеваний и заболеваний ЦНС, соответственно [12].В то время как HD ацикловир снижал заболеваемость младенцев с диссеминированным заболеванием (83% выживших имели нормальные исходы нервного развития), у младенцев с заболеванием ЦНС не наблюдалось значительного улучшения заболеваемости (31% выживших имели нормальные исходы неврологического развития).
Младенцы с поражением SEM имеют наилучший прогноз и, как указано ниже, им требуется всего 14 дней внутривенной терапии ацикловиром на HD.
Недавно супрессивная терапия ацикловиром для младенцев с ЦНС после завершения внутривенного лечения значительно улучшила неврологический исход, измеренный по шкале Bailey Developmental Scores [13].Этот режим привел к тому, что примерно 60% (по сравнению с 31%) детей с заболеванием ЦНС развились нормально или с легкими нарушениями. Лечение проводилось в дозе 300 / мг / м 2 в сутки в течение шести месяцев.
Терапия неонатальных инфекций, вызванных вирусом ветряной оспы
Женщины, перенесшие первичную инфекцию вируса ветряной оспы (VZV) в течение 48 часов после родов, имеют детей с риском развития ветряной оспы в течение первых трех недель жизни. Новорожденным этим женщинам традиционно вводят иммуноглобулин против опоясывающего лишая (ZIG), чтобы предотвратить заболевание.Однако при спорадической нехватке ZIG у некоторых новорожденных могут развиться неонатальные заболевания. Никакие контролируемые клинические испытания не оценивали терапию этого заболевания ацикловиром; однако специалисты рекомендуют этот препарат для лечения болезней новорожденных.
Доступные методы лечения инфекций HSV и VZV
Ацикловир (Ациклогуанозин, Зовиракс, ACV)
Ацикловир является наиболее часто назначаемым противовирусным средством для лечения инфекций HSV новорожденных и младенцев.Он был доступен для клинического использования в течение почти трех десятилетий и продемонстрировал замечательную безопасность и эффективность против легких и тяжелых инфекций, вызванных HSV и VZV, как у здоровых пациентов, так и у пациентов с ослабленным иммунитетом, включая новорожденных.
Химия и механизм действия
Ацикловир — аналог дезоксигуанозина. После преимущественного поглощения инфицированными вирусом клетками ацикловир фосфорилируется кодируемой вирусом тимидинкиназой (ТК). Последующее ди- и трифосфорилирование катализируется ферментами клетки-хозяина.Ацикловиртрифосфат предотвращает синтез вирусной ДНК как за счет ингибирования вирусной ДНК-полимеразы, так и за счет того, что он является терминатором цепи.
Спектр и устойчивость
Ацикловир наиболее активен против ВПГ; активность против VZV также значительна, но примерно в 10 раз меньше. Ацикловир считается препаратом выбора как при неонатальных инфекциях HSV, так и при VZV-инфекциях. Активность против ЦМВ низкая, поскольку ЦМВ не обладает активностью тимидинкиназы, а ДНК-полимераза ЦМВ слабо ингибируется ацикловиртрифосфатом.
Устойчивость HSV и VZV к ацикловиру стала важной клинической проблемой среди пациентов с ослабленным иммунитетом, получающих длительную терапию [14]. Устойчивость вирусов к ацикловиру обычно является результатом мутаций в вирусном гене TK, хотя мутации в гене вирусной ДНК-полимеразы также встречаются редко. Резистентные изоляты могут вызывать тяжелые, прогрессирующие, изнурительные заболевания слизистых оболочек у взрослых и, в редких случаях, висцеральное распространение [15, 16]. Изоляты HSV, устойчивые к ацикловиру, также были зарегистрированы у здоровых хозяев, чаще всего у пациентов с часто рецидивирующими генитальными инфекциями, которые лечились хроническим ацикловиром [17].
Показания к применению
Ацикловир эффективен для лечения инфекций, вызванных HSV и VZV, у иммунокомпетентных и иммунодефицитных хозяев, включая новорожденных. Для лечения неонатальных инфекций HSV рекомендуемая доза составляет 20 мг / кг / каждые 8 часов. Продолжительность терапии SEM-заболевания составляет 14 дней, в то время как для детей с ЦНС или диссеминированным заболеванием терапию следует продлить на 21 день.
Ацикловир для перорального применения — это экспериментальный подход к супрессивной терапии, который в настоящее время не одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов.
Фармакокинетика
После внутривенных доз от 2,5 до 15 мг / кг стационарные концентрации ацикловира колеблются от 6,7 до 20,6 мкг / мл. Ацикловир широко распространен; высокие концентрации достигаются в почках, легких, печени, сердце и кожных пузырьках; концентрации в спинномозговой жидкости (CSF) составляют около 50% от концентрации в плазме [18]. Ацикловир проникает через плаценту и накапливается в грудном молоке. Связывание с белками составляет от 9% до 33%, и менее 20% препарата метаболизируется до биологически неактивных метаболитов.Фармакокинетические данные для новорожденных при применении 20 мг / кг / доза отсутствуют.
При отсутствии нарушения функции почек период полувыведения ацикловира составляет от 2 до 3 часов у детей старшего возраста и взрослых и от 2,5 до 5 часов у новорожденных с нормальным клиренсом креатинина. Более 60% введенного препарата выводится с мочой [18]. Выведение продлевается у пациентов с нарушением функции почек; Период полувыведения составляет приблизительно 20 часов у лиц с терминальной стадией почечной недостаточности, что требует изменения дозы для пациентов с клиренсом креатинина менее 50 мл / мин / л.73 м 2 [19]. Ацикловир эффективно удаляется гемодиализом, но не постоянным амбулаторным перитонеальным диализом [20, 21].
Побочные эффекты
Ацикловир, как правило, является безопасным лекарством. Почечная дисфункция возникает в результате обструктивной нефропатии, вызванной образованием кристаллов ацикловира, осаждающихся в почечных канальцах. Иногда внутривенное введение ацикловира вызывает сыпь, потливость, тошноту, головную боль, гематурию и гипотонию. Высокие дозы ацикловира внутривенно (60 мг / кг / день) новорожденным были связаны с нейтропенией [22, 23].
Нейротоксичность может возникать у субъектов с нарушенной функцией почек, которые достигают высоких концентраций препарата в сыворотке [24]. Нейротоксичность проявляется в виде летаргии, спутанности сознания, галлюцинаций, тремора, миоклонуса, судорог, экстрапирамидных признаков и изменений состояния сознания, развивающихся в течение первых нескольких дней после начала терапии. Эти признаки и симптомы обычно проходят спонтанно в течение нескольких дней после прекращения приема ацикловира.
Хотя ацикловир обладает мутагенным действием при высоких концентрациях в некоторых анализах in vitro , он не обладает тератогенным действием на животных.Ограниченные данные о людях позволяют предположить, что использование ацикловира беременными женщинами не связано с врожденными дефектами или другими неблагоприятными исходами беременности.
Лекарственные взаимодействия
Вероятность почечной токсичности ацикловира увеличивается при приеме нефротоксических препаратов, таких как циклоспорин или амфотерицин B.
Терапия врожденной цитомегаловирусной инфекции
Цитомегаловирус (ЦМВ) обычно заражает людей во всем мире серозной инфекцией. 40% у подростков и приближается к 90% у взрослых с плохим социально-экономическим статусом [25, 26].Врожденная ЦМВ-инфекция — наиболее распространенная врожденная инфекция в развитых странах, обнаруживаемая примерно у 1% живорожденных младенцев в Соединенных Штатах [27]. Врожденные ЦМВ-инфекции чаще всего возникают при внутриутробной передаче, но, поскольку вирус распространяется с жидкостями организма, передача также может передаваться перинатально во время родов или постнатально через грудное молоко.
Из всех младенцев, рожденных с врожденной ЦМВ-инфекцией, примерно 7–10% имеют клинически очевидное заболевание при рождении [28].Клинические характеристики внутриутробной инфекции включают ограничение внутриутробного развития, гепатоспленомегалию, желтуху, тромбоцитопению, микроцефалию, перивентрикулярные кальцификации и хориоретинит. Согласно обзору Dollard, истинные показатели смертности трудно получить, и, как сообщается, они достигают 30% для младенцев с симптомами [29], но, скорее всего, в среднем составляют около 5–10% [30]. Смерть обычно происходит из-за проявлений инфекции, не связанных с ЦНС, таких как нарушение функции печени или кровотечение. По оценкам, 40–58% младенцев с симптоматической врожденной ЦМВ-инфекцией имеют необратимые последствия, в то время как младенцы, у которых нет симптомов при рождении, страдают постоянными последствиями почти в 14% случаев [29].Сенсорно-невральная потеря слуха (СНСС), умственная отсталость, судороги, задержка психомоторной и речевой активности, нарушение обучаемости, хориоретинит, атрофия зрительного нерва и дефекты зубных рядов являются наиболее частыми долгосрочными последствиями [31]. В отличие от внутриутробных инфекций, перинатально приобретенные ЦМВ-инфекции обычно не связаны с долгосрочными последствиями, хотя сообщалось об острых заболеваниях у недоношенных детей с очень низкой массой тела при рождении [32]. У доношенных детей перинатальные инфекции обычно протекают бессимптомно, но могут проявляться пневмонитом в течение первых нескольких месяцев жизни [33].
Врожденная ЦМВ-инфекция является следствием инфицирования матери и плода, причем большинство симптоматических врожденных случаев возникает из-за бессимптомной материнской инфекции. При материнской первичной инфекции, по-видимому, происходит нарушение плацентарного кровотока после инфицирования плацентарных вилок [34]. Патогенез поражения ЦНС при врожденной ЦМВ-инфекции начинается с диссеминированного распространения виремии, включая эндотелиальные клетки головного мозга и эпителиальные клетки сосудистого сплетения.Из эндотелиальных клеток головного мозга вирус распространяется на смежные астроциты. Из сосудистого сплетения вирус затем перемещается к эпендимным поверхностям через спинномозговую жидкость (CSF). После инфицирования этих клеток вирус подвергается непрерывной репликации, что приводит к характерным внутриядерным тельцам включения и гибели клеток. Поскольку антитела вырабатываются в условиях непрерывной репликации вируса, также образуются иммунные комплексы, что приводит к дальнейшему иммуноопосредованному повреждению [31]. Хотя специфический патогенез SNHL, опосредованного CMV, не выяснен, гистология показала доказательства инфекции в клетках как улиткового, так и вестибулярного эндолабиринта [35].ЦМВ также был выделен из перилимфы улитки при вскрытии новорожденных с врожденной ЦМВ-инфекцией [36].
Недавние исследования лечения ганцикловиром врожденных ЦМВ-инфекций с поражением ЦНС были многообещающими. Введение ганцикловира в дозах 12 мг / кг / день, разделенных каждые 12 часов в течение 6 недель, улучшило исходы слуха у новорожденных с симптоматической врожденной ЦМВ-инфекцией с поражением ЦНС (о чем свидетельствуют микроцефалия, внутричерепные кальцификации, аномалии спинномозговой жидкости для возраста, хориоретинит и др.) / или нарушения слуха) [37].Первичной конечной точкой был улучшенный ответ, вызванный стволом мозга (BSER) между исходным уровнем и 6-месячным периодом наблюдения (или отсутствие ухудшения в течение 6-месячного последующего наблюдения, если исходный BSER был нормальным). Что касается общего количества ушей, подлежащих оценке, 69% пациентов, получавших ганцикловир, достигли первичной конечной точки по сравнению с 39% в контрольной группе. Ни у одного пациента, получавшего ганцикловир, не было ухудшения слуха от исходного уровня до 6 месяцев. У реципиентов ганцикловира также отмечалось более быстрое разрешение нарушений АЛТ, чем в контрольной группе, хотя вероятность развития нейтропении у них была значительно выше.Дополнительный анализ этого рандомизированного контролируемого исследования позволяет предположить, что ганцикловир может также уменьшать задержки в развитии нервной системы [38]. Улучшение смертности при терапии ганцикловиром пока не показано.
Лечение ЦМВ-инфекций
Ганцикловир (Цитовен)
Ганцикловир был первым противовирусным препаратом, доступным для лечения и профилактики инфекций, вызванных ЦМВ. Доказано, что это очень ценный препарат для пациентов с ослабленным иммунитетом, особенно для пациентов с рецептами трансплантации гемопоэтических стволовых клеток, которые страдают от значительной заболеваемости и смертности от ЦМВ-инфекций, а в последнее время — для детей с врожденной ЦМВ-инфекцией, хотя и не одобрено Управлением по контролю за продуктами и лекарствами США Администрация (FDA) в настоящее время.
Химия и механизм действия
Ганцикловир структурно похож на ацикловир, за исключением гидроксиметильной группы на его ациклической боковой цепи. Первоначальный этап фосфорилирования осуществляется pUL97, вирусной протеинкиназой. Затем клеточные киназы фосфорилируют агент еще два раза, чтобы преобразовать его в его трифосфатное производное, которое способно ингибировать ДНК-полимеразу ЦМВ, кодируемую UL97 , а также встраиваться в вирусную ДНК и обрывать ее.
Ганцикловир трифосфат — конкурентный ингибитор герпесвирусных ДНК-полимераз, приводящий к прекращению удлинения цепи ДНК [1, 20].
Спектр и устойчивость
Ганцикловир имеет сходную с ацикловиром активность против HSV-1, HSV-2 и VZV, но, в отличие от ацикловира, его наибольшая активность против CMV. Устойчивость изолятов ЦМВ обычно возникает в результате мутаций в гене UL97 [39]. Мутации в гене ДНК-полимеразы ЦМВ встречаются реже. Показания .Ганцикловир лицензирован для нескольких показаний за пределами новорожденных. В нескольких обзорах резюмируются эти клинические исходы [2]. Для лечения новорожденных, врожденно инфицированных ЦМВ, было проведено контролируемое исследование [40]. Как отмечалось выше, по сравнению с отсутствием лечения, терапия ганцикловиром предотвращала ухудшение слуха через два года, хотя примерно у двух третей пролеченных младенцев развилась нейтропения, часто требующая изменения дозы.
Фармакокинетика
Пероральная биодоступность ганцикловира низкая, при пероральном приеме всасывается менее 10% препарата [41, 42].Пероральный препарат ганцикловира больше не продается. Пиковые концентрации ганцикловира в сыворотке крови после введения 6 мг / кг (доза для новорожденных) внутривенно вводимого лекарственного средства колеблются от 8 до 11 мкг / мл с концентрациями, достаточными для подавления чувствительных штаммов ЦМВ в водянистой влаге, субретинальной жидкости, спинномозговой жидкости и ткани мозга [ 1]. Период полувыведения ганцикловира составляет от 2 до 3 часов, и большая часть препарата выводится в неизмененном виде с мочой. Фармакокинетика ганцикловира в популяции новорожденных аналогична таковой у взрослых [43, 44].Снижение дозы, пропорциональное степени снижения клиренса креатинина, необходимо лицам с нарушением функции почек. Дополнительная доза рекомендуется после диализа, поскольку она эффективно удаляется гемодиализом [45].
Побочные эффекты
Миелосупрессия — наиболее частое побочное действие ганцикловира; Дозозависимая нейтропения (менее 1000 лейкоцитов / мкл) является наиболее стойким гематологическим отклонением с частотой около 40% [42]. Нейтропения ограничивает дозу примерно в одном из семи курсов и исчезает после прекращения приема препарата.При пероральном приеме ганцикловира нейтропения возникает реже. Тромбоцитопения (менее 50 000 тромбоцитов / мкл) встречается примерно у 20%, а анемия — примерно у 2% реципиентов ганцикловира. От 2 до 5% реципиентов ганцикловира испытывают головную боль, спутанность сознания, изменение психического статуса, галлюцинации, кошмары, беспокойство, атаксию, тремор, судороги. лихорадка, сыпь и аномальные уровни сывороточных печеночных ферментов по отдельности или в некоторой комбинации.
Дозировка
Доза ганцикловира для лечения симптоматической врожденной ЦМВ-инфекции составляет 12 мг / кг / день внутривенно дважды в день в течение 6 недель.
Исследуемый препарат
Валганцикловир (Valcyte)
Валганцикловир был одобрен FDA в марте 2001 г. для лечения ЦМВ-ретинита. Поскольку он хорошо всасывается после перорального приема, он может представлять собой благоприятный вариант по сравнению с внутривенным введением ганцикловира для лечения врожденной ЦМВ-инфекции. В настоящее время он лицензирован для лечения ЦМВ-инфекций в отдельных популяциях трансплантатов и ЦМВ-ретинита у пациентов с ВИЧ / СПИДом.
Химия, механизм действия, спектр и устойчивость
Валганцикловир является пролекарством ганцикловира на основе эфира L-валина и, как таковой, имеет тот же механизм действия, противовирусный спектр и потенциал развития устойчивости, что и ганцикловир [1, 20] .
Показания
Валганцикловир имеет аналогичные показания к ганцикловиру. Однако, основываясь на опубликованных на сегодняшний день ограниченных контролируемых исследованиях, в настоящее время он одобрен для индукционной и поддерживающей терапии ЦМВ-ретинита и для отдельных популяций трансплантатов [46].В настоящее время изучается возможность лечения врожденной ЦМВ-инфекции. В этом рандомизированном контролируемом исследовании, проводимом Группой по совместным антивирусным исследованиям (CASG) Национального института аллергии и инфекционных заболеваний (NIAID), в качестве основной конечной точки используется SNHL.
Фармакокинетика
Валганцикловир быстро превращается в ганцикловир со средним периодом полувыведения из плазмы около 30 минут [46]. Абсолютная биодоступность валганцикловира превышает 60% и фактически увеличивается примерно на 30% при одновременном приеме пищи [47].Площадь под кривой ганцикловира после перорального приема валганцикловира составляет от одной трети до половины площади, полученной после внутривенного введения ганцикловира. Пациентам с нарушением функции почек требуется снижение дозировки, примерно пропорциональное снижению клиренса креатинина.
Побочные эффекты
Наиболее частые побочные эффекты, связанные с терапией валганцикловиром у взрослых, включают диарею (41%), тошноту (30%), нейтропению (27%), анемию (26%) и головную боль (22%) [ 46].Лишь ограниченное число новорожденных получали терапию валганцикловиром. Единственным значимым открытием была нейтропения у 15% пациентов.
Дозировка
Доза валганцикловира зависит от возраста пациента и функции почек. В настоящее время препарат не разрешен к применению у новорожденных с врожденной ЦМВ-инфекцией.
Непроверенные и непроверенные методы лечения неонатальных инфекций HSV, VZV и врожденных ЦМВ-инфекций
Следующие два препарата используются для лечения инфекций HSV, VZV и CMV у детей старшего возраста и взрослых.Данные об этих препаратах предоставляются, если у новорожденных возникает резистентность к противовирусным препаратам при инфекциях ВПГ или ЦМВ. Ни один из препаратов не был оценен в рамках доказательных исследований на новорожденных, и оба связаны со значительной токсичностью. Кроме того, валацикловир может стать доступным для педиатрического применения, особенно для младенцев с инфекцией HSV, ограниченной кожей, глазами и ртом
Цидофовир (HPMPC, Vistide)
Цидофовир был впервые одобрен для использования в США для лечения СПИДа -ассоциированный ретинит, вызванный ЦМВ.Это остается основным показанием к применению этого противовирусного препарата.
Химия и механизм действия
Цидофовир представляет собой новый аналог ациклических фосфонатных нуклеозидов с механизмом действия, аналогичным другим аналогам нуклеозидов. В отличие от ацикловира, вирусные ферменты не требуются для начального фосфорилирования, поскольку нативный цидофовир уже имеет одну присоединенную фосфатную группу. После дифосфорализации клеточными киназами цидофовир конкурентно ингибирует ДНК-полимеразу [48].Активная форма цидофовира проявляет в 25-50 раз большее сродство к вирусной ДНК-полимеразе по сравнению с клеточной ДНК-полимеразой.
Спектр и устойчивость
Цидофовир активен против ВПГ и ЦМВ, включая устойчивые к ацикловиру и фоскарнету изоляты ВПГ и мутанты ЦМВ, устойчивые к ганцикловиру и фоскарнету [49]. Он также активен in vitro против VZV, EBV, вируса герпеса человека-6, вируса герпеса человека-8, полиомавирусов, аденовируса и ВПЧ человека.
Было описано небольшое количество устойчивых к цидофовиру изолятов ЦМВ, которые также устойчивы к ганцикловиру на основе мутаций в гене ДНК-полимеразы [50].Сообщалось также о мутанте ЦМВ, устойчивом к ганцикловиру, фоскарнету и цидофовиру [51].
Показания к применению
Цидофовир замедляет прогрессирование заболевания сетчатки у пациентов со СПИДом [52, 53]. Цидофовир также был полезен при лечении заболеваний, вызванных устойчивыми к ацикловиру изолятами ВПГ [54]. Были опубликованы отдельные сообщения об улучшении папилломатоза гортани после инъекции цидофовира в очаг поражения, но на основании этого ограниченного опыта невозможно сделать окончательные выводы об эффективности [55, 56].
Фармакокинетика
Только 2–26% цидофовира всасывается после перорального приема, поэтому его вводят внутривенно. Период полувыведения цидофовира из плазмы составляет 2,6 часа, но период полураспада активных внутриклеточных метаболитов цидофовира составляет от 17 до 48 часов [ 57]. Девяносто процентов препарата выводится с мочой, в основном с секрецией почечных канальцев [58]. Важно отметить, что препарат не проникает через гематоэнцефалический барьер и, следовательно, не должен использоваться для лечения инфекций ЦНС.
Побочные эффекты
Поскольку цидофовир концентрируется в почечных клетках в количествах в 100 раз больше, чем в других тканях, нефротоксичность является основным побочным эффектом, особенно если гидратация не поддерживается должным образом [57, 58].Проявления почечной токсичности включают протеинурию и глюкозурию. Агрессивная внутривенная прегидратация, одновременное введение пробенецида и отказ от других нефротоксичных агентов снижают вероятность токсичности. Цидофовир противопоказан пациентам с креатинином сыворотки> 1,5 мг / дл, расчетным клиренсом креатинина ≤ 55 мл / мин или белком в моче ≥ 100 мг / дл, и препарат следует прекратить, если креатинин сыворотки повышается на ≥ 0,5 мг / дл выше исходного уровня. .
Дозировка
Цидофовир вводят внутривенно детям старшего возраста и взрослым в дозе 5 мг / кг один раз в неделю с пробенецидом.Пациенты с нарушением функции почек (расчетный клиренс креатинина <55 мл / мин) проходят лечение каждые 2 недели. Дозу следует уменьшить с 5 мг / кг до 3 мг / кг, если креатинин сыворотки повышается на> 0,3 мг / дл выше исходного уровня. Данных о дозировании цидофовира новорожденным нет.
Фоскарнет (PFA, Foscavir)
Фоскарнет — единственный противогерпетический препарат, не являющийся аналогом нуклеозидов. Это не препарат первой линии, но он полезен для лечения инфекций, вызванных устойчивыми вирусами герпеса.
Химия и механизм действия
Фоскарнет — неорганический аналог пирофосфата, который напрямую ингибирует ДНК-полимеразу, блокируя сайт связывания пирофосфата [20, 59].
Спектр и устойчивость
Фоскарнет ингибирует все известные герпесвирусы человека, включая большинство устойчивых к ганцикловиру изолятов ЦМВ и устойчивые к ацикловиру вирусы простого герпеса и вируса зодиака. Он также активен против ВИЧ. Устойчивость возникает в результате мутаций ДНК-полимеразы. Сообщалось о штаммах CMV, HSV и VZV с пониженной чувствительностью к фоскарнету [59, 60].
Показания к применению
Фоскарнет так же эффективен, как и ганцикловир, для лечения угрожающего зрению хориоретинита, вызванного ЦМВ, у взрослых пациентов со СПИДом [61]. Из-за присущей ему активности против ВИЧ, он может даже обеспечить преимущество в выживаемости для пролеченных пациентов [62]. Рефрактерные случаи хориоретинита могут поддаваться лечению комбинацией фоскарнета и ганцикловира. Фоскарнет также эффективен при терапии ЦМВ-инфекций, вызванных ганцикловир-резистентными штаммами вируса [62]. Ограниченные данные также предполагают, что фоскарнет может быть полезным при назначении пациентам со СПИДом, у которых есть желудочно-кишечные и легочные инфекции, вызванные ЦМВ.
Инфекции, вызванные устойчивыми к ацикловиру штаммами HSV и VZV, успешно контролируются с помощью фоскарнета [63, 64].
Фармакокинетика
Только около 20% фоскарнета абсорбируется после перорального приема. Максимальная концентрация в сыворотке, достигаемая после внутривенного введения 60 мг / кг, составляет примерно 500 мкмоль / л [59]. Концентрация в спинномозговой жидкости составляет около двух третей от концентрации в сыворотке. Период полувыведения фоскарнета составляет около 48 часов, и 80% введенной дозы выводится в неизмененном виде с мочой.Необходимо снижение дозы пропорционально уменьшению клиренса креатинина. Гемодиализ эффективно устраняет фоскарнет, поэтому после диализа рекомендуется дополнительная доза [65]. Данных о применении фоскарнета новорожденным нет.
Побочные эффекты
Наиболее частыми побочными эффектами фоскарнета являются нефротоксичность и метаболические нарушения. Доказательства нефротоксичности включают азотемию, протеинурию, острый тубулярный некроз, кристаллурию и интерстициальный нефрит.Концентрация креатинина в сыворотке увеличивается до 50% пациентов. К счастью, функция почек приходит в норму в течение 2–4 недель после прекращения терапии. Существующее ранее заболевание почек, одновременный прием других нефротоксических препаратов, обезвоживание, быстрое введение или непрерывное внутривенное вливание препарата являются факторами риска развития почечной дисфункции [66]. Метаболические нарушения, связанные с терапией фоскарнетом, включают гипо- и гиперкальциемию, а также гипо- и гиперфосфатемию [67]. Гипокальциемия может быть связана с парестезиями, тетанией, судорогами и аритмиями.Метаболические нарушения сводятся к минимуму, если вводить фоскарнет медленной инфузией. Симптомы со стороны ЦНС, связанные с терапией фоскарнетом, включают головную боль, тремор, раздражительность, судороги и галлюцинации. Сообщалось также о лихорадке, тошноте, рвоте, аномальных ферментах сыворотки крови, анемии, гранулоцитопении и генитальных изъязвлениях.
Лекарственные взаимодействия
Одновременное применение амфотерицина B, циклоспорина, гентамицина и других нефротоксических препаратов увеличивает вероятность нарушения функции почек.Одновременный прием пентамидина увеличивает риск гипокальциемии. Анемия и нейтропения чаще встречаются, когда пациенты также получают зидовудин.
Дозировка
Обычная доза фоскарнета при ЦМВ-инфекции составляет 180 мг / кг / день в три приема в течение 14–21 дня, после чего следует ежедневная поддерживающая доза от 90 до 120 мг / кг. Дозировка фоскарнета, используемого при инфекциях, вызванных устойчивыми к ацикловиру HSV и VZV, составляет 120 мг / кг / день в три приема.
Резюме
Несмотря на то, что в лечении врожденных ЦМВ и неонатальных инфекций ВПГ достигнут значительный прогресс, дальнейшие достижения являются обязательными.С появлением новых противовирусных препаратов, обладающих другим механизмом действия, появляется возможность для комбинированной терапии, если можно доказать, что лекарства безопасны.
Выражение признательности
Этот проект полностью или частично финансируется за счет федеральных средств Национального института аллергии и инфекционных заболеваний, Национальных институтов здравоохранения, Министерства здравоохранения и социальных служб по контракту № N01-AI-30025.
Сноски
Заявление издателя: Это PDF-файл неотредактированной рукописи, принятой к публикации.В качестве услуги для наших клиентов мы предоставляем эту раннюю версию рукописи. Рукопись будет подвергнута копированию, верстке и рассмотрению полученного доказательства, прежде чем она будет опубликована в окончательной форме для цитирования. Обратите внимание, что во время производственного процесса могут быть обнаружены ошибки, которые могут повлиять на содержание, и все юридические оговорки, относящиеся к журналу, имеют отношение.
Ссылки
1. Кимберлин Д. Противовирусные агенты. В: Лонг С., Пикеринг Л., Пробер С., редакторы. Принципы и практика детских инфекционных болезней.3-е изд. Нью-Йорк: Эльзевир; 2008. С. 1470–1488. [Google Scholar] 2. Ра Б., Кимберлин Д. В., Уитли Р. Противовирусные препараты. В: Джером К., редактор. Лабораторная диагностика вирусных инфекций. 3-е изд. Нью-Йорк: Informa Healthcare; 2009. [Google Scholar] 3. Brown ZA, Wald A, Morrow RA, Selke S, Zeh J, Corey L. Влияние серологического статуса и кесарева сечения на скорость передачи вируса простого герпеса от матери к ребенку. ДЖАМА. 2003. 289 (2): 203–209. [PubMed] [Google Scholar] 4. Уитли Р.Дж. Вирус простого герпеса.В: Scheld MW, Whitley RJ, Marra CM, редакторы. Инфекции центральной нервной системы. 3-е изд. Филадельфия: Липпинкотт Уильямс и Уилкинс; 2004. С. 123–144. [Google Scholar] 5. Kimberlin DW, Lin CY, Jacobs RF, Powell DA, Frenkel LM, Gruber WC, et al. Естественная история инфекций, вызванных вирусом простого герпеса новорожденных, в эпоху ацикловира. Педиатрия. 2001. 108 (2): 223–229. [PubMed] [Google Scholar] 6. Kimberlin DW. Ведение энцефалита, вызванного вирусом простого герпеса, у взрослых и новорожденных: диагностика, прогноз и лечение.Герпес. 2007 июн; 14 (1): 11–16. [PubMed] [Google Scholar] 7. Хатто С., Арвин А., Джейкобс Р., Стил Р., Стагно С., Лайрин Р. и др. Внутриутробные инфекции, вызванные вирусом простого герпеса. Журнал педиатрии. 1987. 110 (1): 97–101. [PubMed] [Google Scholar] 8. Уитли Р.Дж. Инфекции, вызванные вирусом простого герпеса. В: Remington JS, Klein JO, редакторы. Инфекционные болезни плода и новорожденных. 3-е изд. Филадельфия: W.B. Компания Сондерс; 1990. С. 282–305. [Google Scholar] 9. Уитли Р.Дж., Кори Л., Арвин А., Лейкман Ф.Д., Сумая К.В., Райт П.Ф. и др.Изменение представления инфекции вируса простого герпеса у новорожденных. Журнал инфекционных болезней. 1988. 158 (1): 109–116. [PubMed] [Google Scholar] 10. Уитли Р.Дж., Ройзман Б. Вирусы простого герпеса. В: Ричман Д.Д., Уитли Р.Дж., Хайден Ф.Г., редакторы. Клиническая вирусология. 2-е изд. Вашингтон, округ Колумбия: ASM Press; 2004. С. 375–401. [Google Scholar] 11. Уитли Р., Арвин А., Пробер С., Берчетт С., Кори Л., Пауэлл Д. и др. Контролируемое испытание по сравнению видарабина с ацикловиром при неонатальной инфекции вирусом простого герпеса.Медицинский журнал Новой Англии. 1991. 324 (7): 444–449. [PubMed] [Google Scholar] 12. Kimberlin DW, Lin CY, Jacobs RF, Powell DA, Corey L, Gruber WC, et al. Безопасность и эффективность высоких доз внутривенного ацикловира при лечении инфекций, вызванных вирусом простого герпеса у новорожденных. Педиатрия. 2001. 108 (2): 230–238. [PubMed] [Google Scholar] 13. Кимберлин Д., Уитли Р., Ван В., Пауэлл Д., Сторч Г., Ахмед А. и др. Влияние перорального подавления ацикловира на исходы развития нервной системы и рецидивы кожи после болезни, вызванной вирусом простого герпеса новорожденных.NEJM. 2011 В печати. [Google Scholar] 14. Englund JA, Zimmerman ME, Swierkosz EU, Goodman JL, Scholl D, Balfour HH. Вирус простого герпеса устойчив к ацикловиру. Исследование в центре высокоспециализированной медицинской помощи. Ann Intern Med. 1990; 112: 416–422. [PubMed] [Google Scholar] 15. Полевой АК, Бирон К.К. Возвращение к «концу невинности»: устойчивость герпесвирусов к противовирусным препаратам. Clin Microbiol Rev.1994, январь; 7 (1): 1–13. [Бесплатная статья PMC] [PubMed] [Google Scholar] 16. Лайалл Э.Г., Огилви М.М., Смит Н.М., Бернс С. Устойчивость к ацикловиру ветряной оспы и ВИЧ-инфекция.Arch Dis Child. 1994 Февраль; 70 (2): 133–135. [Бесплатная статья PMC] [PubMed] [Google Scholar] 17. Морфин Ф, Тувено Д. Устойчивость вируса простого герпеса к противовирусным препаратам. J Clin Virol. 2003 Янв; 26 (1): 29–37. [PubMed] [Google Scholar] 18. Wagstaff AJ, Faulds D, Goa Kl. Ацикловир. Переоценка его противовирусной активности, фармакокинетических свойств и терапевтической эффективности. Наркотики. 1994; 47: 153–205. [PubMed] [Google Scholar] 19. Ласкин О.Л., Лонгстрет Дж. А., Велтон А., Красный Х. С., Кини Р. Э., Рокко Л. и др. Влияние почечной недостаточности на фармакокинетику ацикловира.Am J Med. 20 июля 1982 г .; 73 (1A): 197–201. [PubMed] [Google Scholar] 20. Инь М., Браст Дж., Тиеу Х., Хаммер С. Антигепатитные и антиреспираторные вирусные агенты. В: Ричман Д., Уитли Р., Хайден Ф., редакторы. Клиническая вирусология. Вашингтон, округ Колумбия: ASM Press; 2009. С. 217–264. [Google Scholar] 21. Красный ХК, Ляо С.Х., де Миранда П., Ласкин О.Л., Велтон А., Литман П.С. Влияние гемодиализа на фармакокинетику ацикловира у пациентов с хронической почечной недостаточностью. Am J Med. 20 июля 1982 г.; 73 (1A): 202–204. [PubMed] [Google Scholar] 22.Кимберлин Д., Пауэлл Д., Грубер В., Диаз П., Арвин А., Кумар М. и др. Назначение пероральной супрессивной терапии ацикловиром после неонатального заболевания, вызванного вирусом простого герпеса, ограниченным поражением кожи, глаз и рта: результаты тиража фазы I / II. Pediatr Infect Dis J. 1996; 15: 247–254. [PubMed] [Google Scholar] 23. Kimberlin DW, Lin CY, Jacobs RF, Powell DA, Corey L, Gruber WC, et al. Безопасность и эффективность высоких доз внутривенного ацикловира при лечении инфекций, вызванных вирусом простого герпеса у новорожденных. Педиатрия.2001 август; 108 (2): 230–238. [PubMed] [Google Scholar] 24. Реванкар С.Г., Эпплгейт А.Л., Марковиц Д.М. Делирий, связанный с лечением ацикловиром у пациента с почечной недостаточностью. Clin Infect Dis. 1995 августа; 21 (2): 435–436. [PubMed] [Google Scholar] 25. Гриффитс П.Д., Эмери В.К. Цитомегаловирус. В: Ричман Д.Д., Уитли Р.Дж., Хайден Ф.Г., редакторы. Клиническая вирусология. 2-е изд. Вашингтон, округ Колумбия: ASM Press; 2002. С. 433–461. [Google Scholar] 26. Старас С.А., Доллард СК, Рэдфорд К.В., Фландрия В.Д., Пасс РФ, Кэннон М.Дж. Распространенность цитомегаловирусной инфекции в США: 1988–1994 гг.Clin Infect Dis. 2006 г., 1 ноября; 43 (9): 1143–1151. [PubMed] [Google Scholar] 27. Demmler GJ. Американское общество инфекционных болезней и Центры по контролю за заболеваниями. Резюме семинара по надзору за врожденным цитомегаловирусным заболеванием. Обзоры инфекционных болезней. 1991. 13 (2): 315–329. [PubMed] [Google Scholar] 28. Conboy TJ, Pass RF, Stagno S, Alford CA, Myers GJ, Britt WJ и др. Ранние клинические проявления и интеллектуальный исход у детей с симптоматической врожденной цитомегаловирусной инфекцией.Журнал педиатрии. 1987. 111 (3): 343–348. [PubMed] [Google Scholar] 29. Доллард СК, Гросс С.Д., Росс Д.С. Новые оценки распространенности неврологических и сенсорных последствий и смертности, связанных с врожденной цитомегаловирусной инфекцией. Rev Med Virol. 1 июня 2007 г .; [PubMed] [Google Scholar] 30. Росс С.А., Боппана С.Б. Врожденная цитомегаловирусная инфекция: исход и диагноз. Semin Pediatr Infect Dis. 2005 Янв; 16 (1): 44–49. [PubMed] [Google Scholar] 31. Гриффитс PD, Маклафлин JE. Цитомегаловирус.В: Scheld WM, Whitley RJ, Marra CM, редакторы. Инфекции центральной нервной системы. Филадельфия: Липпинкотт Уильямс и Уилкинс; 2004. С. 159–173. [Google Scholar] 32. Машманн Дж., Хампрехт К., Дитц К., Ян Дж., Шпеер С.П. Цитомегаловирусная инфекция младенцев с крайне низкой массой тела при рождении через грудное молоко. Клинические инфекционные болезни. 2001; 33 (12): 1998–2003. [PubMed] [Google Scholar] 33. Brasfield DM, Stagno S, Whitley RJ, Cloud G, Cassell G, Tiller RE. Детский пневмонит, связанный с цитомегаловирусом, хламидиозом, пневмоцистом и уреаплазмой.Педиатрия. 1987. 79: 76–83. [PubMed] [Google Scholar] 34. Перейра Л., Майджи Э. Цитомегаловирусная инфекция в плаценте человека: материнский иммунитет и рецепторы, регулируемые развитием трофобластов, сходятся. Актуальные темы микробиологии и иммунологии. 2008. 325: 383–395. [PubMed] [Google Scholar] 35. Штраус М. Цитомегаловирусный лабиринтит человека. Am J Otolaryngol. Сентябрь – октябрь 1990 г., 11 (5): 292–298. [PubMed] [Google Scholar] 36. Дэвис Л. Е., Джонссон Л. Г., Корнфельд М. Цитомегаловирусный лабиринтит у младенцев: морфологические, вирусологические и иммунофлуоресцентные исследования.J Neuropathol Exp Neurol. 1981, январь; 40 (1): 9–19. [PubMed] [Google Scholar] 37. Kimberlin DW, Lin CY, Sanchez PJ, Demmler GJ, Dankner W, Shelton M и др. Влияние терапии ганцикловиром на слух при симптоматическом врожденном цитомегаловирусном заболевании с поражением центральной нервной системы: рандомизированное контролируемое исследование. Журнал педиатрии. 2003. 143 (1): 16–25. [PubMed] [Google Scholar] 38. Оливер С., Клауд Дж., Санчес П., Деммлер Дж., Данкнер В., Шелтон М. и др. Влияние терапии ганцикловиром (GCV) на исходы нервного развития при симптоматических врожденных цитомегаловирусных (CMV) инфекциях с поражением центральной нервной системы (ЦНС): рандомизированное контролируемое исследование.Ежегодное собрание Общества педиатрических исследований (SPR); 2006 29 апреля; Сан-Франциско, Калифорния. 2006. с. Реферат № 752908. [Google Scholar] 39. Маркхэм А., Фолдс Д. Ганцикловир: обновление его терапевтического использования при цитомегаловирусной инфекции. Наркотики. 1994; 48: 455. [PubMed] [Google Scholar] 40. Kimberlin DW, Lin C-Y, Sanchez PJ, Demmler GJ, Dankner W, Shelton MD, et al. Влияние ганцикловира на слух при симптоматическом врожденном цитомегаловирусном заболевании с поражением центральной нервной системы: рандомизированное контролируемое исследование.J Pediatr. 2003. 143: 16–25. [PubMed] [Google Scholar] 41. Редди В., Хао Ю., Липтон Дж., Мехарчанд Дж., Минден М., Мацзулли Т. и др. Ведение реципиентов аллогенного трансплантата костного мозга с риском цитомегаловирусной болезни с использованием контрольной бронхоскопии и длительной упреждающей терапии ганцикловиром. J Clin Virol. 1999, август; 13 (3): 149–159. [PubMed] [Google Scholar] 42. Jacobson MA, Gambertoglio JG, Aweeka FT, Causey DM, Portale AA. Гипокальциемия, вызванная фоскарнетом, и влияние фоскарнета на метаболизм кальция.J Clin Endocrinol Metab. 1991 Май; 72 (5): 1130–1135. [PubMed] [Google Scholar] 43. Френкель Л.М., Каппарелли Е.В., Данкнер В.М., Сюй Дж., Смит И.Л., Баллоу А. и др. Ганцикловир для приема внутрь у детей: фармакокинетика, безопасность, переносимость и противовирусное действие. Группа педиатрических клинических испытаний СПИДа. Журнал инфекционных болезней. 2000 декабрь; 182 (6): 1616–1624. [PubMed] [Google Scholar] 44. Транг Дж. М., Кидд Л., Грубер В., Сторч Дж., Деммлер Дж., Джейкобс Р. и др. Линейная фармакокинетика однократной дозы ганцикловира у новорожденных с врожденными цитомегаловирусными инфекциями.Clin Pharmacol Ther. 1993; 53: 15–21. [PubMed] [Google Scholar] 45. Свон С.К., Мунар М.Ю., Виггер М.А., Беннетт В.М. Фармакокинетика ганцикловира у пациента, находящегося на гемодиализе. Am J Kidney Dis. 1991, январь; 17 (1): 69–72. [PubMed] [Google Scholar] 46. Cocohoba JM, McNicholl IR. Валганцикловир: прогресс в лечении цитомегаловирусов. Энн Фармакотер. 2002 июнь; 36 (6): 1075–1079. [PubMed] [Google Scholar] 47. Юнг Д., Дорр А. Фармакокинетика однократной дозы валганцикловира у ВИЧ- и ЦМВ-серопозитивных субъектов.J Clin Pharmacol. 1999, август; 39 (8): 800–804. [PubMed] [Google Scholar] 48. Хо Х.Т., Вудс К.Л., Бронсон Дж. Дж., Де Бок Х., Мартин Дж. К., Хичкок МД. Внутриклеточный метаболизм антигерпетических средств -1- {3-гидрокси-2- (фосфонилметокси) пропил} цитозин. Mol Pharmacol. 1992; 41: 197–202. [PubMed] [Google Scholar] 49. Сафрин С, Черрингтон Дж, Джаффе Х.С. Клиническое использование цидофовира. Rev Med Virol. 1997 сентябрь; 7 (3): 145–156. [PubMed] [Google Scholar] 50. Lurain N, Spafford LE, Thompson KD. Мутация в открытой рамке считывания UL97 штаммов цитомегаловируса человека, устойчивых к ганцикловиру.Журнал вирусологии. 1994b; 68: 4427–4431. [Бесплатная статья PMC] [PubMed] [Google Scholar] 51. Черрингтон Дж. М., Майнер Р., Аллен С. Дж. У. и др. Сенситивы клинических изолятов цитомегаловируса человека (HCMV) к цидофовиру. Восьмая международная конференция по противовирусным исследованиям; 1995 г. 23–28 апреля; Санта-Фе, Нью-Мексико. 1995. [Google Scholar] 52. Исследования глазных осложнений Группы исследований СПИДа в сотрудничестве с Группой клинических испытаний СПИДа. Цидофовир (HPMPC) для лечения цитомегаловирусного ретинита у пациентов со СПИДом: исследование HPMPC Peripheral Cytomegalovirus Retinitis Trial.Ann Intern Med. 1997. 126: 264–274. [PubMed] [Google Scholar] 53. Lalezari JP, Staagg RJ, Kuppermann BD, Holland GN, Kramer F, Ives DV, et al. Внутривенное введение цидофовира при периферическом цитомегаловирусном ретините у пациентов со СПИДом: рандомизированное контролируемое исследование. Ann Intern Med. 1997. 126: 257–263. [PubMed] [Google Scholar] 54. Лалезари Дж. П., Дрю В. Л., Глутцер Э., Майнер Д., Сафрин С., Оуэн В. Ф., младший и др. Лечение внутривенным (S) -1- [3-гидрокси-2- (фосфонилметокси) пропил) -цитозином ацикловир-резистентной кожно-слизистой инфекции вирусом простого герпеса у пациента со СПИДом.Журнал инфекционных болезней. 1994; 170: 570–572. [PubMed] [Google Scholar] 55. Кимберлин DW, Малис DJ. Рецидивирующий респираторный папилломатоз с юношеским началом: возможности успешной противовирусной терапии. Antiviral Res. 2000 Февраль; 45 (2): 83–93. [PubMed] [Google Scholar] 56. Прански С.М., Магит А.Е., Кернс Д.Б., Канг Д.Р., Дункан Н.О. Цидофовир внутриочаговый при рецидивирующем респираторном папилломатозе у детей. Arch Otolaryngol Head Neck Surg. 1999 Октябрь; 125 (10): 1143–1148. [PubMed] [Google Scholar] 57. Канди К.С., Петти Б.Г., Флаэрти Дж., Фишер П.Е., Полис М.А., Ваксман М. и др.Клиническая фармакокинетика цидофовира у пациентов, инфицированных вирусом иммунодефицита человека. Антимикробные агенты Chemother. 1995; 39: 1247–1252. [Бесплатная статья PMC] [PubMed] [Google Scholar] 58. Лалезари Дж. П., Дрю В. Л., Глутцер Э., Джеймс С., Майнер Д., Флаэрти Дж. И др. (S) -1 {3-гидрокси-2- (фосфонилметокси) пропил} цитозин (цидофовиир): результаты исследования фазы I / II нового противовирусного аналога нуцелотида. Журнал инфекционных болезней. 1995; 171: 788–796. [PubMed] [Google Scholar] 59. Wagstaff AJ, Bryson HM.Фоскарнет: переоценка его противовирусной активности, фармакокинетических свойств и терапевтического использования у пациентов с ослабленным иммунитетом и вирусной инфекцией. Наркотики. 1994; 48: 199–226. [PubMed] [Google Scholar] 60. Сафрин С., Кеммерли С., Плоткин Б., Смит Т., Вайсбах Н., Де Веранес Д. и др. Инфекция, вызванная устойчивым к фоскарнету вирусом простого герпеса, у больных СПИДом. Журнал инфекционных болезней. 1994; 169: 193–196. [PubMed] [Google Scholar] 61. Снок Р., Андрей Г., Джерард М., Сильверман А., Хеддерман А., Бальзарини Дж. И др.Успешное лечение прогрессирующей кожно-слизистой инфекции, вызванной устойчивым к ацикловиру и фоскарнету вирусом простого герпеса, с помощью (S) -1- (3-гидрокси-2-фосфонилметоксипропил) цитозина (HPMPC) Clin Infect Dis. 1994 Апрель; 18 (4): 570–578. [PubMed] [Google Scholar] 62. Якобсон М.А., Дрю В.Л., Фейнберг Дж., О’Доннелл Дж. Дж., Уитмор П.В., Майнер Р.Д. и др. Терапия фоскарнетом при ганцикловиррезистентном цитомегаловирусном ретините у больных СПИДом. Журнал инфекционных болезней. 1991; 163: 1348–1351. [PubMed] [Google Scholar] 63.Сафрин С., Бергер Т.Г., Гилсон И. Терапия фоскарнетом у пяти пациентов со СПИДом и инфекцией вируса ветряной оспы, устойчивой к ацикловиру. Ann Intern Med. 1991; 115: 19–21. [PubMed] [Google Scholar] 64. Исследования глазных осложнений исследовательской группы СПИДа. Смертность у пациентов с синдромом приобретенного иммунодефицита, получавших фоскарнет или ганцикловир от цитомегаловируса ретинита. N Engl J Med. 1992; 326: 213–220. [PubMed] [Google Scholar] 65. Сафрин С., Крампакер С., Чатис П., Дэвис Р., Хафнер Р., Раш Дж. И др.Контролируемое исследование по сравнению фоскарнета и видарабина при лечении ацикловир-резистентного кожно-слизистого простого герпеса при синдроме приобретенного иммунодефицита. N Engl J Med. 1991; 325: 551–555. [PubMed] [Google Scholar] 66. МакГрегор Р. Р., Грациани А. Л., Вайс Р., Грюнвальд Дж. Э., Гамбертольо Дж. Г.. Успешная терапия фоскарнетом при цитомегаловирусном ретините у пациента со СПИДом, находящегося на гемодиализе: обоснование эмпирического дозирования и мониторинга уровня в плазме. Журнал инфекционных болезней. 1991 Октябрь; 164 (4): 785–787.[PubMed] [Google Scholar] 67. Дерай Г., Мартинес Ф., Катлама С., Левальтье Б., Бофилс Н., Данис М. и др. Нефротоксичность фоскарнета: механизм, частота возникновения и профилактика. Am J Nephrol. 1989. 9 (4): 316–321. [PubMed] [Google Scholar]Использование противовирусных препаратов в период новорожденности
Clin Perinatol. Авторская рукопись; доступно в PMC 1 марта 2013 г.
Опубликован в окончательной редакции как:
PMCID: PMC32
NIHMSID: NIHMS351802
Ричард Дж.Whitley
Заслуженный профессор, стипендиат Леба в области педиатрии, профессор педиатрии, микробиологии, медицины и нейрохирургии, Университет Алабамы в Бирмингеме, Бирмингем, AL
Ричард Дж. Уитли, заслуженный профессор, стипендиат Леба в педиатрии, профессор педиатрии, Микробиология, медицина и нейрохирургия, Университет Алабамы в Бирмингеме, Бирмингем, Алабама;
Окончательная отредактированная версия этой статьи издателем доступна в Clin Perinatol. См. Другие статьи в PMC, в которых цитируется опубликованная статья.Введение
Парентеральная терапия вирусных инфекций новорожденных и младенцев стала реальностью с появлением видарабина (аденин арабинозида) для лечения инфекций, вызванных вирусом простого герпеса (ВПГ) у новорожденных в начале 1980-х годов. С тех пор ацикловир стал препаратом выбора для лечения неонатальных инфекций HSV, а также множества других герпесвирусных инфекций. Аналогичным образом было установлено, что ганцикловир полезен для лечения врожденных цитомегаловирусных (ЦМВ) инфекций, поражающих центральную нервную систему (ЦНС).В этой главе будут рассмотрены уроки, извлеченные из лечения неонатального ВПГ и врожденных ЦМВ-инфекций в связи с применением ацикловира и ганцикловира. Хотя естественная история этих заболеваний рассматривается в другом месте в этом тексте, краткое изложение будет предшествовать подробному обсуждению имеющихся установленных и альтернативных методов лечения. Отсылаем читателя к более обширным обзорам противовирусной терапии у детей и взрослых [1, 2].
Терапия инфекций, вызванных вирусом простого герпеса
Неонатальные инфекции ВПГ встречаются примерно у 1 из 3200 родов в США [3], и примерно у двух третей из них развивается какая-либо форма заболевания ЦНС [4].Большинство случаев вызвано ВПГ-2 [5]. Риск передачи увеличивается при первичной материнской инфекции в третьем триместре, составляет 30–50%, и может быть снижен путем кесарева сечения, если HSV был изолирован из шейки матки или наружных половых органов незадолго до родов [3]. Согласно обзору Кимберлина, 85% случаев неонатального ВПГ происходят из-за передачи в период беременности и родов, в то время как 10% происходят в результате послеродовой передачи, и только 5% связаны с передачей in utero [6].
Младенцы с внутриутробной инфекцией ВПГ характеризуются тремя кожными признаками (активные поражения, рубцы), неврологическими признаками (микроцефалия, гидранэнцефалия) и данными глаз (хориоретинит, микрофтальмия), присутствующими при рождении.Было обнаружено, что внутриутробная инфекция HSV возникает как при первичной, так и при рецидивирующей материнской HSV-инфекции [7], хотя риск повторной инфекции меньше.
Инфекция HSV, приобретенная в послеродовом или послеродовом периоде, может быть классифицирована как заболевание кожи, глаз и / или рта (SEM), заболевание ЦНС или диссеминированное заболевание. По определению, болезнь SEM не затрагивает ЦНС. Распространенное заболевание может поражать ЦНС (75% случаев) вместе с множеством других систем органов, включая печень, надпочечники, желудочно-кишечный тракт, кожу, глаза или рот [8].Заболевание ЦНС также может иметь компонент вовлечения SEM, но не затрагивает другие системы органов. Из всех младенцев с неонатальной инфекцией ВПГ около 33% имеют заболевание ЦНС, а около 25% имеют диссеминированное заболевание [9]. Таким образом, около 50% младенцев с неонатальной инфекцией ВПГ имеют заболевание ЦНС.
Патогенез поражения ЦНС при неонатальных инфекциях ВПГ различается в зависимости от того, является ли инфекция диссеминированной. Энцефалит, связанный с диссеминацией, происходит из-за гематогенного распространения, тогда как изолированный энцефалит или энцефалит, связанный только с вовлечением SEM, вероятно, возникает из-за ретроградного внутринейронального транспорта HSV [4].Это различие соответствует клиническим проявлениям диссеминированного заболевания по сравнению с заболеванием ЦНС в том смысле, что распространение диссеминированного заболевания через кровь проявляется раньше (в среднем от 9 до 11 дней жизни) и вызывает более диффузное поражение мозга с множественными участками геморрагического некроза, в то время как заболевание ЦНС происходящий через более медленный аксональный транспорт, проявляется позже (примерно от 16 до 17 дней жизни) и обычно вызывает более очаговое поражение ЦНС [10].
Ранняя эра противовирусной терапии неонатальной инфекции ВПГ была отмечена повышением смертности при внутривенном введении видарабина, а также при внутривенном введении стандартной дозы (SD) ацикловира (30 мг / кг / день в 3 приема).Годовая смертность от диссеминированного заболевания снизилась с 85% при отсутствии терапии до 50% при использовании видарабина и 61% при использовании ацикловира SD, в то время как смертность за 1 год от заболевания ЦНС снизилась с 35% без лечения до 14% как для видарабина, так и для ацикловира SD [11]. Совсем недавно было показано, что ацикловир в высоких дозах (HD) дополнительно улучшает эти показатели смертности. При внутривенном введении ацикловира на HD (60 мг / кг / день в 3 приема в течение 21 дня) летальность в течение одного года составила 29% и 4% от диссеминированных заболеваний и заболеваний ЦНС, соответственно [12].В то время как HD ацикловир снижал заболеваемость младенцев с диссеминированным заболеванием (83% выживших имели нормальные исходы нервного развития), у младенцев с заболеванием ЦНС не наблюдалось значительного улучшения заболеваемости (31% выживших имели нормальные исходы неврологического развития).
Младенцы с поражением SEM имеют наилучший прогноз и, как указано ниже, им требуется всего 14 дней внутривенной терапии ацикловиром на HD.
Недавно супрессивная терапия ацикловиром для младенцев с ЦНС после завершения внутривенного лечения значительно улучшила неврологический исход, измеренный по шкале Bailey Developmental Scores [13].Этот режим привел к тому, что примерно 60% (по сравнению с 31%) детей с заболеванием ЦНС развились нормально или с легкими нарушениями. Лечение проводилось в дозе 300 / мг / м 2 в сутки в течение шести месяцев.
Терапия неонатальных инфекций, вызванных вирусом ветряной оспы
Женщины, перенесшие первичную инфекцию вируса ветряной оспы (VZV) в течение 48 часов после родов, имеют детей с риском развития ветряной оспы в течение первых трех недель жизни. Новорожденным этим женщинам традиционно вводят иммуноглобулин против опоясывающего лишая (ZIG), чтобы предотвратить заболевание.Однако при спорадической нехватке ZIG у некоторых новорожденных могут развиться неонатальные заболевания. Никакие контролируемые клинические испытания не оценивали терапию этого заболевания ацикловиром; однако специалисты рекомендуют этот препарат для лечения болезней новорожденных.
Доступные методы лечения инфекций HSV и VZV
Ацикловир (Ациклогуанозин, Зовиракс, ACV)
Ацикловир является наиболее часто назначаемым противовирусным средством для лечения инфекций HSV новорожденных и младенцев.Он был доступен для клинического использования в течение почти трех десятилетий и продемонстрировал замечательную безопасность и эффективность против легких и тяжелых инфекций, вызванных HSV и VZV, как у здоровых пациентов, так и у пациентов с ослабленным иммунитетом, включая новорожденных.
Химия и механизм действия
Ацикловир — аналог дезоксигуанозина. После преимущественного поглощения инфицированными вирусом клетками ацикловир фосфорилируется кодируемой вирусом тимидинкиназой (ТК). Последующее ди- и трифосфорилирование катализируется ферментами клетки-хозяина.Ацикловиртрифосфат предотвращает синтез вирусной ДНК как за счет ингибирования вирусной ДНК-полимеразы, так и за счет того, что он является терминатором цепи.
Спектр и устойчивость
Ацикловир наиболее активен против ВПГ; активность против VZV также значительна, но примерно в 10 раз меньше. Ацикловир считается препаратом выбора как при неонатальных инфекциях HSV, так и при VZV-инфекциях. Активность против ЦМВ низкая, поскольку ЦМВ не обладает активностью тимидинкиназы, а ДНК-полимераза ЦМВ слабо ингибируется ацикловиртрифосфатом.
Устойчивость HSV и VZV к ацикловиру стала важной клинической проблемой среди пациентов с ослабленным иммунитетом, получающих длительную терапию [14]. Устойчивость вирусов к ацикловиру обычно является результатом мутаций в вирусном гене TK, хотя мутации в гене вирусной ДНК-полимеразы также встречаются редко. Резистентные изоляты могут вызывать тяжелые, прогрессирующие, изнурительные заболевания слизистых оболочек у взрослых и, в редких случаях, висцеральное распространение [15, 16]. Изоляты HSV, устойчивые к ацикловиру, также были зарегистрированы у здоровых хозяев, чаще всего у пациентов с часто рецидивирующими генитальными инфекциями, которые лечились хроническим ацикловиром [17].
Показания к применению
Ацикловир эффективен для лечения инфекций, вызванных HSV и VZV, у иммунокомпетентных и иммунодефицитных хозяев, включая новорожденных. Для лечения неонатальных инфекций HSV рекомендуемая доза составляет 20 мг / кг / каждые 8 часов. Продолжительность терапии SEM-заболевания составляет 14 дней, в то время как для детей с ЦНС или диссеминированным заболеванием терапию следует продлить на 21 день.
Ацикловир для перорального применения — это экспериментальный подход к супрессивной терапии, который в настоящее время не одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов.
Фармакокинетика
После внутривенных доз от 2,5 до 15 мг / кг стационарные концентрации ацикловира колеблются от 6,7 до 20,6 мкг / мл. Ацикловир широко распространен; высокие концентрации достигаются в почках, легких, печени, сердце и кожных пузырьках; концентрации в спинномозговой жидкости (CSF) составляют около 50% от концентрации в плазме [18]. Ацикловир проникает через плаценту и накапливается в грудном молоке. Связывание с белками составляет от 9% до 33%, и менее 20% препарата метаболизируется до биологически неактивных метаболитов.Фармакокинетические данные для новорожденных при применении 20 мг / кг / доза отсутствуют.
При отсутствии нарушения функции почек период полувыведения ацикловира составляет от 2 до 3 часов у детей старшего возраста и взрослых и от 2,5 до 5 часов у новорожденных с нормальным клиренсом креатинина. Более 60% введенного препарата выводится с мочой [18]. Выведение продлевается у пациентов с нарушением функции почек; Период полувыведения составляет приблизительно 20 часов у лиц с терминальной стадией почечной недостаточности, что требует изменения дозы для пациентов с клиренсом креатинина менее 50 мл / мин / л.73 м 2 [19]. Ацикловир эффективно удаляется гемодиализом, но не постоянным амбулаторным перитонеальным диализом [20, 21].
Побочные эффекты
Ацикловир, как правило, является безопасным лекарством. Почечная дисфункция возникает в результате обструктивной нефропатии, вызванной образованием кристаллов ацикловира, осаждающихся в почечных канальцах. Иногда внутривенное введение ацикловира вызывает сыпь, потливость, тошноту, головную боль, гематурию и гипотонию. Высокие дозы ацикловира внутривенно (60 мг / кг / день) новорожденным были связаны с нейтропенией [22, 23].
Нейротоксичность может возникать у субъектов с нарушенной функцией почек, которые достигают высоких концентраций препарата в сыворотке [24]. Нейротоксичность проявляется в виде летаргии, спутанности сознания, галлюцинаций, тремора, миоклонуса, судорог, экстрапирамидных признаков и изменений состояния сознания, развивающихся в течение первых нескольких дней после начала терапии. Эти признаки и симптомы обычно проходят спонтанно в течение нескольких дней после прекращения приема ацикловира.
Хотя ацикловир обладает мутагенным действием при высоких концентрациях в некоторых анализах in vitro , он не обладает тератогенным действием на животных.Ограниченные данные о людях позволяют предположить, что использование ацикловира беременными женщинами не связано с врожденными дефектами или другими неблагоприятными исходами беременности.
Лекарственные взаимодействия
Вероятность почечной токсичности ацикловира увеличивается при приеме нефротоксических препаратов, таких как циклоспорин или амфотерицин B.
Терапия врожденной цитомегаловирусной инфекции
Цитомегаловирус (ЦМВ) обычно заражает людей во всем мире серозной инфекцией. 40% у подростков и приближается к 90% у взрослых с плохим социально-экономическим статусом [25, 26].Врожденная ЦМВ-инфекция — наиболее распространенная врожденная инфекция в развитых странах, обнаруживаемая примерно у 1% живорожденных младенцев в Соединенных Штатах [27]. Врожденные ЦМВ-инфекции чаще всего возникают при внутриутробной передаче, но, поскольку вирус распространяется с жидкостями организма, передача также может передаваться перинатально во время родов или постнатально через грудное молоко.
Из всех младенцев, рожденных с врожденной ЦМВ-инфекцией, примерно 7–10% имеют клинически очевидное заболевание при рождении [28].Клинические характеристики внутриутробной инфекции включают ограничение внутриутробного развития, гепатоспленомегалию, желтуху, тромбоцитопению, микроцефалию, перивентрикулярные кальцификации и хориоретинит. Согласно обзору Dollard, истинные показатели смертности трудно получить, и, как сообщается, они достигают 30% для младенцев с симптомами [29], но, скорее всего, в среднем составляют около 5–10% [30]. Смерть обычно происходит из-за проявлений инфекции, не связанных с ЦНС, таких как нарушение функции печени или кровотечение. По оценкам, 40–58% младенцев с симптоматической врожденной ЦМВ-инфекцией имеют необратимые последствия, в то время как младенцы, у которых нет симптомов при рождении, страдают постоянными последствиями почти в 14% случаев [29].Сенсорно-невральная потеря слуха (СНСС), умственная отсталость, судороги, задержка психомоторной и речевой активности, нарушение обучаемости, хориоретинит, атрофия зрительного нерва и дефекты зубных рядов являются наиболее частыми долгосрочными последствиями [31]. В отличие от внутриутробных инфекций, перинатально приобретенные ЦМВ-инфекции обычно не связаны с долгосрочными последствиями, хотя сообщалось об острых заболеваниях у недоношенных детей с очень низкой массой тела при рождении [32]. У доношенных детей перинатальные инфекции обычно протекают бессимптомно, но могут проявляться пневмонитом в течение первых нескольких месяцев жизни [33].
Врожденная ЦМВ-инфекция является следствием инфицирования матери и плода, причем большинство симптоматических врожденных случаев возникает из-за бессимптомной материнской инфекции. При материнской первичной инфекции, по-видимому, происходит нарушение плацентарного кровотока после инфицирования плацентарных вилок [34]. Патогенез поражения ЦНС при врожденной ЦМВ-инфекции начинается с диссеминированного распространения виремии, включая эндотелиальные клетки головного мозга и эпителиальные клетки сосудистого сплетения.Из эндотелиальных клеток головного мозга вирус распространяется на смежные астроциты. Из сосудистого сплетения вирус затем перемещается к эпендимным поверхностям через спинномозговую жидкость (CSF). После инфицирования этих клеток вирус подвергается непрерывной репликации, что приводит к характерным внутриядерным тельцам включения и гибели клеток. Поскольку антитела вырабатываются в условиях непрерывной репликации вируса, также образуются иммунные комплексы, что приводит к дальнейшему иммуноопосредованному повреждению [31]. Хотя специфический патогенез SNHL, опосредованного CMV, не выяснен, гистология показала доказательства инфекции в клетках как улиткового, так и вестибулярного эндолабиринта [35].ЦМВ также был выделен из перилимфы улитки при вскрытии новорожденных с врожденной ЦМВ-инфекцией [36].
Недавние исследования лечения ганцикловиром врожденных ЦМВ-инфекций с поражением ЦНС были многообещающими. Введение ганцикловира в дозах 12 мг / кг / день, разделенных каждые 12 часов в течение 6 недель, улучшило исходы слуха у новорожденных с симптоматической врожденной ЦМВ-инфекцией с поражением ЦНС (о чем свидетельствуют микроцефалия, внутричерепные кальцификации, аномалии спинномозговой жидкости для возраста, хориоретинит и др.) / или нарушения слуха) [37].Первичной конечной точкой был улучшенный ответ, вызванный стволом мозга (BSER) между исходным уровнем и 6-месячным периодом наблюдения (или отсутствие ухудшения в течение 6-месячного последующего наблюдения, если исходный BSER был нормальным). Что касается общего количества ушей, подлежащих оценке, 69% пациентов, получавших ганцикловир, достигли первичной конечной точки по сравнению с 39% в контрольной группе. Ни у одного пациента, получавшего ганцикловир, не было ухудшения слуха от исходного уровня до 6 месяцев. У реципиентов ганцикловира также отмечалось более быстрое разрешение нарушений АЛТ, чем в контрольной группе, хотя вероятность развития нейтропении у них была значительно выше.Дополнительный анализ этого рандомизированного контролируемого исследования позволяет предположить, что ганцикловир может также уменьшать задержки в развитии нервной системы [38]. Улучшение смертности при терапии ганцикловиром пока не показано.
Лечение ЦМВ-инфекций
Ганцикловир (Цитовен)
Ганцикловир был первым противовирусным препаратом, доступным для лечения и профилактики инфекций, вызванных ЦМВ. Доказано, что это очень ценный препарат для пациентов с ослабленным иммунитетом, особенно для пациентов с рецептами трансплантации гемопоэтических стволовых клеток, которые страдают от значительной заболеваемости и смертности от ЦМВ-инфекций, а в последнее время — для детей с врожденной ЦМВ-инфекцией, хотя и не одобрено Управлением по контролю за продуктами и лекарствами США Администрация (FDA) в настоящее время.
Химия и механизм действия
Ганцикловир структурно похож на ацикловир, за исключением гидроксиметильной группы на его ациклической боковой цепи. Первоначальный этап фосфорилирования осуществляется pUL97, вирусной протеинкиназой. Затем клеточные киназы фосфорилируют агент еще два раза, чтобы преобразовать его в его трифосфатное производное, которое способно ингибировать ДНК-полимеразу ЦМВ, кодируемую UL97 , а также встраиваться в вирусную ДНК и обрывать ее.
Ганцикловир трифосфат — конкурентный ингибитор герпесвирусных ДНК-полимераз, приводящий к прекращению удлинения цепи ДНК [1, 20].
Спектр и устойчивость
Ганцикловир имеет сходную с ацикловиром активность против HSV-1, HSV-2 и VZV, но, в отличие от ацикловира, его наибольшая активность против CMV. Устойчивость изолятов ЦМВ обычно возникает в результате мутаций в гене UL97 [39]. Мутации в гене ДНК-полимеразы ЦМВ встречаются реже. Показания .Ганцикловир лицензирован для нескольких показаний за пределами новорожденных. В нескольких обзорах резюмируются эти клинические исходы [2]. Для лечения новорожденных, врожденно инфицированных ЦМВ, было проведено контролируемое исследование [40]. Как отмечалось выше, по сравнению с отсутствием лечения, терапия ганцикловиром предотвращала ухудшение слуха через два года, хотя примерно у двух третей пролеченных младенцев развилась нейтропения, часто требующая изменения дозы.
Фармакокинетика
Пероральная биодоступность ганцикловира низкая, при пероральном приеме всасывается менее 10% препарата [41, 42].Пероральный препарат ганцикловира больше не продается. Пиковые концентрации ганцикловира в сыворотке крови после введения 6 мг / кг (доза для новорожденных) внутривенно вводимого лекарственного средства колеблются от 8 до 11 мкг / мл с концентрациями, достаточными для подавления чувствительных штаммов ЦМВ в водянистой влаге, субретинальной жидкости, спинномозговой жидкости и ткани мозга [ 1]. Период полувыведения ганцикловира составляет от 2 до 3 часов, и большая часть препарата выводится в неизмененном виде с мочой. Фармакокинетика ганцикловира в популяции новорожденных аналогична таковой у взрослых [43, 44].Снижение дозы, пропорциональное степени снижения клиренса креатинина, необходимо лицам с нарушением функции почек. Дополнительная доза рекомендуется после диализа, поскольку она эффективно удаляется гемодиализом [45].
Побочные эффекты
Миелосупрессия — наиболее частое побочное действие ганцикловира; Дозозависимая нейтропения (менее 1000 лейкоцитов / мкл) является наиболее стойким гематологическим отклонением с частотой около 40% [42]. Нейтропения ограничивает дозу примерно в одном из семи курсов и исчезает после прекращения приема препарата.При пероральном приеме ганцикловира нейтропения возникает реже. Тромбоцитопения (менее 50 000 тромбоцитов / мкл) встречается примерно у 20%, а анемия — примерно у 2% реципиентов ганцикловира. От 2 до 5% реципиентов ганцикловира испытывают головную боль, спутанность сознания, изменение психического статуса, галлюцинации, кошмары, беспокойство, атаксию, тремор, судороги. лихорадка, сыпь и аномальные уровни сывороточных печеночных ферментов по отдельности или в некоторой комбинации.
Дозировка
Доза ганцикловира для лечения симптоматической врожденной ЦМВ-инфекции составляет 12 мг / кг / день внутривенно дважды в день в течение 6 недель.
Исследуемый препарат
Валганцикловир (Valcyte)
Валганцикловир был одобрен FDA в марте 2001 г. для лечения ЦМВ-ретинита. Поскольку он хорошо всасывается после перорального приема, он может представлять собой благоприятный вариант по сравнению с внутривенным введением ганцикловира для лечения врожденной ЦМВ-инфекции. В настоящее время он лицензирован для лечения ЦМВ-инфекций в отдельных популяциях трансплантатов и ЦМВ-ретинита у пациентов с ВИЧ / СПИДом.
Химия, механизм действия, спектр и устойчивость
Валганцикловир является пролекарством ганцикловира на основе эфира L-валина и, как таковой, имеет тот же механизм действия, противовирусный спектр и потенциал развития устойчивости, что и ганцикловир [1, 20] .
Показания
Валганцикловир имеет аналогичные показания к ганцикловиру. Однако, основываясь на опубликованных на сегодняшний день ограниченных контролируемых исследованиях, в настоящее время он одобрен для индукционной и поддерживающей терапии ЦМВ-ретинита и для отдельных популяций трансплантатов [46].В настоящее время изучается возможность лечения врожденной ЦМВ-инфекции. В этом рандомизированном контролируемом исследовании, проводимом Группой по совместным антивирусным исследованиям (CASG) Национального института аллергии и инфекционных заболеваний (NIAID), в качестве основной конечной точки используется SNHL.
Фармакокинетика
Валганцикловир быстро превращается в ганцикловир со средним периодом полувыведения из плазмы около 30 минут [46]. Абсолютная биодоступность валганцикловира превышает 60% и фактически увеличивается примерно на 30% при одновременном приеме пищи [47].Площадь под кривой ганцикловира после перорального приема валганцикловира составляет от одной трети до половины площади, полученной после внутривенного введения ганцикловира. Пациентам с нарушением функции почек требуется снижение дозировки, примерно пропорциональное снижению клиренса креатинина.
Побочные эффекты
Наиболее частые побочные эффекты, связанные с терапией валганцикловиром у взрослых, включают диарею (41%), тошноту (30%), нейтропению (27%), анемию (26%) и головную боль (22%) [ 46].Лишь ограниченное число новорожденных получали терапию валганцикловиром. Единственным значимым открытием была нейтропения у 15% пациентов.
Дозировка
Доза валганцикловира зависит от возраста пациента и функции почек. В настоящее время препарат не разрешен к применению у новорожденных с врожденной ЦМВ-инфекцией.
Непроверенные и непроверенные методы лечения неонатальных инфекций HSV, VZV и врожденных ЦМВ-инфекций
Следующие два препарата используются для лечения инфекций HSV, VZV и CMV у детей старшего возраста и взрослых.Данные об этих препаратах предоставляются, если у новорожденных возникает резистентность к противовирусным препаратам при инфекциях ВПГ или ЦМВ. Ни один из препаратов не был оценен в рамках доказательных исследований на новорожденных, и оба связаны со значительной токсичностью. Кроме того, валацикловир может стать доступным для педиатрического применения, особенно для младенцев с инфекцией HSV, ограниченной кожей, глазами и ртом
Цидофовир (HPMPC, Vistide)
Цидофовир был впервые одобрен для использования в США для лечения СПИДа -ассоциированный ретинит, вызванный ЦМВ.Это остается основным показанием к применению этого противовирусного препарата.
Химия и механизм действия
Цидофовир представляет собой новый аналог ациклических фосфонатных нуклеозидов с механизмом действия, аналогичным другим аналогам нуклеозидов. В отличие от ацикловира, вирусные ферменты не требуются для начального фосфорилирования, поскольку нативный цидофовир уже имеет одну присоединенную фосфатную группу. После дифосфорализации клеточными киназами цидофовир конкурентно ингибирует ДНК-полимеразу [48].Активная форма цидофовира проявляет в 25-50 раз большее сродство к вирусной ДНК-полимеразе по сравнению с клеточной ДНК-полимеразой.
Спектр и устойчивость
Цидофовир активен против ВПГ и ЦМВ, включая устойчивые к ацикловиру и фоскарнету изоляты ВПГ и мутанты ЦМВ, устойчивые к ганцикловиру и фоскарнету [49]. Он также активен in vitro против VZV, EBV, вируса герпеса человека-6, вируса герпеса человека-8, полиомавирусов, аденовируса и ВПЧ человека.
Было описано небольшое количество устойчивых к цидофовиру изолятов ЦМВ, которые также устойчивы к ганцикловиру на основе мутаций в гене ДНК-полимеразы [50].Сообщалось также о мутанте ЦМВ, устойчивом к ганцикловиру, фоскарнету и цидофовиру [51].
Показания к применению
Цидофовир замедляет прогрессирование заболевания сетчатки у пациентов со СПИДом [52, 53]. Цидофовир также был полезен при лечении заболеваний, вызванных устойчивыми к ацикловиру изолятами ВПГ [54]. Были опубликованы отдельные сообщения об улучшении папилломатоза гортани после инъекции цидофовира в очаг поражения, но на основании этого ограниченного опыта невозможно сделать окончательные выводы об эффективности [55, 56].
Фармакокинетика
Только 2–26% цидофовира всасывается после перорального приема, поэтому его вводят внутривенно. Период полувыведения цидофовира из плазмы составляет 2,6 часа, но период полураспада активных внутриклеточных метаболитов цидофовира составляет от 17 до 48 часов [ 57]. Девяносто процентов препарата выводится с мочой, в основном с секрецией почечных канальцев [58]. Важно отметить, что препарат не проникает через гематоэнцефалический барьер и, следовательно, не должен использоваться для лечения инфекций ЦНС.
Побочные эффекты
Поскольку цидофовир концентрируется в почечных клетках в количествах в 100 раз больше, чем в других тканях, нефротоксичность является основным побочным эффектом, особенно если гидратация не поддерживается должным образом [57, 58].Проявления почечной токсичности включают протеинурию и глюкозурию. Агрессивная внутривенная прегидратация, одновременное введение пробенецида и отказ от других нефротоксичных агентов снижают вероятность токсичности. Цидофовир противопоказан пациентам с креатинином сыворотки> 1,5 мг / дл, расчетным клиренсом креатинина ≤ 55 мл / мин или белком в моче ≥ 100 мг / дл, и препарат следует прекратить, если креатинин сыворотки повышается на ≥ 0,5 мг / дл выше исходного уровня. .
Дозировка
Цидофовир вводят внутривенно детям старшего возраста и взрослым в дозе 5 мг / кг один раз в неделю с пробенецидом.Пациенты с нарушением функции почек (расчетный клиренс креатинина <55 мл / мин) проходят лечение каждые 2 недели. Дозу следует уменьшить с 5 мг / кг до 3 мг / кг, если креатинин сыворотки повышается на> 0,3 мг / дл выше исходного уровня. Данных о дозировании цидофовира новорожденным нет.
Фоскарнет (PFA, Foscavir)
Фоскарнет — единственный противогерпетический препарат, не являющийся аналогом нуклеозидов. Это не препарат первой линии, но он полезен для лечения инфекций, вызванных устойчивыми вирусами герпеса.
Химия и механизм действия
Фоскарнет — неорганический аналог пирофосфата, который напрямую ингибирует ДНК-полимеразу, блокируя сайт связывания пирофосфата [20, 59].
Спектр и устойчивость
Фоскарнет ингибирует все известные герпесвирусы человека, включая большинство устойчивых к ганцикловиру изолятов ЦМВ и устойчивые к ацикловиру вирусы простого герпеса и вируса зодиака. Он также активен против ВИЧ. Устойчивость возникает в результате мутаций ДНК-полимеразы. Сообщалось о штаммах CMV, HSV и VZV с пониженной чувствительностью к фоскарнету [59, 60].
Показания к применению
Фоскарнет так же эффективен, как и ганцикловир, для лечения угрожающего зрению хориоретинита, вызванного ЦМВ, у взрослых пациентов со СПИДом [61]. Из-за присущей ему активности против ВИЧ, он может даже обеспечить преимущество в выживаемости для пролеченных пациентов [62]. Рефрактерные случаи хориоретинита могут поддаваться лечению комбинацией фоскарнета и ганцикловира. Фоскарнет также эффективен при терапии ЦМВ-инфекций, вызванных ганцикловир-резистентными штаммами вируса [62]. Ограниченные данные также предполагают, что фоскарнет может быть полезным при назначении пациентам со СПИДом, у которых есть желудочно-кишечные и легочные инфекции, вызванные ЦМВ.
Инфекции, вызванные устойчивыми к ацикловиру штаммами HSV и VZV, успешно контролируются с помощью фоскарнета [63, 64].
Фармакокинетика
Только около 20% фоскарнета абсорбируется после перорального приема. Максимальная концентрация в сыворотке, достигаемая после внутривенного введения 60 мг / кг, составляет примерно 500 мкмоль / л [59]. Концентрация в спинномозговой жидкости составляет около двух третей от концентрации в сыворотке. Период полувыведения фоскарнета составляет около 48 часов, и 80% введенной дозы выводится в неизмененном виде с мочой.Необходимо снижение дозы пропорционально уменьшению клиренса креатинина. Гемодиализ эффективно устраняет фоскарнет, поэтому после диализа рекомендуется дополнительная доза [65]. Данных о применении фоскарнета новорожденным нет.
Побочные эффекты
Наиболее частыми побочными эффектами фоскарнета являются нефротоксичность и метаболические нарушения. Доказательства нефротоксичности включают азотемию, протеинурию, острый тубулярный некроз, кристаллурию и интерстициальный нефрит.Концентрация креатинина в сыворотке увеличивается до 50% пациентов. К счастью, функция почек приходит в норму в течение 2–4 недель после прекращения терапии. Существующее ранее заболевание почек, одновременный прием других нефротоксических препаратов, обезвоживание, быстрое введение или непрерывное внутривенное вливание препарата являются факторами риска развития почечной дисфункции [66]. Метаболические нарушения, связанные с терапией фоскарнетом, включают гипо- и гиперкальциемию, а также гипо- и гиперфосфатемию [67]. Гипокальциемия может быть связана с парестезиями, тетанией, судорогами и аритмиями.Метаболические нарушения сводятся к минимуму, если вводить фоскарнет медленной инфузией. Симптомы со стороны ЦНС, связанные с терапией фоскарнетом, включают головную боль, тремор, раздражительность, судороги и галлюцинации. Сообщалось также о лихорадке, тошноте, рвоте, аномальных ферментах сыворотки крови, анемии, гранулоцитопении и генитальных изъязвлениях.
Лекарственные взаимодействия
Одновременное применение амфотерицина B, циклоспорина, гентамицина и других нефротоксических препаратов увеличивает вероятность нарушения функции почек.Одновременный прием пентамидина увеличивает риск гипокальциемии. Анемия и нейтропения чаще встречаются, когда пациенты также получают зидовудин.
Дозировка
Обычная доза фоскарнета при ЦМВ-инфекции составляет 180 мг / кг / день в три приема в течение 14–21 дня, после чего следует ежедневная поддерживающая доза от 90 до 120 мг / кг. Дозировка фоскарнета, используемого при инфекциях, вызванных устойчивыми к ацикловиру HSV и VZV, составляет 120 мг / кг / день в три приема.
Резюме
Несмотря на то, что в лечении врожденных ЦМВ и неонатальных инфекций ВПГ достигнут значительный прогресс, дальнейшие достижения являются обязательными.С появлением новых противовирусных препаратов, обладающих другим механизмом действия, появляется возможность для комбинированной терапии, если можно доказать, что лекарства безопасны.
Выражение признательности
Этот проект полностью или частично финансируется за счет федеральных средств Национального института аллергии и инфекционных заболеваний, Национальных институтов здравоохранения, Министерства здравоохранения и социальных служб по контракту № N01-AI-30025.
Сноски
Заявление издателя: Это PDF-файл неотредактированной рукописи, принятой к публикации.В качестве услуги для наших клиентов мы предоставляем эту раннюю версию рукописи. Рукопись будет подвергнута копированию, верстке и рассмотрению полученного доказательства, прежде чем она будет опубликована в окончательной форме для цитирования. Обратите внимание, что во время производственного процесса могут быть обнаружены ошибки, которые могут повлиять на содержание, и все юридические оговорки, относящиеся к журналу, имеют отношение.
Ссылки
1. Кимберлин Д. Противовирусные агенты. В: Лонг С., Пикеринг Л., Пробер С., редакторы. Принципы и практика детских инфекционных болезней.3-е изд. Нью-Йорк: Эльзевир; 2008. С. 1470–1488. [Google Scholar] 2. Ра Б., Кимберлин Д. В., Уитли Р. Противовирусные препараты. В: Джером К., редактор. Лабораторная диагностика вирусных инфекций. 3-е изд. Нью-Йорк: Informa Healthcare; 2009. [Google Scholar] 3. Brown ZA, Wald A, Morrow RA, Selke S, Zeh J, Corey L. Влияние серологического статуса и кесарева сечения на скорость передачи вируса простого герпеса от матери к ребенку. ДЖАМА. 2003. 289 (2): 203–209. [PubMed] [Google Scholar] 4. Уитли Р.Дж. Вирус простого герпеса.В: Scheld MW, Whitley RJ, Marra CM, редакторы. Инфекции центральной нервной системы. 3-е изд. Филадельфия: Липпинкотт Уильямс и Уилкинс; 2004. С. 123–144. [Google Scholar] 5. Kimberlin DW, Lin CY, Jacobs RF, Powell DA, Frenkel LM, Gruber WC, et al. Естественная история инфекций, вызванных вирусом простого герпеса новорожденных, в эпоху ацикловира. Педиатрия. 2001. 108 (2): 223–229. [PubMed] [Google Scholar] 6. Kimberlin DW. Ведение энцефалита, вызванного вирусом простого герпеса, у взрослых и новорожденных: диагностика, прогноз и лечение.Герпес. 2007 июн; 14 (1): 11–16. [PubMed] [Google Scholar] 7. Хатто С., Арвин А., Джейкобс Р., Стил Р., Стагно С., Лайрин Р. и др. Внутриутробные инфекции, вызванные вирусом простого герпеса. Журнал педиатрии. 1987. 110 (1): 97–101. [PubMed] [Google Scholar] 8. Уитли Р.Дж. Инфекции, вызванные вирусом простого герпеса. В: Remington JS, Klein JO, редакторы. Инфекционные болезни плода и новорожденных. 3-е изд. Филадельфия: W.B. Компания Сондерс; 1990. С. 282–305. [Google Scholar] 9. Уитли Р.Дж., Кори Л., Арвин А., Лейкман Ф.Д., Сумая К.В., Райт П.Ф. и др.Изменение представления инфекции вируса простого герпеса у новорожденных. Журнал инфекционных болезней. 1988. 158 (1): 109–116. [PubMed] [Google Scholar] 10. Уитли Р.Дж., Ройзман Б. Вирусы простого герпеса. В: Ричман Д.Д., Уитли Р.Дж., Хайден Ф.Г., редакторы. Клиническая вирусология. 2-е изд. Вашингтон, округ Колумбия: ASM Press; 2004. С. 375–401. [Google Scholar] 11. Уитли Р., Арвин А., Пробер С., Берчетт С., Кори Л., Пауэлл Д. и др. Контролируемое испытание по сравнению видарабина с ацикловиром при неонатальной инфекции вирусом простого герпеса.Медицинский журнал Новой Англии. 1991. 324 (7): 444–449. [PubMed] [Google Scholar] 12. Kimberlin DW, Lin CY, Jacobs RF, Powell DA, Corey L, Gruber WC, et al. Безопасность и эффективность высоких доз внутривенного ацикловира при лечении инфекций, вызванных вирусом простого герпеса у новорожденных. Педиатрия. 2001. 108 (2): 230–238. [PubMed] [Google Scholar] 13. Кимберлин Д., Уитли Р., Ван В., Пауэлл Д., Сторч Г., Ахмед А. и др. Влияние перорального подавления ацикловира на исходы развития нервной системы и рецидивы кожи после болезни, вызванной вирусом простого герпеса новорожденных.NEJM. 2011 В печати. [Google Scholar] 14. Englund JA, Zimmerman ME, Swierkosz EU, Goodman JL, Scholl D, Balfour HH. Вирус простого герпеса устойчив к ацикловиру. Исследование в центре высокоспециализированной медицинской помощи. Ann Intern Med. 1990; 112: 416–422. [PubMed] [Google Scholar] 15. Полевой АК, Бирон К.К. Возвращение к «концу невинности»: устойчивость герпесвирусов к противовирусным препаратам. Clin Microbiol Rev.1994, январь; 7 (1): 1–13. [Бесплатная статья PMC] [PubMed] [Google Scholar] 16. Лайалл Э.Г., Огилви М.М., Смит Н.М., Бернс С. Устойчивость к ацикловиру ветряной оспы и ВИЧ-инфекция.Arch Dis Child. 1994 Февраль; 70 (2): 133–135. [Бесплатная статья PMC] [PubMed] [Google Scholar] 17. Морфин Ф, Тувено Д. Устойчивость вируса простого герпеса к противовирусным препаратам. J Clin Virol. 2003 Янв; 26 (1): 29–37. [PubMed] [Google Scholar] 18. Wagstaff AJ, Faulds D, Goa Kl. Ацикловир. Переоценка его противовирусной активности, фармакокинетических свойств и терапевтической эффективности. Наркотики. 1994; 47: 153–205. [PubMed] [Google Scholar] 19. Ласкин О.Л., Лонгстрет Дж. А., Велтон А., Красный Х. С., Кини Р. Э., Рокко Л. и др. Влияние почечной недостаточности на фармакокинетику ацикловира.Am J Med. 20 июля 1982 г .; 73 (1A): 197–201. [PubMed] [Google Scholar] 20. Инь М., Браст Дж., Тиеу Х., Хаммер С. Антигепатитные и антиреспираторные вирусные агенты. В: Ричман Д., Уитли Р., Хайден Ф., редакторы. Клиническая вирусология. Вашингтон, округ Колумбия: ASM Press; 2009. С. 217–264. [Google Scholar] 21. Красный ХК, Ляо С.Х., де Миранда П., Ласкин О.Л., Велтон А., Литман П.С. Влияние гемодиализа на фармакокинетику ацикловира у пациентов с хронической почечной недостаточностью. Am J Med. 20 июля 1982 г.; 73 (1A): 202–204. [PubMed] [Google Scholar] 22.Кимберлин Д., Пауэлл Д., Грубер В., Диаз П., Арвин А., Кумар М. и др. Назначение пероральной супрессивной терапии ацикловиром после неонатального заболевания, вызванного вирусом простого герпеса, ограниченным поражением кожи, глаз и рта: результаты тиража фазы I / II. Pediatr Infect Dis J. 1996; 15: 247–254. [PubMed] [Google Scholar] 23. Kimberlin DW, Lin CY, Jacobs RF, Powell DA, Corey L, Gruber WC, et al. Безопасность и эффективность высоких доз внутривенного ацикловира при лечении инфекций, вызванных вирусом простого герпеса у новорожденных. Педиатрия.2001 август; 108 (2): 230–238. [PubMed] [Google Scholar] 24. Реванкар С.Г., Эпплгейт А.Л., Марковиц Д.М. Делирий, связанный с лечением ацикловиром у пациента с почечной недостаточностью. Clin Infect Dis. 1995 августа; 21 (2): 435–436. [PubMed] [Google Scholar] 25. Гриффитс П.Д., Эмери В.К. Цитомегаловирус. В: Ричман Д.Д., Уитли Р.Дж., Хайден Ф.Г., редакторы. Клиническая вирусология. 2-е изд. Вашингтон, округ Колумбия: ASM Press; 2002. С. 433–461. [Google Scholar] 26. Старас С.А., Доллард СК, Рэдфорд К.В., Фландрия В.Д., Пасс РФ, Кэннон М.Дж. Распространенность цитомегаловирусной инфекции в США: 1988–1994 гг.Clin Infect Dis. 2006 г., 1 ноября; 43 (9): 1143–1151. [PubMed] [Google Scholar] 27. Demmler GJ. Американское общество инфекционных болезней и Центры по контролю за заболеваниями. Резюме семинара по надзору за врожденным цитомегаловирусным заболеванием. Обзоры инфекционных болезней. 1991. 13 (2): 315–329. [PubMed] [Google Scholar] 28. Conboy TJ, Pass RF, Stagno S, Alford CA, Myers GJ, Britt WJ и др. Ранние клинические проявления и интеллектуальный исход у детей с симптоматической врожденной цитомегаловирусной инфекцией.Журнал педиатрии. 1987. 111 (3): 343–348. [PubMed] [Google Scholar] 29. Доллард СК, Гросс С.Д., Росс Д.С. Новые оценки распространенности неврологических и сенсорных последствий и смертности, связанных с врожденной цитомегаловирусной инфекцией. Rev Med Virol. 1 июня 2007 г .; [PubMed] [Google Scholar] 30. Росс С.А., Боппана С.Б. Врожденная цитомегаловирусная инфекция: исход и диагноз. Semin Pediatr Infect Dis. 2005 Янв; 16 (1): 44–49. [PubMed] [Google Scholar] 31. Гриффитс PD, Маклафлин JE. Цитомегаловирус.В: Scheld WM, Whitley RJ, Marra CM, редакторы. Инфекции центральной нервной системы. Филадельфия: Липпинкотт Уильямс и Уилкинс; 2004. С. 159–173. [Google Scholar] 32. Машманн Дж., Хампрехт К., Дитц К., Ян Дж., Шпеер С.П. Цитомегаловирусная инфекция младенцев с крайне низкой массой тела при рождении через грудное молоко. Клинические инфекционные болезни. 2001; 33 (12): 1998–2003. [PubMed] [Google Scholar] 33. Brasfield DM, Stagno S, Whitley RJ, Cloud G, Cassell G, Tiller RE. Детский пневмонит, связанный с цитомегаловирусом, хламидиозом, пневмоцистом и уреаплазмой.Педиатрия. 1987. 79: 76–83. [PubMed] [Google Scholar] 34. Перейра Л., Майджи Э. Цитомегаловирусная инфекция в плаценте человека: материнский иммунитет и рецепторы, регулируемые развитием трофобластов, сходятся. Актуальные темы микробиологии и иммунологии. 2008. 325: 383–395. [PubMed] [Google Scholar] 35. Штраус М. Цитомегаловирусный лабиринтит человека. Am J Otolaryngol. Сентябрь – октябрь 1990 г., 11 (5): 292–298. [PubMed] [Google Scholar] 36. Дэвис Л. Е., Джонссон Л. Г., Корнфельд М. Цитомегаловирусный лабиринтит у младенцев: морфологические, вирусологические и иммунофлуоресцентные исследования.J Neuropathol Exp Neurol. 1981, январь; 40 (1): 9–19. [PubMed] [Google Scholar] 37. Kimberlin DW, Lin CY, Sanchez PJ, Demmler GJ, Dankner W, Shelton M и др. Влияние терапии ганцикловиром на слух при симптоматическом врожденном цитомегаловирусном заболевании с поражением центральной нервной системы: рандомизированное контролируемое исследование. Журнал педиатрии. 2003. 143 (1): 16–25. [PubMed] [Google Scholar] 38. Оливер С., Клауд Дж., Санчес П., Деммлер Дж., Данкнер В., Шелтон М. и др. Влияние терапии ганцикловиром (GCV) на исходы нервного развития при симптоматических врожденных цитомегаловирусных (CMV) инфекциях с поражением центральной нервной системы (ЦНС): рандомизированное контролируемое исследование.Ежегодное собрание Общества педиатрических исследований (SPR); 2006 29 апреля; Сан-Франциско, Калифорния. 2006. с. Реферат № 752908. [Google Scholar] 39. Маркхэм А., Фолдс Д. Ганцикловир: обновление его терапевтического использования при цитомегаловирусной инфекции. Наркотики. 1994; 48: 455. [PubMed] [Google Scholar] 40. Kimberlin DW, Lin C-Y, Sanchez PJ, Demmler GJ, Dankner W, Shelton MD, et al. Влияние ганцикловира на слух при симптоматическом врожденном цитомегаловирусном заболевании с поражением центральной нервной системы: рандомизированное контролируемое исследование.J Pediatr. 2003. 143: 16–25. [PubMed] [Google Scholar] 41. Редди В., Хао Ю., Липтон Дж., Мехарчанд Дж., Минден М., Мацзулли Т. и др. Ведение реципиентов аллогенного трансплантата костного мозга с риском цитомегаловирусной болезни с использованием контрольной бронхоскопии и длительной упреждающей терапии ганцикловиром. J Clin Virol. 1999, август; 13 (3): 149–159. [PubMed] [Google Scholar] 42. Jacobson MA, Gambertoglio JG, Aweeka FT, Causey DM, Portale AA. Гипокальциемия, вызванная фоскарнетом, и влияние фоскарнета на метаболизм кальция.J Clin Endocrinol Metab. 1991 Май; 72 (5): 1130–1135. [PubMed] [Google Scholar] 43. Френкель Л.М., Каппарелли Е.В., Данкнер В.М., Сюй Дж., Смит И.Л., Баллоу А. и др. Ганцикловир для приема внутрь у детей: фармакокинетика, безопасность, переносимость и противовирусное действие. Группа педиатрических клинических испытаний СПИДа. Журнал инфекционных болезней. 2000 декабрь; 182 (6): 1616–1624. [PubMed] [Google Scholar] 44. Транг Дж. М., Кидд Л., Грубер В., Сторч Дж., Деммлер Дж., Джейкобс Р. и др. Линейная фармакокинетика однократной дозы ганцикловира у новорожденных с врожденными цитомегаловирусными инфекциями.Clin Pharmacol Ther. 1993; 53: 15–21. [PubMed] [Google Scholar] 45. Свон С.К., Мунар М.Ю., Виггер М.А., Беннетт В.М. Фармакокинетика ганцикловира у пациента, находящегося на гемодиализе. Am J Kidney Dis. 1991, январь; 17 (1): 69–72. [PubMed] [Google Scholar] 46. Cocohoba JM, McNicholl IR. Валганцикловир: прогресс в лечении цитомегаловирусов. Энн Фармакотер. 2002 июнь; 36 (6): 1075–1079. [PubMed] [Google Scholar] 47. Юнг Д., Дорр А. Фармакокинетика однократной дозы валганцикловира у ВИЧ- и ЦМВ-серопозитивных субъектов.J Clin Pharmacol. 1999, август; 39 (8): 800–804. [PubMed] [Google Scholar] 48. Хо Х.Т., Вудс К.Л., Бронсон Дж. Дж., Де Бок Х., Мартин Дж. К., Хичкок МД. Внутриклеточный метаболизм антигерпетических средств -1- {3-гидрокси-2- (фосфонилметокси) пропил} цитозин. Mol Pharmacol. 1992; 41: 197–202. [PubMed] [Google Scholar] 49. Сафрин С, Черрингтон Дж, Джаффе Х.С. Клиническое использование цидофовира. Rev Med Virol. 1997 сентябрь; 7 (3): 145–156. [PubMed] [Google Scholar] 50. Lurain N, Spafford LE, Thompson KD. Мутация в открытой рамке считывания UL97 штаммов цитомегаловируса человека, устойчивых к ганцикловиру.Журнал вирусологии. 1994b; 68: 4427–4431. [Бесплатная статья PMC] [PubMed] [Google Scholar] 51. Черрингтон Дж. М., Майнер Р., Аллен С. Дж. У. и др. Сенситивы клинических изолятов цитомегаловируса человека (HCMV) к цидофовиру. Восьмая международная конференция по противовирусным исследованиям; 1995 г. 23–28 апреля; Санта-Фе, Нью-Мексико. 1995. [Google Scholar] 52. Исследования глазных осложнений Группы исследований СПИДа в сотрудничестве с Группой клинических испытаний СПИДа. Цидофовир (HPMPC) для лечения цитомегаловирусного ретинита у пациентов со СПИДом: исследование HPMPC Peripheral Cytomegalovirus Retinitis Trial.Ann Intern Med. 1997. 126: 264–274. [PubMed] [Google Scholar] 53. Lalezari JP, Staagg RJ, Kuppermann BD, Holland GN, Kramer F, Ives DV, et al. Внутривенное введение цидофовира при периферическом цитомегаловирусном ретините у пациентов со СПИДом: рандомизированное контролируемое исследование. Ann Intern Med. 1997. 126: 257–263. [PubMed] [Google Scholar] 54. Лалезари Дж. П., Дрю В. Л., Глутцер Э., Майнер Д., Сафрин С., Оуэн В. Ф., младший и др. Лечение внутривенным (S) -1- [3-гидрокси-2- (фосфонилметокси) пропил) -цитозином ацикловир-резистентной кожно-слизистой инфекции вирусом простого герпеса у пациента со СПИДом.Журнал инфекционных болезней. 1994; 170: 570–572. [PubMed] [Google Scholar] 55. Кимберлин DW, Малис DJ. Рецидивирующий респираторный папилломатоз с юношеским началом: возможности успешной противовирусной терапии. Antiviral Res. 2000 Февраль; 45 (2): 83–93. [PubMed] [Google Scholar] 56. Прански С.М., Магит А.Е., Кернс Д.Б., Канг Д.Р., Дункан Н.О. Цидофовир внутриочаговый при рецидивирующем респираторном папилломатозе у детей. Arch Otolaryngol Head Neck Surg. 1999 Октябрь; 125 (10): 1143–1148. [PubMed] [Google Scholar] 57. Канди К.С., Петти Б.Г., Флаэрти Дж., Фишер П.Е., Полис М.А., Ваксман М. и др.Клиническая фармакокинетика цидофовира у пациентов, инфицированных вирусом иммунодефицита человека. Антимикробные агенты Chemother. 1995; 39: 1247–1252. [Бесплатная статья PMC] [PubMed] [Google Scholar] 58. Лалезари Дж. П., Дрю В. Л., Глутцер Э., Джеймс С., Майнер Д., Флаэрти Дж. И др. (S) -1 {3-гидрокси-2- (фосфонилметокси) пропил} цитозин (цидофовиир): результаты исследования фазы I / II нового противовирусного аналога нуцелотида. Журнал инфекционных болезней. 1995; 171: 788–796. [PubMed] [Google Scholar] 59. Wagstaff AJ, Bryson HM.Фоскарнет: переоценка его противовирусной активности, фармакокинетических свойств и терапевтического использования у пациентов с ослабленным иммунитетом и вирусной инфекцией. Наркотики. 1994; 48: 199–226. [PubMed] [Google Scholar] 60. Сафрин С., Кеммерли С., Плоткин Б., Смит Т., Вайсбах Н., Де Веранес Д. и др. Инфекция, вызванная устойчивым к фоскарнету вирусом простого герпеса, у больных СПИДом. Журнал инфекционных болезней. 1994; 169: 193–196. [PubMed] [Google Scholar] 61. Снок Р., Андрей Г., Джерард М., Сильверман А., Хеддерман А., Бальзарини Дж. И др.Успешное лечение прогрессирующей кожно-слизистой инфекции, вызванной устойчивым к ацикловиру и фоскарнету вирусом простого герпеса, с помощью (S) -1- (3-гидрокси-2-фосфонилметоксипропил) цитозина (HPMPC) Clin Infect Dis. 1994 Апрель; 18 (4): 570–578. [PubMed] [Google Scholar] 62. Якобсон М.А., Дрю В.Л., Фейнберг Дж., О’Доннелл Дж. Дж., Уитмор П.В., Майнер Р.Д. и др. Терапия фоскарнетом при ганцикловиррезистентном цитомегаловирусном ретините у больных СПИДом. Журнал инфекционных болезней. 1991; 163: 1348–1351. [PubMed] [Google Scholar] 63.Сафрин С., Бергер Т.Г., Гилсон И. Терапия фоскарнетом у пяти пациентов со СПИДом и инфекцией вируса ветряной оспы, устойчивой к ацикловиру. Ann Intern Med. 1991; 115: 19–21. [PubMed] [Google Scholar] 64. Исследования глазных осложнений исследовательской группы СПИДа. Смертность у пациентов с синдромом приобретенного иммунодефицита, получавших фоскарнет или ганцикловир от цитомегаловируса ретинита. N Engl J Med. 1992; 326: 213–220. [PubMed] [Google Scholar] 65. Сафрин С., Крампакер С., Чатис П., Дэвис Р., Хафнер Р., Раш Дж. И др.Контролируемое исследование по сравнению фоскарнета и видарабина при лечении ацикловир-резистентного кожно-слизистого простого герпеса при синдроме приобретенного иммунодефицита. N Engl J Med. 1991; 325: 551–555. [PubMed] [Google Scholar] 66. МакГрегор Р. Р., Грациани А. Л., Вайс Р., Грюнвальд Дж. Э., Гамбертольо Дж. Г.. Успешная терапия фоскарнетом при цитомегаловирусном ретините у пациента со СПИДом, находящегося на гемодиализе: обоснование эмпирического дозирования и мониторинга уровня в плазме. Журнал инфекционных болезней. 1991 Октябрь; 164 (4): 785–787.[PubMed] [Google Scholar] 67. Дерай Г., Мартинес Ф., Катлама С., Левальтье Б., Бофилс Н., Данис М. и др. Нефротоксичность фоскарнета: механизм, частота возникновения и профилактика. Am J Nephrol. 1989. 9 (4): 316–321. [PubMed] [Google Scholar]Использование противовирусных препаратов в период новорожденности
Clin Perinatol. Авторская рукопись; доступно в PMC 1 марта 2013 г.
Опубликован в окончательной редакции как:
PMCID: PMC32
NIHMSID: NIHMS351802
Ричард Дж.Whitley
Заслуженный профессор, стипендиат Леба в области педиатрии, профессор педиатрии, микробиологии, медицины и нейрохирургии, Университет Алабамы в Бирмингеме, Бирмингем, AL
Ричард Дж. Уитли, заслуженный профессор, стипендиат Леба в педиатрии, профессор педиатрии, Микробиология, медицина и нейрохирургия, Университет Алабамы в Бирмингеме, Бирмингем, Алабама;
Окончательная отредактированная версия этой статьи издателем доступна в Clin Perinatol. См. Другие статьи в PMC, в которых цитируется опубликованная статья.Введение
Парентеральная терапия вирусных инфекций новорожденных и младенцев стала реальностью с появлением видарабина (аденин арабинозида) для лечения инфекций, вызванных вирусом простого герпеса (ВПГ) у новорожденных в начале 1980-х годов. С тех пор ацикловир стал препаратом выбора для лечения неонатальных инфекций HSV, а также множества других герпесвирусных инфекций. Аналогичным образом было установлено, что ганцикловир полезен для лечения врожденных цитомегаловирусных (ЦМВ) инфекций, поражающих центральную нервную систему (ЦНС).В этой главе будут рассмотрены уроки, извлеченные из лечения неонатального ВПГ и врожденных ЦМВ-инфекций в связи с применением ацикловира и ганцикловира. Хотя естественная история этих заболеваний рассматривается в другом месте в этом тексте, краткое изложение будет предшествовать подробному обсуждению имеющихся установленных и альтернативных методов лечения. Отсылаем читателя к более обширным обзорам противовирусной терапии у детей и взрослых [1, 2].
Терапия инфекций, вызванных вирусом простого герпеса
Неонатальные инфекции ВПГ встречаются примерно у 1 из 3200 родов в США [3], и примерно у двух третей из них развивается какая-либо форма заболевания ЦНС [4].Большинство случаев вызвано ВПГ-2 [5]. Риск передачи увеличивается при первичной материнской инфекции в третьем триместре, составляет 30–50%, и может быть снижен путем кесарева сечения, если HSV был изолирован из шейки матки или наружных половых органов незадолго до родов [3]. Согласно обзору Кимберлина, 85% случаев неонатального ВПГ происходят из-за передачи в период беременности и родов, в то время как 10% происходят в результате послеродовой передачи, и только 5% связаны с передачей in utero [6].
Младенцы с внутриутробной инфекцией ВПГ характеризуются тремя кожными признаками (активные поражения, рубцы), неврологическими признаками (микроцефалия, гидранэнцефалия) и данными глаз (хориоретинит, микрофтальмия), присутствующими при рождении.Было обнаружено, что внутриутробная инфекция HSV возникает как при первичной, так и при рецидивирующей материнской HSV-инфекции [7], хотя риск повторной инфекции меньше.
Инфекция HSV, приобретенная в послеродовом или послеродовом периоде, может быть классифицирована как заболевание кожи, глаз и / или рта (SEM), заболевание ЦНС или диссеминированное заболевание. По определению, болезнь SEM не затрагивает ЦНС. Распространенное заболевание может поражать ЦНС (75% случаев) вместе с множеством других систем органов, включая печень, надпочечники, желудочно-кишечный тракт, кожу, глаза или рот [8].Заболевание ЦНС также может иметь компонент вовлечения SEM, но не затрагивает другие системы органов. Из всех младенцев с неонатальной инфекцией ВПГ около 33% имеют заболевание ЦНС, а около 25% имеют диссеминированное заболевание [9]. Таким образом, около 50% младенцев с неонатальной инфекцией ВПГ имеют заболевание ЦНС.
Патогенез поражения ЦНС при неонатальных инфекциях ВПГ различается в зависимости от того, является ли инфекция диссеминированной. Энцефалит, связанный с диссеминацией, происходит из-за гематогенного распространения, тогда как изолированный энцефалит или энцефалит, связанный только с вовлечением SEM, вероятно, возникает из-за ретроградного внутринейронального транспорта HSV [4].Это различие соответствует клиническим проявлениям диссеминированного заболевания по сравнению с заболеванием ЦНС в том смысле, что распространение диссеминированного заболевания через кровь проявляется раньше (в среднем от 9 до 11 дней жизни) и вызывает более диффузное поражение мозга с множественными участками геморрагического некроза, в то время как заболевание ЦНС происходящий через более медленный аксональный транспорт, проявляется позже (примерно от 16 до 17 дней жизни) и обычно вызывает более очаговое поражение ЦНС [10].
Ранняя эра противовирусной терапии неонатальной инфекции ВПГ была отмечена повышением смертности при внутривенном введении видарабина, а также при внутривенном введении стандартной дозы (SD) ацикловира (30 мг / кг / день в 3 приема).Годовая смертность от диссеминированного заболевания снизилась с 85% при отсутствии терапии до 50% при использовании видарабина и 61% при использовании ацикловира SD, в то время как смертность за 1 год от заболевания ЦНС снизилась с 35% без лечения до 14% как для видарабина, так и для ацикловира SD [11]. Совсем недавно было показано, что ацикловир в высоких дозах (HD) дополнительно улучшает эти показатели смертности. При внутривенном введении ацикловира на HD (60 мг / кг / день в 3 приема в течение 21 дня) летальность в течение одного года составила 29% и 4% от диссеминированных заболеваний и заболеваний ЦНС, соответственно [12].В то время как HD ацикловир снижал заболеваемость младенцев с диссеминированным заболеванием (83% выживших имели нормальные исходы нервного развития), у младенцев с заболеванием ЦНС не наблюдалось значительного улучшения заболеваемости (31% выживших имели нормальные исходы неврологического развития).
Младенцы с поражением SEM имеют наилучший прогноз и, как указано ниже, им требуется всего 14 дней внутривенной терапии ацикловиром на HD.
Недавно супрессивная терапия ацикловиром для младенцев с ЦНС после завершения внутривенного лечения значительно улучшила неврологический исход, измеренный по шкале Bailey Developmental Scores [13].Этот режим привел к тому, что примерно 60% (по сравнению с 31%) детей с заболеванием ЦНС развились нормально или с легкими нарушениями. Лечение проводилось в дозе 300 / мг / м 2 в сутки в течение шести месяцев.
Терапия неонатальных инфекций, вызванных вирусом ветряной оспы
Женщины, перенесшие первичную инфекцию вируса ветряной оспы (VZV) в течение 48 часов после родов, имеют детей с риском развития ветряной оспы в течение первых трех недель жизни. Новорожденным этим женщинам традиционно вводят иммуноглобулин против опоясывающего лишая (ZIG), чтобы предотвратить заболевание.Однако при спорадической нехватке ZIG у некоторых новорожденных могут развиться неонатальные заболевания. Никакие контролируемые клинические испытания не оценивали терапию этого заболевания ацикловиром; однако специалисты рекомендуют этот препарат для лечения болезней новорожденных.
Доступные методы лечения инфекций HSV и VZV
Ацикловир (Ациклогуанозин, Зовиракс, ACV)
Ацикловир является наиболее часто назначаемым противовирусным средством для лечения инфекций HSV новорожденных и младенцев.Он был доступен для клинического использования в течение почти трех десятилетий и продемонстрировал замечательную безопасность и эффективность против легких и тяжелых инфекций, вызванных HSV и VZV, как у здоровых пациентов, так и у пациентов с ослабленным иммунитетом, включая новорожденных.
Химия и механизм действия
Ацикловир — аналог дезоксигуанозина. После преимущественного поглощения инфицированными вирусом клетками ацикловир фосфорилируется кодируемой вирусом тимидинкиназой (ТК). Последующее ди- и трифосфорилирование катализируется ферментами клетки-хозяина.Ацикловиртрифосфат предотвращает синтез вирусной ДНК как за счет ингибирования вирусной ДНК-полимеразы, так и за счет того, что он является терминатором цепи.
Спектр и устойчивость
Ацикловир наиболее активен против ВПГ; активность против VZV также значительна, но примерно в 10 раз меньше. Ацикловир считается препаратом выбора как при неонатальных инфекциях HSV, так и при VZV-инфекциях. Активность против ЦМВ низкая, поскольку ЦМВ не обладает активностью тимидинкиназы, а ДНК-полимераза ЦМВ слабо ингибируется ацикловиртрифосфатом.
Устойчивость HSV и VZV к ацикловиру стала важной клинической проблемой среди пациентов с ослабленным иммунитетом, получающих длительную терапию [14]. Устойчивость вирусов к ацикловиру обычно является результатом мутаций в вирусном гене TK, хотя мутации в гене вирусной ДНК-полимеразы также встречаются редко. Резистентные изоляты могут вызывать тяжелые, прогрессирующие, изнурительные заболевания слизистых оболочек у взрослых и, в редких случаях, висцеральное распространение [15, 16]. Изоляты HSV, устойчивые к ацикловиру, также были зарегистрированы у здоровых хозяев, чаще всего у пациентов с часто рецидивирующими генитальными инфекциями, которые лечились хроническим ацикловиром [17].
Показания к применению
Ацикловир эффективен для лечения инфекций, вызванных HSV и VZV, у иммунокомпетентных и иммунодефицитных хозяев, включая новорожденных. Для лечения неонатальных инфекций HSV рекомендуемая доза составляет 20 мг / кг / каждые 8 часов. Продолжительность терапии SEM-заболевания составляет 14 дней, в то время как для детей с ЦНС или диссеминированным заболеванием терапию следует продлить на 21 день.
Ацикловир для перорального применения — это экспериментальный подход к супрессивной терапии, который в настоящее время не одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов.
Фармакокинетика
После внутривенных доз от 2,5 до 15 мг / кг стационарные концентрации ацикловира колеблются от 6,7 до 20,6 мкг / мл. Ацикловир широко распространен; высокие концентрации достигаются в почках, легких, печени, сердце и кожных пузырьках; концентрации в спинномозговой жидкости (CSF) составляют около 50% от концентрации в плазме [18]. Ацикловир проникает через плаценту и накапливается в грудном молоке. Связывание с белками составляет от 9% до 33%, и менее 20% препарата метаболизируется до биологически неактивных метаболитов.Фармакокинетические данные для новорожденных при применении 20 мг / кг / доза отсутствуют.
При отсутствии нарушения функции почек период полувыведения ацикловира составляет от 2 до 3 часов у детей старшего возраста и взрослых и от 2,5 до 5 часов у новорожденных с нормальным клиренсом креатинина. Более 60% введенного препарата выводится с мочой [18]. Выведение продлевается у пациентов с нарушением функции почек; Период полувыведения составляет приблизительно 20 часов у лиц с терминальной стадией почечной недостаточности, что требует изменения дозы для пациентов с клиренсом креатинина менее 50 мл / мин / л.73 м 2 [19]. Ацикловир эффективно удаляется гемодиализом, но не постоянным амбулаторным перитонеальным диализом [20, 21].
Побочные эффекты
Ацикловир, как правило, является безопасным лекарством. Почечная дисфункция возникает в результате обструктивной нефропатии, вызванной образованием кристаллов ацикловира, осаждающихся в почечных канальцах. Иногда внутривенное введение ацикловира вызывает сыпь, потливость, тошноту, головную боль, гематурию и гипотонию. Высокие дозы ацикловира внутривенно (60 мг / кг / день) новорожденным были связаны с нейтропенией [22, 23].
Нейротоксичность может возникать у субъектов с нарушенной функцией почек, которые достигают высоких концентраций препарата в сыворотке [24]. Нейротоксичность проявляется в виде летаргии, спутанности сознания, галлюцинаций, тремора, миоклонуса, судорог, экстрапирамидных признаков и изменений состояния сознания, развивающихся в течение первых нескольких дней после начала терапии. Эти признаки и симптомы обычно проходят спонтанно в течение нескольких дней после прекращения приема ацикловира.
Хотя ацикловир обладает мутагенным действием при высоких концентрациях в некоторых анализах in vitro , он не обладает тератогенным действием на животных.Ограниченные данные о людях позволяют предположить, что использование ацикловира беременными женщинами не связано с врожденными дефектами или другими неблагоприятными исходами беременности.
Лекарственные взаимодействия
Вероятность почечной токсичности ацикловира увеличивается при приеме нефротоксических препаратов, таких как циклоспорин или амфотерицин B.
Терапия врожденной цитомегаловирусной инфекции
Цитомегаловирус (ЦМВ) обычно заражает людей во всем мире серозной инфекцией. 40% у подростков и приближается к 90% у взрослых с плохим социально-экономическим статусом [25, 26].Врожденная ЦМВ-инфекция — наиболее распространенная врожденная инфекция в развитых странах, обнаруживаемая примерно у 1% живорожденных младенцев в Соединенных Штатах [27]. Врожденные ЦМВ-инфекции чаще всего возникают при внутриутробной передаче, но, поскольку вирус распространяется с жидкостями организма, передача также может передаваться перинатально во время родов или постнатально через грудное молоко.
Из всех младенцев, рожденных с врожденной ЦМВ-инфекцией, примерно 7–10% имеют клинически очевидное заболевание при рождении [28].Клинические характеристики внутриутробной инфекции включают ограничение внутриутробного развития, гепатоспленомегалию, желтуху, тромбоцитопению, микроцефалию, перивентрикулярные кальцификации и хориоретинит. Согласно обзору Dollard, истинные показатели смертности трудно получить, и, как сообщается, они достигают 30% для младенцев с симптомами [29], но, скорее всего, в среднем составляют около 5–10% [30]. Смерть обычно происходит из-за проявлений инфекции, не связанных с ЦНС, таких как нарушение функции печени или кровотечение. По оценкам, 40–58% младенцев с симптоматической врожденной ЦМВ-инфекцией имеют необратимые последствия, в то время как младенцы, у которых нет симптомов при рождении, страдают постоянными последствиями почти в 14% случаев [29].Сенсорно-невральная потеря слуха (СНСС), умственная отсталость, судороги, задержка психомоторной и речевой активности, нарушение обучаемости, хориоретинит, атрофия зрительного нерва и дефекты зубных рядов являются наиболее частыми долгосрочными последствиями [31]. В отличие от внутриутробных инфекций, перинатально приобретенные ЦМВ-инфекции обычно не связаны с долгосрочными последствиями, хотя сообщалось об острых заболеваниях у недоношенных детей с очень низкой массой тела при рождении [32]. У доношенных детей перинатальные инфекции обычно протекают бессимптомно, но могут проявляться пневмонитом в течение первых нескольких месяцев жизни [33].
Врожденная ЦМВ-инфекция является следствием инфицирования матери и плода, причем большинство симптоматических врожденных случаев возникает из-за бессимптомной материнской инфекции. При материнской первичной инфекции, по-видимому, происходит нарушение плацентарного кровотока после инфицирования плацентарных вилок [34]. Патогенез поражения ЦНС при врожденной ЦМВ-инфекции начинается с диссеминированного распространения виремии, включая эндотелиальные клетки головного мозга и эпителиальные клетки сосудистого сплетения.Из эндотелиальных клеток головного мозга вирус распространяется на смежные астроциты. Из сосудистого сплетения вирус затем перемещается к эпендимным поверхностям через спинномозговую жидкость (CSF). После инфицирования этих клеток вирус подвергается непрерывной репликации, что приводит к характерным внутриядерным тельцам включения и гибели клеток. Поскольку антитела вырабатываются в условиях непрерывной репликации вируса, также образуются иммунные комплексы, что приводит к дальнейшему иммуноопосредованному повреждению [31]. Хотя специфический патогенез SNHL, опосредованного CMV, не выяснен, гистология показала доказательства инфекции в клетках как улиткового, так и вестибулярного эндолабиринта [35].ЦМВ также был выделен из перилимфы улитки при вскрытии новорожденных с врожденной ЦМВ-инфекцией [36].
Недавние исследования лечения ганцикловиром врожденных ЦМВ-инфекций с поражением ЦНС были многообещающими. Введение ганцикловира в дозах 12 мг / кг / день, разделенных каждые 12 часов в течение 6 недель, улучшило исходы слуха у новорожденных с симптоматической врожденной ЦМВ-инфекцией с поражением ЦНС (о чем свидетельствуют микроцефалия, внутричерепные кальцификации, аномалии спинномозговой жидкости для возраста, хориоретинит и др.) / или нарушения слуха) [37].Первичной конечной точкой был улучшенный ответ, вызванный стволом мозга (BSER) между исходным уровнем и 6-месячным периодом наблюдения (или отсутствие ухудшения в течение 6-месячного последующего наблюдения, если исходный BSER был нормальным). Что касается общего количества ушей, подлежащих оценке, 69% пациентов, получавших ганцикловир, достигли первичной конечной точки по сравнению с 39% в контрольной группе. Ни у одного пациента, получавшего ганцикловир, не было ухудшения слуха от исходного уровня до 6 месяцев. У реципиентов ганцикловира также отмечалось более быстрое разрешение нарушений АЛТ, чем в контрольной группе, хотя вероятность развития нейтропении у них была значительно выше.Дополнительный анализ этого рандомизированного контролируемого исследования позволяет предположить, что ганцикловир может также уменьшать задержки в развитии нервной системы [38]. Улучшение смертности при терапии ганцикловиром пока не показано.
Лечение ЦМВ-инфекций
Ганцикловир (Цитовен)
Ганцикловир был первым противовирусным препаратом, доступным для лечения и профилактики инфекций, вызванных ЦМВ. Доказано, что это очень ценный препарат для пациентов с ослабленным иммунитетом, особенно для пациентов с рецептами трансплантации гемопоэтических стволовых клеток, которые страдают от значительной заболеваемости и смертности от ЦМВ-инфекций, а в последнее время — для детей с врожденной ЦМВ-инфекцией, хотя и не одобрено Управлением по контролю за продуктами и лекарствами США Администрация (FDA) в настоящее время.
Химия и механизм действия
Ганцикловир структурно похож на ацикловир, за исключением гидроксиметильной группы на его ациклической боковой цепи. Первоначальный этап фосфорилирования осуществляется pUL97, вирусной протеинкиназой. Затем клеточные киназы фосфорилируют агент еще два раза, чтобы преобразовать его в его трифосфатное производное, которое способно ингибировать ДНК-полимеразу ЦМВ, кодируемую UL97 , а также встраиваться в вирусную ДНК и обрывать ее.
Ганцикловир трифосфат — конкурентный ингибитор герпесвирусных ДНК-полимераз, приводящий к прекращению удлинения цепи ДНК [1, 20].
Спектр и устойчивость
Ганцикловир имеет сходную с ацикловиром активность против HSV-1, HSV-2 и VZV, но, в отличие от ацикловира, его наибольшая активность против CMV. Устойчивость изолятов ЦМВ обычно возникает в результате мутаций в гене UL97 [39]. Мутации в гене ДНК-полимеразы ЦМВ встречаются реже. Показания .Ганцикловир лицензирован для нескольких показаний за пределами новорожденных. В нескольких обзорах резюмируются эти клинические исходы [2]. Для лечения новорожденных, врожденно инфицированных ЦМВ, было проведено контролируемое исследование [40]. Как отмечалось выше, по сравнению с отсутствием лечения, терапия ганцикловиром предотвращала ухудшение слуха через два года, хотя примерно у двух третей пролеченных младенцев развилась нейтропения, часто требующая изменения дозы.
Фармакокинетика
Пероральная биодоступность ганцикловира низкая, при пероральном приеме всасывается менее 10% препарата [41, 42].Пероральный препарат ганцикловира больше не продается. Пиковые концентрации ганцикловира в сыворотке крови после введения 6 мг / кг (доза для новорожденных) внутривенно вводимого лекарственного средства колеблются от 8 до 11 мкг / мл с концентрациями, достаточными для подавления чувствительных штаммов ЦМВ в водянистой влаге, субретинальной жидкости, спинномозговой жидкости и ткани мозга [ 1]. Период полувыведения ганцикловира составляет от 2 до 3 часов, и большая часть препарата выводится в неизмененном виде с мочой. Фармакокинетика ганцикловира в популяции новорожденных аналогична таковой у взрослых [43, 44].Снижение дозы, пропорциональное степени снижения клиренса креатинина, необходимо лицам с нарушением функции почек. Дополнительная доза рекомендуется после диализа, поскольку она эффективно удаляется гемодиализом [45].
Побочные эффекты
Миелосупрессия — наиболее частое побочное действие ганцикловира; Дозозависимая нейтропения (менее 1000 лейкоцитов / мкл) является наиболее стойким гематологическим отклонением с частотой около 40% [42]. Нейтропения ограничивает дозу примерно в одном из семи курсов и исчезает после прекращения приема препарата.При пероральном приеме ганцикловира нейтропения возникает реже. Тромбоцитопения (менее 50 000 тромбоцитов / мкл) встречается примерно у 20%, а анемия — примерно у 2% реципиентов ганцикловира. От 2 до 5% реципиентов ганцикловира испытывают головную боль, спутанность сознания, изменение психического статуса, галлюцинации, кошмары, беспокойство, атаксию, тремор, судороги. лихорадка, сыпь и аномальные уровни сывороточных печеночных ферментов по отдельности или в некоторой комбинации.
Дозировка
Доза ганцикловира для лечения симптоматической врожденной ЦМВ-инфекции составляет 12 мг / кг / день внутривенно дважды в день в течение 6 недель.
Исследуемый препарат
Валганцикловир (Valcyte)
Валганцикловир был одобрен FDA в марте 2001 г. для лечения ЦМВ-ретинита. Поскольку он хорошо всасывается после перорального приема, он может представлять собой благоприятный вариант по сравнению с внутривенным введением ганцикловира для лечения врожденной ЦМВ-инфекции. В настоящее время он лицензирован для лечения ЦМВ-инфекций в отдельных популяциях трансплантатов и ЦМВ-ретинита у пациентов с ВИЧ / СПИДом.
Химия, механизм действия, спектр и устойчивость
Валганцикловир является пролекарством ганцикловира на основе эфира L-валина и, как таковой, имеет тот же механизм действия, противовирусный спектр и потенциал развития устойчивости, что и ганцикловир [1, 20] .
Показания
Валганцикловир имеет аналогичные показания к ганцикловиру. Однако, основываясь на опубликованных на сегодняшний день ограниченных контролируемых исследованиях, в настоящее время он одобрен для индукционной и поддерживающей терапии ЦМВ-ретинита и для отдельных популяций трансплантатов [46].В настоящее время изучается возможность лечения врожденной ЦМВ-инфекции. В этом рандомизированном контролируемом исследовании, проводимом Группой по совместным антивирусным исследованиям (CASG) Национального института аллергии и инфекционных заболеваний (NIAID), в качестве основной конечной точки используется SNHL.
Фармакокинетика
Валганцикловир быстро превращается в ганцикловир со средним периодом полувыведения из плазмы около 30 минут [46]. Абсолютная биодоступность валганцикловира превышает 60% и фактически увеличивается примерно на 30% при одновременном приеме пищи [47].Площадь под кривой ганцикловира после перорального приема валганцикловира составляет от одной трети до половины площади, полученной после внутривенного введения ганцикловира. Пациентам с нарушением функции почек требуется снижение дозировки, примерно пропорциональное снижению клиренса креатинина.
Побочные эффекты
Наиболее частые побочные эффекты, связанные с терапией валганцикловиром у взрослых, включают диарею (41%), тошноту (30%), нейтропению (27%), анемию (26%) и головную боль (22%) [ 46].Лишь ограниченное число новорожденных получали терапию валганцикловиром. Единственным значимым открытием была нейтропения у 15% пациентов.
Дозировка
Доза валганцикловира зависит от возраста пациента и функции почек. В настоящее время препарат не разрешен к применению у новорожденных с врожденной ЦМВ-инфекцией.
Непроверенные и непроверенные методы лечения неонатальных инфекций HSV, VZV и врожденных ЦМВ-инфекций
Следующие два препарата используются для лечения инфекций HSV, VZV и CMV у детей старшего возраста и взрослых.Данные об этих препаратах предоставляются, если у новорожденных возникает резистентность к противовирусным препаратам при инфекциях ВПГ или ЦМВ. Ни один из препаратов не был оценен в рамках доказательных исследований на новорожденных, и оба связаны со значительной токсичностью. Кроме того, валацикловир может стать доступным для педиатрического применения, особенно для младенцев с инфекцией HSV, ограниченной кожей, глазами и ртом
Цидофовир (HPMPC, Vistide)
Цидофовир был впервые одобрен для использования в США для лечения СПИДа -ассоциированный ретинит, вызванный ЦМВ.Это остается основным показанием к применению этого противовирусного препарата.
Химия и механизм действия
Цидофовир представляет собой новый аналог ациклических фосфонатных нуклеозидов с механизмом действия, аналогичным другим аналогам нуклеозидов. В отличие от ацикловира, вирусные ферменты не требуются для начального фосфорилирования, поскольку нативный цидофовир уже имеет одну присоединенную фосфатную группу. После дифосфорализации клеточными киназами цидофовир конкурентно ингибирует ДНК-полимеразу [48].Активная форма цидофовира проявляет в 25-50 раз большее сродство к вирусной ДНК-полимеразе по сравнению с клеточной ДНК-полимеразой.
Спектр и устойчивость
Цидофовир активен против ВПГ и ЦМВ, включая устойчивые к ацикловиру и фоскарнету изоляты ВПГ и мутанты ЦМВ, устойчивые к ганцикловиру и фоскарнету [49]. Он также активен in vitro против VZV, EBV, вируса герпеса человека-6, вируса герпеса человека-8, полиомавирусов, аденовируса и ВПЧ человека.
Было описано небольшое количество устойчивых к цидофовиру изолятов ЦМВ, которые также устойчивы к ганцикловиру на основе мутаций в гене ДНК-полимеразы [50].Сообщалось также о мутанте ЦМВ, устойчивом к ганцикловиру, фоскарнету и цидофовиру [51].
Показания к применению
Цидофовир замедляет прогрессирование заболевания сетчатки у пациентов со СПИДом [52, 53]. Цидофовир также был полезен при лечении заболеваний, вызванных устойчивыми к ацикловиру изолятами ВПГ [54]. Были опубликованы отдельные сообщения об улучшении папилломатоза гортани после инъекции цидофовира в очаг поражения, но на основании этого ограниченного опыта невозможно сделать окончательные выводы об эффективности [55, 56].
Фармакокинетика
Только 2–26% цидофовира всасывается после перорального приема, поэтому его вводят внутривенно. Период полувыведения цидофовира из плазмы составляет 2,6 часа, но период полураспада активных внутриклеточных метаболитов цидофовира составляет от 17 до 48 часов [ 57]. Девяносто процентов препарата выводится с мочой, в основном с секрецией почечных канальцев [58]. Важно отметить, что препарат не проникает через гематоэнцефалический барьер и, следовательно, не должен использоваться для лечения инфекций ЦНС.
Побочные эффекты
Поскольку цидофовир концентрируется в почечных клетках в количествах в 100 раз больше, чем в других тканях, нефротоксичность является основным побочным эффектом, особенно если гидратация не поддерживается должным образом [57, 58].Проявления почечной токсичности включают протеинурию и глюкозурию. Агрессивная внутривенная прегидратация, одновременное введение пробенецида и отказ от других нефротоксичных агентов снижают вероятность токсичности. Цидофовир противопоказан пациентам с креатинином сыворотки> 1,5 мг / дл, расчетным клиренсом креатинина ≤ 55 мл / мин или белком в моче ≥ 100 мг / дл, и препарат следует прекратить, если креатинин сыворотки повышается на ≥ 0,5 мг / дл выше исходного уровня. .
Дозировка
Цидофовир вводят внутривенно детям старшего возраста и взрослым в дозе 5 мг / кг один раз в неделю с пробенецидом.Пациенты с нарушением функции почек (расчетный клиренс креатинина <55 мл / мин) проходят лечение каждые 2 недели. Дозу следует уменьшить с 5 мг / кг до 3 мг / кг, если креатинин сыворотки повышается на> 0,3 мг / дл выше исходного уровня. Данных о дозировании цидофовира новорожденным нет.
Фоскарнет (PFA, Foscavir)
Фоскарнет — единственный противогерпетический препарат, не являющийся аналогом нуклеозидов. Это не препарат первой линии, но он полезен для лечения инфекций, вызванных устойчивыми вирусами герпеса.
Химия и механизм действия
Фоскарнет — неорганический аналог пирофосфата, который напрямую ингибирует ДНК-полимеразу, блокируя сайт связывания пирофосфата [20, 59].
Спектр и устойчивость
Фоскарнет ингибирует все известные герпесвирусы человека, включая большинство устойчивых к ганцикловиру изолятов ЦМВ и устойчивые к ацикловиру вирусы простого герпеса и вируса зодиака. Он также активен против ВИЧ. Устойчивость возникает в результате мутаций ДНК-полимеразы. Сообщалось о штаммах CMV, HSV и VZV с пониженной чувствительностью к фоскарнету [59, 60].
Показания к применению
Фоскарнет так же эффективен, как и ганцикловир, для лечения угрожающего зрению хориоретинита, вызванного ЦМВ, у взрослых пациентов со СПИДом [61]. Из-за присущей ему активности против ВИЧ, он может даже обеспечить преимущество в выживаемости для пролеченных пациентов [62]. Рефрактерные случаи хориоретинита могут поддаваться лечению комбинацией фоскарнета и ганцикловира. Фоскарнет также эффективен при терапии ЦМВ-инфекций, вызванных ганцикловир-резистентными штаммами вируса [62]. Ограниченные данные также предполагают, что фоскарнет может быть полезным при назначении пациентам со СПИДом, у которых есть желудочно-кишечные и легочные инфекции, вызванные ЦМВ.
Инфекции, вызванные устойчивыми к ацикловиру штаммами HSV и VZV, успешно контролируются с помощью фоскарнета [63, 64].
Фармакокинетика
Только около 20% фоскарнета абсорбируется после перорального приема. Максимальная концентрация в сыворотке, достигаемая после внутривенного введения 60 мг / кг, составляет примерно 500 мкмоль / л [59]. Концентрация в спинномозговой жидкости составляет около двух третей от концентрации в сыворотке. Период полувыведения фоскарнета составляет около 48 часов, и 80% введенной дозы выводится в неизмененном виде с мочой.Необходимо снижение дозы пропорционально уменьшению клиренса креатинина. Гемодиализ эффективно устраняет фоскарнет, поэтому после диализа рекомендуется дополнительная доза [65]. Данных о применении фоскарнета новорожденным нет.
Побочные эффекты
Наиболее частыми побочными эффектами фоскарнета являются нефротоксичность и метаболические нарушения. Доказательства нефротоксичности включают азотемию, протеинурию, острый тубулярный некроз, кристаллурию и интерстициальный нефрит.Концентрация креатинина в сыворотке увеличивается до 50% пациентов. К счастью, функция почек приходит в норму в течение 2–4 недель после прекращения терапии. Существующее ранее заболевание почек, одновременный прием других нефротоксических препаратов, обезвоживание, быстрое введение или непрерывное внутривенное вливание препарата являются факторами риска развития почечной дисфункции [66]. Метаболические нарушения, связанные с терапией фоскарнетом, включают гипо- и гиперкальциемию, а также гипо- и гиперфосфатемию [67]. Гипокальциемия может быть связана с парестезиями, тетанией, судорогами и аритмиями.Метаболические нарушения сводятся к минимуму, если вводить фоскарнет медленной инфузией. Симптомы со стороны ЦНС, связанные с терапией фоскарнетом, включают головную боль, тремор, раздражительность, судороги и галлюцинации. Сообщалось также о лихорадке, тошноте, рвоте, аномальных ферментах сыворотки крови, анемии, гранулоцитопении и генитальных изъязвлениях.
Лекарственные взаимодействия
Одновременное применение амфотерицина B, циклоспорина, гентамицина и других нефротоксических препаратов увеличивает вероятность нарушения функции почек.Одновременный прием пентамидина увеличивает риск гипокальциемии. Анемия и нейтропения чаще встречаются, когда пациенты также получают зидовудин.
Дозировка
Обычная доза фоскарнета при ЦМВ-инфекции составляет 180 мг / кг / день в три приема в течение 14–21 дня, после чего следует ежедневная поддерживающая доза от 90 до 120 мг / кг. Дозировка фоскарнета, используемого при инфекциях, вызванных устойчивыми к ацикловиру HSV и VZV, составляет 120 мг / кг / день в три приема.
Резюме
Несмотря на то, что в лечении врожденных ЦМВ и неонатальных инфекций ВПГ достигнут значительный прогресс, дальнейшие достижения являются обязательными.С появлением новых противовирусных препаратов, обладающих другим механизмом действия, появляется возможность для комбинированной терапии, если можно доказать, что лекарства безопасны.
Выражение признательности
Этот проект полностью или частично финансируется за счет федеральных средств Национального института аллергии и инфекционных заболеваний, Национальных институтов здравоохранения, Министерства здравоохранения и социальных служб по контракту № N01-AI-30025.
Сноски
Заявление издателя: Это PDF-файл неотредактированной рукописи, принятой к публикации.В качестве услуги для наших клиентов мы предоставляем эту раннюю версию рукописи. Рукопись будет подвергнута копированию, верстке и рассмотрению полученного доказательства, прежде чем она будет опубликована в окончательной форме для цитирования. Обратите внимание, что во время производственного процесса могут быть обнаружены ошибки, которые могут повлиять на содержание, и все юридические оговорки, относящиеся к журналу, имеют отношение.
Ссылки
1. Кимберлин Д. Противовирусные агенты. В: Лонг С., Пикеринг Л., Пробер С., редакторы. Принципы и практика детских инфекционных болезней.3-е изд. Нью-Йорк: Эльзевир; 2008. С. 1470–1488. [Google Scholar] 2. Ра Б., Кимберлин Д. В., Уитли Р. Противовирусные препараты. В: Джером К., редактор. Лабораторная диагностика вирусных инфекций. 3-е изд. Нью-Йорк: Informa Healthcare; 2009. [Google Scholar] 3. Brown ZA, Wald A, Morrow RA, Selke S, Zeh J, Corey L. Влияние серологического статуса и кесарева сечения на скорость передачи вируса простого герпеса от матери к ребенку. ДЖАМА. 2003. 289 (2): 203–209. [PubMed] [Google Scholar] 4. Уитли Р.Дж. Вирус простого герпеса.В: Scheld MW, Whitley RJ, Marra CM, редакторы. Инфекции центральной нервной системы. 3-е изд. Филадельфия: Липпинкотт Уильямс и Уилкинс; 2004. С. 123–144. [Google Scholar] 5. Kimberlin DW, Lin CY, Jacobs RF, Powell DA, Frenkel LM, Gruber WC, et al. Естественная история инфекций, вызванных вирусом простого герпеса новорожденных, в эпоху ацикловира. Педиатрия. 2001. 108 (2): 223–229. [PubMed] [Google Scholar] 6. Kimberlin DW. Ведение энцефалита, вызванного вирусом простого герпеса, у взрослых и новорожденных: диагностика, прогноз и лечение.Герпес. 2007 июн; 14 (1): 11–16. [PubMed] [Google Scholar] 7. Хатто С., Арвин А., Джейкобс Р., Стил Р., Стагно С., Лайрин Р. и др. Внутриутробные инфекции, вызванные вирусом простого герпеса. Журнал педиатрии. 1987. 110 (1): 97–101. [PubMed] [Google Scholar] 8. Уитли Р.Дж. Инфекции, вызванные вирусом простого герпеса. В: Remington JS, Klein JO, редакторы. Инфекционные болезни плода и новорожденных. 3-е изд. Филадельфия: W.B. Компания Сондерс; 1990. С. 282–305. [Google Scholar] 9. Уитли Р.Дж., Кори Л., Арвин А., Лейкман Ф.Д., Сумая К.В., Райт П.Ф. и др.Изменение представления инфекции вируса простого герпеса у новорожденных. Журнал инфекционных болезней. 1988. 158 (1): 109–116. [PubMed] [Google Scholar] 10. Уитли Р.Дж., Ройзман Б. Вирусы простого герпеса. В: Ричман Д.Д., Уитли Р.Дж., Хайден Ф.Г., редакторы. Клиническая вирусология. 2-е изд. Вашингтон, округ Колумбия: ASM Press; 2004. С. 375–401. [Google Scholar] 11. Уитли Р., Арвин А., Пробер С., Берчетт С., Кори Л., Пауэлл Д. и др. Контролируемое испытание по сравнению видарабина с ацикловиром при неонатальной инфекции вирусом простого герпеса.Медицинский журнал Новой Англии. 1991. 324 (7): 444–449. [PubMed] [Google Scholar] 12. Kimberlin DW, Lin CY, Jacobs RF, Powell DA, Corey L, Gruber WC, et al. Безопасность и эффективность высоких доз внутривенного ацикловира при лечении инфекций, вызванных вирусом простого герпеса у новорожденных. Педиатрия. 2001. 108 (2): 230–238. [PubMed] [Google Scholar] 13. Кимберлин Д., Уитли Р., Ван В., Пауэлл Д., Сторч Г., Ахмед А. и др. Влияние перорального подавления ацикловира на исходы развития нервной системы и рецидивы кожи после болезни, вызванной вирусом простого герпеса новорожденных.NEJM. 2011 В печати. [Google Scholar] 14. Englund JA, Zimmerman ME, Swierkosz EU, Goodman JL, Scholl D, Balfour HH. Вирус простого герпеса устойчив к ацикловиру. Исследование в центре высокоспециализированной медицинской помощи. Ann Intern Med. 1990; 112: 416–422. [PubMed] [Google Scholar] 15. Полевой АК, Бирон К.К. Возвращение к «концу невинности»: устойчивость герпесвирусов к противовирусным препаратам. Clin Microbiol Rev.1994, январь; 7 (1): 1–13. [Бесплатная статья PMC] [PubMed] [Google Scholar] 16. Лайалл Э.Г., Огилви М.М., Смит Н.М., Бернс С. Устойчивость к ацикловиру ветряной оспы и ВИЧ-инфекция.Arch Dis Child. 1994 Февраль; 70 (2): 133–135. [Бесплатная статья PMC] [PubMed] [Google Scholar] 17. Морфин Ф, Тувено Д. Устойчивость вируса простого герпеса к противовирусным препаратам. J Clin Virol. 2003 Янв; 26 (1): 29–37. [PubMed] [Google Scholar] 18. Wagstaff AJ, Faulds D, Goa Kl. Ацикловир. Переоценка его противовирусной активности, фармакокинетических свойств и терапевтической эффективности. Наркотики. 1994; 47: 153–205. [PubMed] [Google Scholar] 19. Ласкин О.Л., Лонгстрет Дж. А., Велтон А., Красный Х. С., Кини Р. Э., Рокко Л. и др. Влияние почечной недостаточности на фармакокинетику ацикловира.Am J Med. 20 июля 1982 г .; 73 (1A): 197–201. [PubMed] [Google Scholar] 20. Инь М., Браст Дж., Тиеу Х., Хаммер С. Антигепатитные и антиреспираторные вирусные агенты. В: Ричман Д., Уитли Р., Хайден Ф., редакторы. Клиническая вирусология. Вашингтон, округ Колумбия: ASM Press; 2009. С. 217–264. [Google Scholar] 21. Красный ХК, Ляо С.Х., де Миранда П., Ласкин О.Л., Велтон А., Литман П.С. Влияние гемодиализа на фармакокинетику ацикловира у пациентов с хронической почечной недостаточностью. Am J Med. 20 июля 1982 г.; 73 (1A): 202–204. [PubMed] [Google Scholar] 22.Кимберлин Д., Пауэлл Д., Грубер В., Диаз П., Арвин А., Кумар М. и др. Назначение пероральной супрессивной терапии ацикловиром после неонатального заболевания, вызванного вирусом простого герпеса, ограниченным поражением кожи, глаз и рта: результаты тиража фазы I / II. Pediatr Infect Dis J. 1996; 15: 247–254. [PubMed] [Google Scholar] 23. Kimberlin DW, Lin CY, Jacobs RF, Powell DA, Corey L, Gruber WC, et al. Безопасность и эффективность высоких доз внутривенного ацикловира при лечении инфекций, вызванных вирусом простого герпеса у новорожденных. Педиатрия.2001 август; 108 (2): 230–238. [PubMed] [Google Scholar] 24. Реванкар С.Г., Эпплгейт А.Л., Марковиц Д.М. Делирий, связанный с лечением ацикловиром у пациента с почечной недостаточностью. Clin Infect Dis. 1995 августа; 21 (2): 435–436. [PubMed] [Google Scholar] 25. Гриффитс П.Д., Эмери В.К. Цитомегаловирус. В: Ричман Д.Д., Уитли Р.Дж., Хайден Ф.Г., редакторы. Клиническая вирусология. 2-е изд. Вашингтон, округ Колумбия: ASM Press; 2002. С. 433–461. [Google Scholar] 26. Старас С.А., Доллард СК, Рэдфорд К.В., Фландрия В.Д., Пасс РФ, Кэннон М.Дж. Распространенность цитомегаловирусной инфекции в США: 1988–1994 гг.Clin Infect Dis. 2006 г., 1 ноября; 43 (9): 1143–1151. [PubMed] [Google Scholar] 27. Demmler GJ. Американское общество инфекционных болезней и Центры по контролю за заболеваниями. Резюме семинара по надзору за врожденным цитомегаловирусным заболеванием. Обзоры инфекционных болезней. 1991. 13 (2): 315–329. [PubMed] [Google Scholar] 28. Conboy TJ, Pass RF, Stagno S, Alford CA, Myers GJ, Britt WJ и др. Ранние клинические проявления и интеллектуальный исход у детей с симптоматической врожденной цитомегаловирусной инфекцией.Журнал педиатрии. 1987. 111 (3): 343–348. [PubMed] [Google Scholar] 29. Доллард СК, Гросс С.Д., Росс Д.С. Новые оценки распространенности неврологических и сенсорных последствий и смертности, связанных с врожденной цитомегаловирусной инфекцией. Rev Med Virol. 1 июня 2007 г .; [PubMed] [Google Scholar] 30. Росс С.А., Боппана С.Б. Врожденная цитомегаловирусная инфекция: исход и диагноз. Semin Pediatr Infect Dis. 2005 Янв; 16 (1): 44–49. [PubMed] [Google Scholar] 31. Гриффитс PD, Маклафлин JE. Цитомегаловирус.В: Scheld WM, Whitley RJ, Marra CM, редакторы. Инфекции центральной нервной системы. Филадельфия: Липпинкотт Уильямс и Уилкинс; 2004. С. 159–173. [Google Scholar] 32. Машманн Дж., Хампрехт К., Дитц К., Ян Дж., Шпеер С.П. Цитомегаловирусная инфекция младенцев с крайне низкой массой тела при рождении через грудное молоко. Клинические инфекционные болезни. 2001; 33 (12): 1998–2003. [PubMed] [Google Scholar] 33. Brasfield DM, Stagno S, Whitley RJ, Cloud G, Cassell G, Tiller RE. Детский пневмонит, связанный с цитомегаловирусом, хламидиозом, пневмоцистом и уреаплазмой.Педиатрия. 1987. 79: 76–83. [PubMed] [Google Scholar] 34. Перейра Л., Майджи Э. Цитомегаловирусная инфекция в плаценте человека: материнский иммунитет и рецепторы, регулируемые развитием трофобластов, сходятся. Актуальные темы микробиологии и иммунологии. 2008. 325: 383–395. [PubMed] [Google Scholar] 35. Штраус М. Цитомегаловирусный лабиринтит человека. Am J Otolaryngol. Сентябрь – октябрь 1990 г., 11 (5): 292–298. [PubMed] [Google Scholar] 36. Дэвис Л. Е., Джонссон Л. Г., Корнфельд М. Цитомегаловирусный лабиринтит у младенцев: морфологические, вирусологические и иммунофлуоресцентные исследования.J Neuropathol Exp Neurol. 1981, январь; 40 (1): 9–19. [PubMed] [Google Scholar] 37. Kimberlin DW, Lin CY, Sanchez PJ, Demmler GJ, Dankner W, Shelton M и др. Влияние терапии ганцикловиром на слух при симптоматическом врожденном цитомегаловирусном заболевании с поражением центральной нервной системы: рандомизированное контролируемое исследование. Журнал педиатрии. 2003. 143 (1): 16–25. [PubMed] [Google Scholar] 38. Оливер С., Клауд Дж., Санчес П., Деммлер Дж., Данкнер В., Шелтон М. и др. Влияние терапии ганцикловиром (GCV) на исходы нервного развития при симптоматических врожденных цитомегаловирусных (CMV) инфекциях с поражением центральной нервной системы (ЦНС): рандомизированное контролируемое исследование.Ежегодное собрание Общества педиатрических исследований (SPR); 2006 29 апреля; Сан-Франциско, Калифорния. 2006. с. Реферат № 752908. [Google Scholar] 39. Маркхэм А., Фолдс Д. Ганцикловир: обновление его терапевтического использования при цитомегаловирусной инфекции. Наркотики. 1994; 48: 455. [PubMed] [Google Scholar] 40. Kimberlin DW, Lin C-Y, Sanchez PJ, Demmler GJ, Dankner W, Shelton MD, et al. Влияние ганцикловира на слух при симптоматическом врожденном цитомегаловирусном заболевании с поражением центральной нервной системы: рандомизированное контролируемое исследование.J Pediatr. 2003. 143: 16–25. [PubMed] [Google Scholar] 41. Редди В., Хао Ю., Липтон Дж., Мехарчанд Дж., Минден М., Мацзулли Т. и др. Ведение реципиентов аллогенного трансплантата костного мозга с риском цитомегаловирусной болезни с использованием контрольной бронхоскопии и длительной упреждающей терапии ганцикловиром. J Clin Virol. 1999, август; 13 (3): 149–159. [PubMed] [Google Scholar] 42. Jacobson MA, Gambertoglio JG, Aweeka FT, Causey DM, Portale AA. Гипокальциемия, вызванная фоскарнетом, и влияние фоскарнета на метаболизм кальция.J Clin Endocrinol Metab. 1991 Май; 72 (5): 1130–1135. [PubMed] [Google Scholar] 43. Френкель Л.М., Каппарелли Е.В., Данкнер В.М., Сюй Дж., Смит И.Л., Баллоу А. и др. Ганцикловир для приема внутрь у детей: фармакокинетика, безопасность, переносимость и противовирусное действие. Группа педиатрических клинических испытаний СПИДа. Журнал инфекционных болезней. 2000 декабрь; 182 (6): 1616–1624. [PubMed] [Google Scholar] 44. Транг Дж. М., Кидд Л., Грубер В., Сторч Дж., Деммлер Дж., Джейкобс Р. и др. Линейная фармакокинетика однократной дозы ганцикловира у новорожденных с врожденными цитомегаловирусными инфекциями.Clin Pharmacol Ther. 1993; 53: 15–21. [PubMed] [Google Scholar] 45. Свон С.К., Мунар М.Ю., Виггер М.А., Беннетт В.М. Фармакокинетика ганцикловира у пациента, находящегося на гемодиализе. Am J Kidney Dis. 1991, январь; 17 (1): 69–72. [PubMed] [Google Scholar] 46. Cocohoba JM, McNicholl IR. Валганцикловир: прогресс в лечении цитомегаловирусов. Энн Фармакотер. 2002 июнь; 36 (6): 1075–1079. [PubMed] [Google Scholar] 47. Юнг Д., Дорр А. Фармакокинетика однократной дозы валганцикловира у ВИЧ- и ЦМВ-серопозитивных субъектов.J Clin Pharmacol. 1999, август; 39 (8): 800–804. [PubMed] [Google Scholar] 48. Хо Х.Т., Вудс К.Л., Бронсон Дж. Дж., Де Бок Х., Мартин Дж. К., Хичкок МД. Внутриклеточный метаболизм антигерпетических средств -1- {3-гидрокси-2- (фосфонилметокси) пропил} цитозин. Mol Pharmacol. 1992; 41: 197–202. [PubMed] [Google Scholar] 49. Сафрин С, Черрингтон Дж, Джаффе Х.С. Клиническое использование цидофовира. Rev Med Virol. 1997 сентябрь; 7 (3): 145–156. [PubMed] [Google Scholar] 50. Lurain N, Spafford LE, Thompson KD. Мутация в открытой рамке считывания UL97 штаммов цитомегаловируса человека, устойчивых к ганцикловиру.Журнал вирусологии. 1994b; 68: 4427–4431. [Бесплатная статья PMC] [PubMed] [Google Scholar] 51. Черрингтон Дж. М., Майнер Р., Аллен С. Дж. У. и др. Сенситивы клинических изолятов цитомегаловируса человека (HCMV) к цидофовиру. Восьмая международная конференция по противовирусным исследованиям; 1995 г. 23–28 апреля; Санта-Фе, Нью-Мексико. 1995. [Google Scholar] 52. Исследования глазных осложнений Группы исследований СПИДа в сотрудничестве с Группой клинических испытаний СПИДа. Цидофовир (HPMPC) для лечения цитомегаловирусного ретинита у пациентов со СПИДом: исследование HPMPC Peripheral Cytomegalovirus Retinitis Trial.Ann Intern Med. 1997. 126: 264–274. [PubMed] [Google Scholar] 53. Lalezari JP, Staagg RJ, Kuppermann BD, Holland GN, Kramer F, Ives DV, et al. Внутривенное введение цидофовира при периферическом цитомегаловирусном ретините у пациентов со СПИДом: рандомизированное контролируемое исследование. Ann Intern Med. 1997. 126: 257–263. [PubMed] [Google Scholar] 54. Лалезари Дж. П., Дрю В. Л., Глутцер Э., Майнер Д., Сафрин С., Оуэн В. Ф., младший и др. Лечение внутривенным (S) -1- [3-гидрокси-2- (фосфонилметокси) пропил) -цитозином ацикловир-резистентной кожно-слизистой инфекции вирусом простого герпеса у пациента со СПИДом.Журнал инфекционных болезней. 1994; 170: 570–572. [PubMed] [Google Scholar] 55. Кимберлин DW, Малис DJ. Рецидивирующий респираторный папилломатоз с юношеским началом: возможности успешной противовирусной терапии. Antiviral Res. 2000 Февраль; 45 (2): 83–93. [PubMed] [Google Scholar] 56. Прански С.М., Магит А.Е., Кернс Д.Б., Канг Д.Р., Дункан Н.О. Цидофовир внутриочаговый при рецидивирующем респираторном папилломатозе у детей. Arch Otolaryngol Head Neck Surg. 1999 Октябрь; 125 (10): 1143–1148. [PubMed] [Google Scholar] 57. Канди К.С., Петти Б.Г., Флаэрти Дж., Фишер П.Е., Полис М.А., Ваксман М. и др.Клиническая фармакокинетика цидофовира у пациентов, инфицированных вирусом иммунодефицита человека. Антимикробные агенты Chemother. 1995; 39: 1247–1252. [Бесплатная статья PMC] [PubMed] [Google Scholar] 58. Лалезари Дж. П., Дрю В. Л., Глутцер Э., Джеймс С., Майнер Д., Флаэрти Дж. И др. (S) -1 {3-гидрокси-2- (фосфонилметокси) пропил} цитозин (цидофовиир): результаты исследования фазы I / II нового противовирусного аналога нуцелотида. Журнал инфекционных болезней. 1995; 171: 788–796. [PubMed] [Google Scholar] 59. Wagstaff AJ, Bryson HM.Фоскарнет: переоценка его противовирусной активности, фармакокинетических свойств и терапевтического использования у пациентов с ослабленным иммунитетом и вирусной инфекцией. Наркотики. 1994; 48: 199–226. [PubMed] [Google Scholar] 60. Сафрин С., Кеммерли С., Плоткин Б., Смит Т., Вайсбах Н., Де Веранес Д. и др. Инфекция, вызванная устойчивым к фоскарнету вирусом простого герпеса, у больных СПИДом. Журнал инфекционных болезней. 1994; 169: 193–196. [PubMed] [Google Scholar] 61. Снок Р., Андрей Г., Джерард М., Сильверман А., Хеддерман А., Бальзарини Дж. И др.Успешное лечение прогрессирующей кожно-слизистой инфекции, вызванной устойчивым к ацикловиру и фоскарнету вирусом простого герпеса, с помощью (S) -1- (3-гидрокси-2-фосфонилметоксипропил) цитозина (HPMPC) Clin Infect Dis. 1994 Апрель; 18 (4): 570–578. [PubMed] [Google Scholar] 62. Якобсон М.А., Дрю В.Л., Фейнберг Дж., О’Доннелл Дж. Дж., Уитмор П.В., Майнер Р.Д. и др. Терапия фоскарнетом при ганцикловиррезистентном цитомегаловирусном ретините у больных СПИДом. Журнал инфекционных болезней. 1991; 163: 1348–1351. [PubMed] [Google Scholar] 63.Сафрин С., Бергер Т.Г., Гилсон И. Терапия фоскарнетом у пяти пациентов со СПИДом и инфекцией вируса ветряной оспы, устойчивой к ацикловиру. Ann Intern Med. 1991; 115: 19–21. [PubMed] [Google Scholar] 64. Исследования глазных осложнений исследовательской группы СПИДа. Смертность у пациентов с синдромом приобретенного иммунодефицита, получавших фоскарнет или ганцикловир от цитомегаловируса ретинита. N Engl J Med. 1992; 326: 213–220. [PubMed] [Google Scholar] 65. Сафрин С., Крампакер С., Чатис П., Дэвис Р., Хафнер Р., Раш Дж. И др.Контролируемое исследование по сравнению фоскарнета и видарабина при лечении ацикловир-резистентного кожно-слизистого простого герпеса при синдроме приобретенного иммунодефицита. N Engl J Med. 1991; 325: 551–555. [PubMed] [Google Scholar] 66. МакГрегор Р. Р., Грациани А. Л., Вайс Р., Грюнвальд Дж. Э., Гамбертольо Дж. Г.. Успешная терапия фоскарнетом при цитомегаловирусном ретините у пациента со СПИДом, находящегося на гемодиализе: обоснование эмпирического дозирования и мониторинга уровня в плазме. Журнал инфекционных болезней. 1991 Октябрь; 164 (4): 785–787.[PubMed] [Google Scholar] 67. Дерай Г., Мартинес Ф., Катлама С., Левальтье Б., Бофилс Н., Данис М. и др. Нефротоксичность фоскарнета: механизм, частота возникновения и профилактика. Am J Nephrol. 1989. 9 (4): 316–321. [PubMed] [Google Scholar]противовирусных препаратов для здоровых детей
КЭТРИН Л. МАРГО, доктор медицинских наук, и АЛЛЕН Ф. ШОГНЕССИ, PHARM.D., Программа резидентуры по семейной практике в Гаррисбурге, Харрисбург, Пенсильвания
Am Famician. 1 марта 1998 г .; 57 (5): 1073-1077.
Существует несколько противовирусных средств для лечения вирусных заболеваний у здоровых детей.У некоторых детей лечение ацикловиром является альтернативой вакцинации для лечения и профилактики ветряной оспы. Ацикловир также может быть полезен при лечении или профилактике инфекций простого герпеса у новорожденных. Рибавирин, который когда-то рекомендовался в качестве рутинной терапии для младенцев из группы высокого риска с респираторно-синцитиальным вирусом, теперь предназначен для применения у отдельных детей. Амантадин и римантидин эффективны против гриппа типа А и могут использоваться для защиты детей от гриппа, а также для уменьшения продолжительности и тяжести заболевания у тех, кто уже болен.
Вирусные инфекции новорожденных, младенцев и детей варьируются от простуды до чрезвычайно редкого, но смертельного менингита, вызванного вирусом простого герпеса. Хотя для профилактики или лечения простуды можно сделать немногое, противовирусные препараты могут сократить продолжительность некоторых вирусных заболеваний.
В этом обзоре кратко описывается текущее состояние противовирусных препаратов в лечении ветряной оспы, инфекций, вызванных вирусом простого герпеса, и респираторно-синцитиальных вирусных инфекций, а также в профилактике и лечении инфекции гриппа.Комплексные потребности детей с ослабленным иммунитетом выходят за рамки данной статьи.
Ветряная оспа
Инфекция ветряной оспы (ветряная оспа) встречается примерно у 3-4 миллионов детей в год. Однако эта заболеваемость должна резко снизиться в результате недавнего утверждения вакцины против ветряной оспы (Варивакс) и рекомендации о ее широком использовании Консультативным комитетом по практике иммунизации Центров по контролю и профилактике заболеваний.1,2
In Помимо конституциональных проявлений ветряной оспы, наиболее частыми побочными эффектами, связанными с инфекцией, являются дни, пропущенные из школы (в среднем 8.7 дней) и рабочие дни, потерянные родителями (в среднем 0,5 дня), которые должны оставаться дома со своим ребенком.3 Серьезные осложнения у детей, такие как пневмония и энцефалит, редки, хотя ежегодно происходит около 50 смертей. Группы с наибольшим риском осложнений включают младенцев в возрасте до одного года, подростков, беременных женщин и пациентов, принимающих кортикостероиды в высоких дозах. Пациенты старшего возраста имеют более тяжелое клиническое течение.
Ацикловир (Зовиракс) одобрен для неотложной терапии ветряной оспы у детей и взрослых.Когда ацикловир назначается в течение первых 24 часов после появления сыпи у детей, конституциональные симптомы и зуд уменьшаются. Количество повреждений и время до образования корки также уменьшаются. В среднем у детей, прошедших лечение, замедление отравления происходит быстрее (день 1 по сравнению со вторым днем). Однако к третьему дню у всех леченных детей и 75 процентов нелеченных детей наблюдается афебрилитет.4 Когда терапия ацикловиром начинается через 24 или более часов после появления сыпи, пользы не наблюдается.
В настоящее время нет данных о том, что лечение ветряной оспы ацикловиром ускоряет возвращение детей в школу или родителей на работу; Активная терапия не снизила скорость развития осложнений.
Побочные эффекты, связанные с ацикловиром, встречаются редко. Проблемы с желудочно-кишечным трактом возникают нечасто. На иммунный ответ после ветряной оспы терапия ацикловиром не влияет. Не было показано никакого эффекта на последующее развитие ветряной оспы у детей, получавших ацикловир.
Дозировка ацикловира перорально составляет 20 мг на кг на дозу, четыре раза в день, до 800 мг на дозу. Терапия ацикловиром не показана беременным женщинам и детям младше двух лет.Терапия продолжается пять дней и стоит от 70 до 80 долларов.
Ацикловир также использовался для предотвращения развития ветряной оспы после заражения в домашних условиях. В одном неслепом нерандомизированном исследовании 5 детям, подвергшимся воздействию, давали ацикловир, начиная с семи-девяти дней после воздействия и продолжая в течение семи дней. Ветряная оспа развилась у 16 процентов детей, получавших лечение, по сравнению со 100 процентами детей, не получавших лечения. Сероконверсия, маркер субклинической инфекции, произошла у 85 процентов детей, получавших ацикловир.
Второе исследование6 также показало, что профилактика ацикловиром, проводимая на второй неделе после воздействия, допускала сероконверсию без развития симптомов. Эта защита не наблюдалась у всех испытуемых, поэтому до сих пор неизвестно, является ли ацикловир подходящей альтернативой иммуноглобулину против ветряной оспы для защиты после контакта.
Американская академия педиатрии7 (AAP) не рекомендует рутинное использование ацикловира в случаях неосложненной ветряной оспы у здоровых детей.Он рекомендует лечение ацикловиром восприимчивых небеременных подростков. Терапия ацикловиром также может быть рассмотрена у детей старше 12 месяцев, которые получают длительную терапию салицилатами (из-за риска синдрома Рея), у детей с хроническими легочными или кожными проблемами, а также у тех, кто получает кортикостероиды в аэрозольной форме. Однако преимущества терапии в этих группах не доказаны.
Дети с ослабленным иммунитетом, включая детей, получающих пероральные кортикостероиды в дозах 2 или более мг на кг в день, должны получать ацикловир внутривенно для профилактики или лечения диссеминированной ветряной оспы.Дозировка составляет 500 мг на 1 м 2 2 каждые восемь часов. Для детей младше 12 месяцев доза составляет 30 мг на кг в сутки в три приема. Терапия продолжается от семи до 10 дней.8 (p635)
Два других противовирусных препарата, фамцикловир (Фамвир) и валацикловир (Валтрекс), доступны для лечения опоясывающего герпеса и рецидивирующего генитального герпеса. Ни один из этих агентов не предназначен для лечения ветряной оспы у детей, и нет исследований, оценивающих использование этих агентов у детей с опоясывающим лишаем.
Таким образом, терапия ацикловиром может несколько уменьшить тяжесть и продолжительность острой ветряной оспы. Чтобы терапия была эффективной, ее следует начинать в течение 24 часов с момента появления сыпи, что может быть затруднительно. Его влияние на последующее развитие опоясывающего лишая неизвестно. В связи с маркетингом вакцины против ветряной оспы немногие дети должны нуждаться в лечении от острой инфекции ветряной оспы.
Вирус простого герпеса
Вирус простого герпеса чаще всего вызывает «герпес» (herpes labialis) у младенцев и детей и генитальный герпес у подростков.Вирус простого герпеса также является причиной глазных инфекций у детей и поражений дистальных частей пальцев (герпетическая ямка) и других участков.
Наиболее впечатляющие результаты применения противовирусной терапии у здоровых детей были получены при использовании ацикловира при лечении гингивостоматита, вызванного простым герпесом. Недавнее исследование9 с участием 72 детей, получавших ацикловир по 15 мг на кг пять раз в день в течение семи дней, показало заметное преимущество лечения по сравнению с плацебо.Интраоральные поражения исчезли значительно быстрее (четыре дня по сравнению с 10 днями) при использовании ацикловира. Другие признаки и симптомы исчезли значительно быстрее при лечении: лихорадка (один день по сравнению с тремя днями), трудности с приемом пищи (четыре дня по сравнению с семью днями), трудности с питьем (три дня по сравнению с шестью днями) и наличие поражений вокруг рта (ноль против пяти и одного дня). -половину суток).
Гораздо большее беспокойство вызывает инфекция новорожденных, вызванная вирусом простого герпеса. Чаще всего вирус передается младенцам от матери во время родов через естественные родовые пути или, иногда, через восходящую инфекцию.
Передача инфекции гораздо более вероятна во время вагинальных родов у матери, у которой первый эпизод генитального герпеса. В таких случаях скорость передачи может составлять от 33 до 50 процентов. К сожалению, в большинстве случаев инфицированные новорожденные рождаются от женщин, у которых ни анамнез, ни физикальное обследование не свидетельствуют об активной инфекции.8 (p268)
Инфекция, вызванная простым герпесом у новорожденных, может варьироваться от местной инфекции кожи, глаз и рот к генерализованной системной инфекции или локализованной инфекции центральной нервной системы.Неонатальный менингит встречается крайне редко: недавно опубликованное исследование10 всех причин неонатального менингита в Англии и Уэльсе в период с 1975 по 1991 год выявило только 10 случаев, вызванных вирусом простого герпеса, из 26 090 зарегистрированных случаев. По этой причине AAP8 (p272) не рекомендует эмпирическое лечение младенцев, рожденных от матерей с активными первичными или рецидивирующими генитальными инфекциями герпеса, если только посевы не являются положительными или не проявляются проявления инфекции вируса простого герпеса.
Младенцы с зарегистрированными инфекциями, вызванными вирусом простого герпеса, локализованными, системными или поражающими центральную нервную систему, должны лечиться ацикловиром. Обычная доза составляет 30 мг на кг в день, вводимая внутривенно в три приема. Пациенты должны получать лечение от 14 до 21 дня.
Рибавирин против респираторно-синцитиального вируса
Рибавирин (виразол) одобрен с начала 1980-х годов для лечения респираторно-синцитиальной вирусной инфекции.Его вводят в виде аэрозоля, как правило, через кислородную палатку, надувной ящик или маску с использованием специального генератора аэрозолей мелких частиц. Первоначальное дозирование состоит из непрерывных ингаляций от 12 до 20 часов в день в течение четырех-пяти дней. Препарат также можно давать в высоких дозах по два часа трижды в день.
Недавние исследования эффективности рибавирина опровергли предыдущие результаты. В результате AAP8 (p445) , 11 изменил свои рекомендации по применению рибавирина у младенцев с высоким риском серьезного респираторно-синцитиального заболевания.Предыдущая рекомендация о том, что рибавирин «следует использовать», была изменена в последнем отчете на менее определенную «является соображением».
Два недавних исследования12,13 не подтвердили эффективность рибавирина. В одном исследовании12 сравнивалась продолжительность пребывания в больнице, количество дней кислородной терапии и количество пациентов, которым требовалась искусственная вентиляция легких, в одной больнице, которая использовала рибавирин, и в одной больнице, в которой ее не использовали. Никакой разницы в этих результатах между двумя группами не наблюдалось.Второе рандомизированное исследование13, сравнивающее рибавирин с плацебо с физиологическим раствором, также не продемонстрировало положительных результатов, измеренных по тем же стандартам. Два метаанализа подтвердили отсутствие пользы рибавирина в отношении смертности, респираторного ухудшения или продолжительности госпитализации14. В результате этой новой информации AAP рекомендует рассмотреть возможность применения рибавирина у младенцев с тяжелыми заболеваниями сердца или легких или иммуносупрессия, или у тех, кто тяжело болен.
Использование рибавирина заменяется иммунизацией внутривенным введением респираторно-синцитиального вирусного иммуноглобулина (RespiGam) у детей, которые подвержены риску развития респираторно-синцитиальной вирусной инфекции.Было показано, что использование иммуноглобулина снижает частоту госпитализаций и продолжительность госпитализации по поводу респираторно-синцитиальных вирусных инфекций или других респираторных инфекций.15 Его назначают один раз в месяц в сезон респираторно-синцитиального вируса детям в возрасте до двух лет. с бронхолегочной дисплазией, получавших или получающих кислородную терапию. Она также используется у недоношенных младенцев (менее 35 недель беременности) .16
Профилактика и лечение гриппа
Ежегодная вакцинация противогриппозной вакциной является предпочтительным методом защиты детей от гриппа, особенно тех, кто подвержен высокому риску осложнений .Вакцина недорогая, простая в применении и эффективна против вирусов гриппа как типа A, так и типа B (при условии, что они выбраны для включения в вакцину). Пероральные противовирусные средства — амантадин (симметрел) и римантадин (флумадин) — эффективны только против вирусов гриппа типа А. Однако они на 70–90 процентов эффективны в предотвращении заболеваний, вызываемых этими вирусами, и их защита начинается быстрее, чем вакцинация, что делает их полезной альтернативой, особенно во время эпидемий гриппа типа А.
Амантадин и римантадин одобрены для профилактики гриппа типа А у детей в возрасте одного года и старше.17 Эти лекарства можно назначать детям, которые впервые получают вакцину против гриппа, поскольку для развития адекватного уровня антител требуется шесть недель. Пероральные агенты не влияют на реакцию антител на вакцину.
Амантадин, но не римантадин, также предназначен для лечения гриппа типа А у детей. Своевременное лечение в течение 48 часов с момента появления симптомов снижает тяжесть и сокращает продолжительность болезни.Влияние лечения на развитие осложнений неизвестно.
Дозировки амантадина и римантадина для лечения и профилактики гриппа типа A перечислены в таблице 1. Оба агента доступны в жидкой и таблетированной или капсульной формах. Типичные затраты на одну неделю терапии составляют 10 долларов США за сироп амантадина и 12 долларов за сироп римантадина.
Просмотр / печать таблицы
ТАБЛИЦА 1Рекомендуемые дозы для лечения и профилактики амантадина (симметрел) и римантадина (флумадин)
| Противовирусное средство | От 1 до 9 лет и <40888 | 90 От 10 до 18 лет и ≥ 40 кг (88 фунтов) | Продолжительность терапии |
|---|---|---|---|
Амантадин | |||
Лечение | 5 мг на кг в день, до 150 мг в два приема | 100 мг два раза в день | До 24-48 часов после исчезновения симптомов (обычно всего семь дней) |
Профилактика | 5 мг на кг в день, до 150 мг через два дозы | 100 мг два раза в день | До шести недель (четыре недели, если пациент одновременно вакцинирован) |
Римантадин 90 901 | |||
Лечение | Неприменимо | ||
Профилактика | 5 мг на кг в день, до 150 мг в два приема 9904 9901 2 раза в день | До шести недель (четыре недели, если пациент одновременно прошел иммунизацию) | |
Рекомендуемые дозировки для лечения и профилактики амантадина (симметрел) и римантадина (флумадин)
| Противовирусное средство 9 лет и <40 кг (88 фунтов) | От 10 до 18 лет и ≥ 40 кг (88 фунтов) | Продолжительность терапии | |
|---|---|---|---|
Амантадин | |||
Лечение | 5 мг на кг в день, до 150 мг в два приема | 100 мг два раза в день | До 24-48 часов после исчезновения симптомов (обычно всего семь дней) |
Профилактика | 5 мг на кг в день, до 150 мг в два приема | 100 мг два раза в день | До шести недель (четыре недели при одновременной иммунизации) |
Римантадин | |||
Лечение | Неприменимо | ||
| 9000 за сутки до 150 мг в два приема | 100 мг два раза в день | До шести недель (четыре недели, если пациент одновременно иммунизируется) | |
Частота побочных эффектов выше у пациентов, получавших амантадин, чем у тех, кто лечился римантадином.Оба агента могут вызывать тошноту и анорексию. Побочные эффекты со стороны центральной нервной системы могут варьироваться от нервозности и головокружения до бреда, галлюцинаций и судорог. Эти побочные эффекты зависят от дозы.
Ваш ребенок и грипп: Медицинская энциклопедия MedlinePlus
СИМПТОМЫ ГРИППА У МЛАДЕНЦЕВ И ДЕТЕЙ
Грипп — это инфекция носа, горла и (иногда) легких. Если вы заметили какой-либо из следующих признаков, позвоните врачу вашего ребенка:
- Постоянная усталость и раздражительность и плохое питание
- Кашель
- Диарея и рвота
- Повышенная температура или ощущение лихорадки (при отсутствии термометра)
- Насморк
- Боли в теле и общее недомогание
КАК ЛЕЧИТЬ ГРИП У МЛАДЕНЦЕВ?
Детей младше 2 лет часто нужно лечить лекарствами, которые борются с вирусом гриппа.Это называется противовирусным препаратом. Лекарство работает лучше всего, если его начать в течение 48 часов после появления симптомов, если это возможно.
Озельтамивир (Тамифлю), вероятно, будет использоваться в жидкой форме. После обсуждения риска побочных эффектов при возможных осложнениях гриппа у вашего ребенка вы и ваш врач можете решить использовать это лекарство для лечения гриппа.
Ацетаминофен (Тайленол) и ибупрофен (Адвил, Мотрин) помогают снизить температуру у детей. Иногда ваш поставщик услуг говорит вам использовать оба типа лекарств.
Всегда проконсультируйтесь с врачом, прежде чем давать какие-либо лекарства от простуды младенцу или малышу.
ДОЛЖЕН ЛИ МОЙ РЕБЕНОК ПОЛУЧИТЬ ВАКЦИНУ ОТ ГРИПА?
Все дети в возрасте 6 месяцев и старше должны получить вакцину от гриппа, даже если они болеют гриппоподобным заболеванием. Вакцина против гриппа не одобрена для детей младше 6 месяцев.
- Вашему ребенку потребуется вторая вакцинация от гриппа примерно через 4 недели после вакцинации в первый раз.
- Есть два типа вакцины против гриппа.Один вводится в виде укола, а другой распыляется в нос вашему ребенку.
Прививка от гриппа содержит убитые (неактивные) вирусы. От вакцины этого типа невозможно заразиться гриппом. Прививка от гриппа разрешена для людей в возрасте от 6 месяцев и старше.
Вакцина против гриппа в виде назального спрея использует живой ослабленный вирус вместо мертвого, такого как прививка от гриппа. Разрешен для здоровых детей старше 2 лет.
Всем, кто живет с ребенком младше 6 месяцев или находится в тесном контакте с ним, также следует сделать прививку от гриппа.
ВРЕДИТ ЛИ ВАКЦИНА МОЕМУ РЕБЕНКУ?
Вы или ваш ребенок НЕ МОЖЕТЕ заразиться гриппом ни от одной из вакцин. У некоторых детей через день или два после прививки может возникнуть субфебрильная температура. Если развиваются более серьезные симптомы или они длятся более 2 дней, вам следует позвонить своему врачу.
Некоторые родители опасаются, что вакцина может навредить их ребенку. Но дети в возрасте до 2 лет чаще заболевают гриппом в тяжелой форме. Трудно предсказать, насколько ваш ребенок может заболеть гриппом, потому что у детей сначала часто бывает легкое заболевание.Они могут очень быстро заболеть.
Небольшое количество ртути (называемое тимеросалом) является обычным консервантом в многодозовых вакцинах. Несмотря на опасения, вакцины, содержащие тимеросал, НЕ вызывают аутизм, СДВГ или любые другие проблемы со здоровьем.
Однако все стандартные вакцины также доступны без добавления тимеросала. Спросите своего поставщика, предлагают ли они этот тип вакцины.
КАК Я МОГУ ПРЕДОТВРАТИТЬ СВОЕГО РЕБЕНКА ОТ ЗАРАЖЕНИЯ ГРИППА?
Всем, у кого есть симптомы гриппа, не следует ухаживать за новорожденным или младенцем, включая кормление.Если человеку с симптомами необходимо ухаживать за ребенком, воспитатель должен использовать маску для лица и хорошо вымыть руки. Каждый, кто находится в тесном контакте с вашим ребенком, должен делать следующее:
- Прикрывайте нос и рот салфеткой, когда кашляете или чихаете. Выбросьте салфетку после ее использования.
- Часто мойте руки водой с мылом в течение 15–20 секунд, особенно после кашля или чихания. Вы также можете использовать средства для мытья рук на спиртовой основе.
Если вашему ребенку меньше 6 месяцев и он тесно контактирует с больным гриппом, сообщите об этом своему врачу.
ЕСЛИ У МЕНЯ ЕСТЬ СИМПТОМЫ ГРИППА, МОГУ ЛИ Я КОРМЛЕНИЕ РЕБЕНКА?
Если мать не болеет гриппом, кормление грудью поощряется.
Если вы заболели, вам может потребоваться сцеживание молока для кормления из бутылочки здоровым человеком. Маловероятно, что новорожденный может заразиться гриппом от грудного молока, когда вы больны. Грудное молоко считается безопасным, если вы принимаете противовирусные препараты.
КОГДА СЛЕДУЕТ ВЫЗВАТЬ ВРАЧУ?
Поговорите с врачом вашего ребенка или обратитесь в отделение неотложной помощи, если:
- Ваш ребенок не ведет себя настороженно или не чувствует себя более комфортно, когда температура снижается.
- Симптомы лихорадки и гриппа возвращаются после того, как исчезли.
- Ребенок не плачет, когда плачет.
- Детские подгузники не мокрые, или ребенок не мочился последние 8 часов.
- У вашего ребенка проблемы с дыханием.
Безопасность Тамифлю для детей
Тамифлю (осельтамивир) — популярный пероральный противовирусный препарат, используемый для лечения или профилактики гриппа (гриппа). Несмотря на свою популярность, использование Тамифлю у детей остается несколько спорным.
Родители нередко заявляют, что это не всегда работает, читают отчеты, предполагающие, что чрезмерное употребление может привести к развитию устойчивых к лечению штаммов гриппа, или слышать, как некоторые предупреждают, что использование Тамифлю вызывает галлюцинации и суицидальные мысли у детей. Иногда бывает сложно отделить факты от вымысла, поэтому вот что говорится в исследовании.
Веривелл / Александра ГордонПреимущества
Тамифлю — один из четырех противовирусных препаратов, одобренных U.S. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) для лечения и профилактики гриппа.
К двум другим относятся внутривенный препарат Рапиваб (перамивир) и ингаляционный препарат Реленза (занамивир). В отличие от других противовирусных препаратов, используемых для лечения гриппа, эти три препарата эффективны при лечении как вирусов гриппа A, так и вирусов гриппа B.
Тамифлю был одобрен FDA специально для лечения гриппа у детей в возрасте 2 недель и старше и для профилактики гриппа у детей в возрасте 1 года и старше.Однако это не рекомендуется для легких случаев.
Согласно отчету Центров по контролю и профилактике заболеваний (CDC), использование этих противовирусных препаратов дает ряд преимуществ. Главный из них — профилактика гриппа.
Профилактика гриппа
Противовирусные препараты эффективны в предотвращении гриппа от 70% до 90%, поэтому они важны для профилактики гриппа у детей, которые подвержены высокому риску осложнений в течение 48 часов после заражения.
Считается, что дети подвержены высокому риску осложнений гриппа, таких как пневмония и дыхательная недостаточность, если они моложе 5 лет и / или у них есть основное заболевание, такое как астма, заболевание легких, диабет, эпилепсия, болезнь сердца, почек. или проблемы с печенью, заболевания крови, рак, иммунодефицит или церебральный паралич.
Эти препараты также являются источником профилактики для подвергшихся воздействию детей детей, которые не могут получить прививку от гриппа, например, тех, у кого ранее была аллергическая реакция на вакцину.
Прочие льготы
Другие преимущества, определенные CDC, включают:
- Сокращение продолжительности и тяжести симптомов : Использование противовирусных препаратов, таких как Тамифлю, в течение 48 часов после появления симптомов, может уменьшить продолжительность симптомов гриппа, а также уменьшить их тяжесть.
- Снижение риска осложнений : Противовирусные препараты могут снизить риск осложнений, которые могут возникнуть при гриппе, включая пневмонию, ушные инфекции, госпитализацию и дыхательную недостаточность.
- Более короткое пребывание в больнице : Когда дети госпитализируются из-за гриппа, раннее противовирусное лечение может сократить продолжительность их госпитализации и помочь предотвратить дыхательную недостаточность или смерть. Даже если у вашего ребенка прошло 48-часовое окно, противовирусный препарат все равно может помочь.
- Эффективен для младенцев : Хотя это не одобрено FDA, CDC и Американская академия педиатрии (AAP) рекомендуют использовать Тамифлю для лечения детей в возрасте до 14 дней с гриппом и для профилактики гриппа у детей в возрасте от 3 месяцев до 1 года. год, так как у этих детей особенно высок риск осложнений от гриппа.
Минусы
Несмотря на доказательства, подтверждающие использование Тамифлю у детей, существует ряд препятствий, мешающих родителям использовать его.
Стоимость
Цена — главная проблема, так как пятидневный курс без страховки стоит более 100 долларов. Хотя сейчас доступны более дешевые дженерики, цена по-прежнему высока. Если вашему ребенку нужен Тамифлю, попробуйте поискать в Интернете скидки по рецептам и купоны.
Не понимаю, как это работает
Некоторые родители не верят, что Тамифлю действительно работает. Однако в большинстве случаев это связано больше с неправильным его использованием или нереалистичными ожиданиями, чем с самим наркотиком.
Фактически, эффективность Тамифлю может варьироваться в зависимости от того, когда начато лечение. С этой целью большинство врачей рекомендуют принимать препарат в течение 48 часов с момента появления первых симптомов.
Проблема, конечно, в том, что родители могут иногда пропускать или игнорировать незначительные симптомы, такие как насморк или першение в горле, на день или два, особенно если в остальном ребенок выглядит здоровым.
Более того, хотя некоторые люди думают, что Тамифлю должен немедленно убить вирус гриппа и устранить все симптомы, дело в том, что он не работает как антибиотик, хотя, вероятно, уменьшит продолжительность болезни вашего ребенка.Тамифлю также не действует на другие виды вирусов, поэтому он не поможет, если он или она болеют чем-то, кроме гриппа.
Не использовать для профилактики
Тамифлю может быть чрезвычайно эффективным средством профилактики гриппа у ребенка, который еще не был вакцинирован или который находится в группе высокого риска осложнений и был рядом с другими больными гриппом. Однако, поскольку преимущества в значительной степени незаметны, родители часто обращаются к нему только при появлении симптомов, а не используют его для профилактики.Это ошибка.
Детей из группы высокого риска следует лечить Тамифлю как можно скорее после заражения гриппом.
Побочные эффекты
Родители часто связывают цену с потенцией и опасаются, что такой препарат, как Тамифлю, может вызвать больше симптомов, чем облегчить. По большей части это неправда.
По данным FDA, двумя наиболее распространенными побочными эффектами являются тошнота и рвота, которые обычно не так серьезны и возникают в течение двух дней после начала лечения.Прием Тамифлю с пищей обычно снижает риск этих побочных эффектов. Другие побочные эффекты могут включать легкую боль в животе, кровотечение из носа, головную боль и усталость.
Сообщалось о более серьезных побочных эффектах. В сообщениях, поступающих в основном из Японии в 2005 и 2006 годах, предполагается, что Тамифлю увеличивает риск психоневрологических симптомов, таких как делирий и галлюцинации, и может вызвать у подростков мысли о самоповреждении или самоубийстве.
На сегодняшний день о подобных событиях не сообщалось, и дальнейшие исследования не обнаружили повышенного риска нейропсихиатрических эффектов у пользователей Тамифлю.Однако обновленные этикетки продуктов теперь содержат информацию о том, что галлюцинации, членовредительство, ненормальное поведение и суицидальные мысли возможны, хотя и встречаются крайне редко.
Если вы заметили какие-либо серьезные побочные эффекты, пока ваш ребенок принимает Тамифлю, немедленно обратитесь к врачу.
Устойчивость к противовирусным препаратам
Как и в случае с антибиотиками, используемыми для лечения бактериальных инфекций, давно существуют опасения, что широкое использование противовирусных препаратов от гриппа может привести к развитию супервируса.На сегодняшний день мы этого не видели.
Поскольку вирусы гриппа могут меняться так быстро, CDC регулярно проверяет устойчивость к противовирусным препаратам и практически не обнаружил устойчивости в течение последних сезонов гриппа.