— фракции белков крови — Биохимия
Плазма крови человека в норме содержит более 100 видов белков. Примерно 90% всего белка крови составляют альбумины, иммуноглобулины, липопротеины, фибриноген, трансферрин; другие белки присутствуют в плазме в небольших количествах.
Синтез белков плазмы крови осуществляют:
- печень – полностью синтезирует фибриноген и альбумины крови, большую часть α- и β-глобулинов,
- клетки ретикулоэндотелиальной системы (РЭС) костного мозга и лимфатических узлов – часть β-глобулинов и γ-глобулины (иммуноглобулины).
Существует довольно много различных методов разделения белков в зависимости от их некоторых качеств. Наиболее распространенным методом фракционирования белков крови является электрофорез..
Электрофорез белков
Ацетатцеллюлозная пленка, гель, специальная бумага (носитель) помещается на рамку, при этом противоположные края носителя свисают в кюветы с буферным раствором. На линию старта наносится сыворотка крови. Метод заключается в движении заряженых молекул белка по поверхности носителя под влиянием электрического поля. Молекулы с наибольшим отрицательным зарядом и наименьшим размером, т.е. альбумины, двигаются быстрее остальных. Наиболее крупные и нейтральные (γ-глобулины) оказываются последними.
На ход электрофореза влияет подвижность разделяемых веществ, находящаяся в зависимости от ряда факторов: заряд белков, величина электрического поля, состав растворителя (буферной смеси), тип носителя (бумага, пленка, гель).
Общий вид электрофореза
Количество выделяемых фракций определяется условиями проведения электрофореза. При электрофорезе на бумаге и пленках ацетата целлюлозы в клинико-диагностических лабораториях выделяют 5 фракций (альбумины, α1-, α2-, β- и γ-глобулины), в то время как в полиакриламидном геле – до 20 и более фракций. При использовании более совершенных методов (радиальная иммунодиффузия, иммуноэлектрофорез и других) в составе глобулиновых фракций выявляются многочисленные индивидуальные белки.
Электрофореграмма (вверху) и графический результат ее обработки (внизу)
На вид протеинограммы оказывают влияние только те белки, концентрация которых достаточно высока.
Нормальные величины белковых фракций плазмы крови
| Общий белок | взрослые | 65-85 г/л |
| дети 1-3 года | 55-85 г/л | |
| Белковые фракции | ||
| Альбумины | 50-70 % | 30-50 г/л |
| α1-Глобулины | 3-6 % | 1-3 г/л |
| α2-Глобулины | 9-15 % | 6-10 г/л |
| β-Глобулины | 8-18 % | 7-11 г/л |
| γ-Глобулины | 15-25 % | 8-16 г/л |
Нормальные величины фракций белков в ликворе и моче можно посмотреть здесь.
Особенности содержания белков в крови у детей
У новорожденных содержание общего белка в сыворотке крови значительно ниже, чем у взрослых, и становится минимальным к концу первого месяца жизни (до 48 г/л). Ко второму-третьему годам жизни общий белок повышается до уровня взрослых.
В течение первых месяцев жизни концентрация глобулиновых фракций низка, что приводит к относительной гиперальбуминемии до 66-76%. В периоде между 2-м и 12-м месяцами концентрация α2-глобулинов временно превышает взрослый уровень.
Количество фибриногена при рождении гораздо ниже, чем у взрослых (около 2,0 г/л), но к концу первого месяца достигает обычной нормы (4,0 г/л).
Типы протеинограмм
В клинической практике для сыворотки выделяют 10 типов электрофореграмм (протеинограмм), соответствующих различным патологическим состояниям.
Тип протеинограммы |
Альбумины |
Фракции глобулинов |
Примеры заболеваний |
|||
| α1 | α2 | β | γ | |||
| Острые воспаления | ↓↓ | ↑ | ↑ | — | ↑ | Начальные стадии пневмоний, острые полиартриты, экссудативный туберкулез легких, острые инфекционные заболевания, сепсис, инфаркт миокарда |
| Хронические воспаления | ↓ | — | ↑↑ |
↑↑ | Поздние стадии пневмоний, хронический туберкулез легких, хронический эндокардит, холецистит, цистит и пиелит | |
| Нарушения почечного фильтра |
↓↓ |
— | ↑ | ↑ | ↓ | Генуинный, липоидный или амилоидный нефроз, нефрит, нефросклероз, токсикоз беременности, терминальные стадии туберкулеза легких, кахексии |
| Злокачественные опухоли |
↓↓ |
↑↑ | ↑↑ | ↑↑↑ | ↑↑ | Метастатические новообразования с различной локализацией первичной опухоли |
| Гепатиты | ↓ | — | — | ↑ | ↑↑ | Последствия токсического повреждения печени, гепатиты, гемолитические процессы, лейкемии, злокачественные новообразования кроветворного и лимфатического аппарата, некоторые формы полиартрита, дерматозы |
| Некроз печени | ↓↓ | — | ↓ | ↑ | ↑↑ | Цирроз печени, тяжелые формы индуративного туберкулеза легких, некоторые формы хронического полиартрита и коллагенозов |
| Механические желтухи | ↓ | — | ↑ | ↑ | Обтурационная желтуха, желтухи, вызванные развитием рака желчевыводящих путей и головки поджелудочной железы | |
| α2-глобулиновые плазмоцитомы | ↓ | ↓ | ↑↑ | ↓ | ↓ | α2-Плазмоцитомы |
| β-глобулиновые плазмоцитомы | ↓ | ↓ | ↓ | ↑↑ | ↓ | β1-Плазмоцитомы, β1-плазмоклеточная лейкемия и макроглобулинемия Вальденштрема |
| γ-глобулиновые плазмоцитомы | ↓ | ↓ | ↓ | ↓ | ↑↑ | γ-Плазмоцитомы, макроглобулинемия и некоторые ретикулезы |
|
На вид протеинограммы оказывают влияние только те белки, концентрация которых достаточно высока. Нормальные величины белковых фракций плазмы крови
Особенности содержания белков в крови у детей У новорожденных содержание общего белка в сыворотке крови значительно ниже, чем у взрослых, и становится минимальным к концу первого месяца жизни (до 48 г/л). Ко второму-третьему годам жизни общий белок повышается до уровня взрослых. В течение первых месяцев жизни концентрация глобулиновых фракций низка, что приводит к относительной гиперальбуминемии до 66-76%. В периоде между 2-м и 12-м месяцами концентрация α2-глобулинов временно превышает взрослый уровень. Количество фибриногена при рождении гораздо ниже, чем у взрослых (около 2,0 г/л), но к концу первого месяца достигает обычной нормы (4,0 г/л). Типы протеинограмм В клинической практике для сыворотки выделяют 10 типов электрофореграмм (протеинограмм), соответствующих различным патологическим состояниям.
Типы гиперлипидемий Классификация типов гиперлипидемий была разработана Дональдом Фредиксоном в 1965 году и была принята Всемирной организацией здравоохранения в качестве международного стандарта. Она используется до сих пор.
Согласно классификации Фредиксона, существует пять типов гиперлипидемий.
— Тип I. Это редкий тип гиперлипидемии, развивается при недостаточности липопротеинлипазы или дефекте в белке-активаторе липопротеинлипазы. При этом типе заболевания повышается уровень хиломикронов (липопротеины, которые переносят липиды из кишечника в печень). Гиперлипидемия усугубляется после приема жирной пищи и снижается после ограничения жиров, поэтому основное лечение — это назначение диеты.
— Тип II. Распространенный тип гиперлипидемии, при котором повышается уровень липопротеинов низкой плотности. Подразделяется на два подтипа в зависимости от наличия высоких триглицеридов, которые при лечении требуют дополнительного назначения гемфиброзила. Гиперлипидемия этого типа приводит к развитию атеросклероза после 20-30 лет и может стать причиной инфаркта в возрасте 40-50 дет у мужчин и 55-60 лет у женщин.
— Тип III. Тип гиперлипидемии, который еще называют дис-бета-липопротеиненией. Заболевание характеризуется наследственными причинами, и связан с дефектом Аполипопротеина E, а также характеризуется повышением уровня липопротеинов повышенной плотности. Носители гиперлипидемии склонны к ожирению, подагре, легкой форме сахарного диабета и входят в группу риска по атеросклерозу.
— Тип IV. Тип гиперлипидемии, для которого характерна повышенная концентрация триглицеридов. Их уровень повышается после приема углеводов и алкоголя. На фоне этого синдрома может развиться атеросклероз, ожирение, сахарный диабет и панкреатит. — — Тип V. Тип гиперлипидемии, похожий на первый, но в отличие от него повышается не только уровень хиломикронов, но и липопротеинов очень низкой плотности. Поэтому, как и в случае с первым типом, содержание жиров в крови подскакивает после приема жирной и углеводной пищи. Гиперлипидемия этого типа чревата развитием тяжелого панкреатита, который развивается на фоне приема слишком жирной пищи. Помимо этой классификации существуют еще два типа гиперлипидемии — гипо-альфа-липопротеинемия и гипо-бета-липопротеинемия. Читайте также: Рекомендуемые страницы: Поиск по сайту |
Поиск по сайту: |
Общий вид электрофореза
Количество выделяемых фракций определяется условиями проведения электрофореза. При электрофорезе на бумаге и пленках ацетата целлюлозы в клинико-диагностических лабораториях выделяют 5 фракций (альбумины, α1-, α2-, β- и γ-глобулины), в то время как в полиакриламидном геле – до 20 и более фракций. При использовании более совершенных методов (радиальная иммунодиффузия, иммуноэлектрофорез и других) в составе глобулиновых фракций выявляются многочисленные индивидуальные белки.
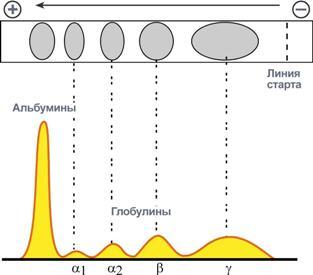
Электрофореграмма (вверху) и графический результат ее обработки (внизу)
На вид протеинограммы оказывают влияние только те белки, концентрация которых достаточно высока.
Нормальные величины белковых фракций плазмы крови
Общий белок | взрослые | 65-85 г/л |
дети 1-3 года | 55-85 г/л | |
Белковые фракции | ||
Альбумины | 50-70 % | 30-50 г/л |
α1-Глобулины | 3-6 % | 1-3 г/л |
α2-Глобулины | 9-15 % | 6-10 г/л |
β-Глобулины | 8-18 % | 7-11 г/л |
γ-Глобулины | 15-25 % | 8-16 г/л |
У новорожденных содержание общего белка в сыворотке крови значительно ниже, чем у взрослых, и становится минимальным к концу первого месяца жизни (до 48 г/л). Ко второму-третьему годам жизни общий белок повышается до уровня взрослых.
В течение первых месяцев жизни концентрация глобулиновых фракций низка, что приводит к относительной гиперальбуминемии до 66-76%. В периоде между 2-м и 12-м месяцами концентрация α2-глобулинов временно превышает взрослый уровень.
Количество фибриногена при рождении гораздо ниже, чем у взрослых (около 2,0 г/л), но к концу первого месяца достигает обычной нормы (4,0 г/л).
Типы протеинограмм
В клинической практике для сыворотки выделяют 10 типов электрофореграмм (протеинограмм), соответствующих различным патологическим состояниям.
Тип протеинограммы | Альбумины | Фракции глобулинов | Примеры заболеваний | ||||
α1 | α2 | β | γ | ||||
Острые воспаления | ↓↓ | ↑ | ↑ | — | ↑ | Начальные стадии пневмоний, острые полиартриты, экссудативный туберкулез легких, острые инфекционные заболевания, сепсис, инфаркт миокарда | |
Хронические воспаления | ↓ | — | ↑↑ | — | ↑↑ | Поздние стадии пневмоний, хронический туберкулез легких, хронический эндокардит, холецистит, цистит и пиелит | |
Нарушения почечного фильтра | ↓↓ | — | ↑ | ↑ | ↓ | Генуинный, липоидный или амилоидный нефроз, нефрит, нефросклероз, токсикоз беременности, терминальные стадии туберкулеза легких, кахексии | |
Злокачественные опухоли | ↓↓ | ↑↑ | ↑↑ | ↑↑↑ | ↑↑ | Метастатические новообразования с различной локализацией первичной опухоли | |
Гепатиты | ↓ | — | — | ↑ | ↑↑ | Последствия токсического повреждения печени, гепатиты, гемолитические процессы, лейкемии, злокачественные новообразования кроветворного и лимфатического аппарата, некоторые формы полиартрита, дерматозы | |
Некроз печени | ↓↓ | — | ↓ | ↑ | ↑↑ | Цирроз печени, тяжелые формы индуративного туберкулеза легких, некоторые формы хронического полиартрита и коллагенозов | |
Механические желтухи | ↓ | — | ↑ | ↑ | ↑ | Обтурационная желтуха, желтухи, вызванные развитием рака желчевыводящих путей и головки поджелудочной железы | |
α2-глобулиновые плазмоцитомы | ↓ | ↓ | ↑↑ | ↓ | ↓ | α2-Плазмоцитомы | |
β-глобулиновые плазмоцитомы | ↓ | ↓ | ↓ | ↑↑ | ↓ | β1-Плазмоцитомы, β1-плазмоклеточная лейкемия и макроглобулинемия Вальденштрема | |
γ-глобулиновые плазмоцитомы | ↓ | ↓ | ↓ | ↓ | ↑↑ | γ-Плазмоцитомы, макроглобулинемия и некоторые ретикулезы | |
Общий вид электрофореза
Количество выделяемых фракций определяется условиями проведения электрофореза. При электрофорезе на бумаге и пленках ацетата целлюлозы в клинико-диагностических лабораториях выделяют 5 фракций (альбумины, α1-, α2-, β- и γ-глобулины), в то время как в полиакриламидном геле – до 20 и более фракций. При использовании более совершенных методов (радиальная иммунодиффузия, иммуноэлектрофорез и других) в составе глобулиновых фракций выявляются многочисленные индивидуальные белки.
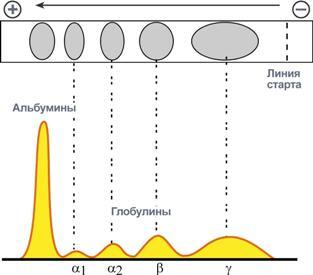
Электрофореграмма (вверху) и графический результат ее обработки (внизу)
На вид протеинограммы оказывают влияние только те белки, концентрация которых достаточно высока.
Нормальные величины белковых фракций плазмы крови
Общий белок | взрослые | 65-85 г/л |
дети 1-3 года | 55-85 г/л | |
Белковые фракции | ||
Альбумины | 50-70 % | 30-50 г/л |
α1-Глобулины | 3-6 % | 1-3 г/л |
α2-Глобулины | 9-15 % | 6-10 г/л |
β-Глобулины | 8-18 % | 7-11 г/л |
γ-Глобулины | 15-25 % | 8-16 г/л |
У новорожденных содержание общего белка в сыворотке крови значительно ниже, чем у взрослых, и становится минимальным к концу первого месяца жизни (до 48 г/л). Ко второму-третьему годам жизни общий белок повышается до уровня взрослых.
В течение первых месяцев жизни концентрация глобулиновых фракций низка, что приводит к относительной гиперальбуминемии до 66-76%. В периоде между 2-м и 12-м месяцами концентрация α2-глобулинов временно превышает взрослый уровень.
Количество фибриногена при рождении гораздо ниже, чем у взрослых (около 2,0 г/л), но к концу первого месяца достигает обычной нормы (4,0 г/л).
Типы протеинограмм
В клинической практике для сыворотки выделяют 10 типов электрофореграмм (протеинограмм), соответствующих различным патологическим состояниям.
Тип протеинограммы | Альбумины | Фракции глобулинов | Примеры заболеваний | ||||
α1 | α2 | β | γ | ||||
Острые воспаления | ↓↓ | ↑ | ↑ | — | ↑ | Начальные стадии пневмоний, острые полиартриты, экссудативный туберкулез легких, острые инфекционные заболевания, сепсис, инфаркт миокарда | |
Хронические воспаления | ↓ | — | ↑↑ | — | ↑↑ | Поздние стадии пневмоний, хронический туберкулез легких, хронический эндокардит, холецистит, цистит и пиелит | |
Нарушения почечного фильтра | ↓↓ | — | ↑ | ↑ | ↓ | Генуинный, липоидный или амилоидный нефроз, нефрит, нефросклероз, токсикоз беременности, терминальные стадии туберкулеза легких, кахексии | |
Злокачественные опухоли | ↓↓ | ↑↑ | ↑↑ | ↑↑↑ | ↑↑ | Метастатические новообразования с различной локализацией первичной опухоли | |
Гепатиты | ↓ | — | — | ↑ | ↑↑ | Последствия токсического повреждения печени, гепатиты, гемолитические процессы, лейкемии, злокачественные новообразования кроветворного и лимфатического аппарата, некоторые формы полиартрита, дерматозы | |
Некроз печени | ↓↓ | — | ↓ | ↑ | ↑↑ | Цирроз печени, тяжелые формы индуративного туберкулеза легких, некоторые формы хронического полиартрита и коллагенозов | |
Механические желтухи | ↓ | — | ↑ | ↑ | ↑ | Обтурационная желтуха, желтухи, вызванные развитием рака желчевыводящих путей и головки поджелудочной железы | |
α2-глобулиновые плазмоцитомы | ↓ | ↓ | ↑↑ | ↓ | ↓ | α2-Плазмоцитомы | |
β-глобулиновые плазмоцитомы | ↓ | ↓ | ↓ | ↑↑ | ↓ | β1-Плазмоцитомы, β1-плазмоклеточная лейкемия и макроглобулинемия Вальденштрема | |
γ-глобулиновые плазмоцитомы | ↓ | ↓ | ↓ | ↓ | ↑↑ | γ-Плазмоцитомы, макроглобулинемия и некоторые ретикулезы | |
Электрофореграмма (вверху) и графический результат ее обработки (внизу)
⇐ ПредыдущаяСтр 72 из 89Следующая ⇒
На вид протеинограммы оказывают влияние только те белки, концентрация которых достаточно высока.
Нормальные величины белковых фракций плазмы крови
| Общий белок | взрослые | 65-85 г/л |
| дети 1-3 года | 55-85 г/л | |
| Белковые фракции | ||
| Альбумины | 50-70 % | 30-50 г/л |
| α1-Глобулины | 3-6 % | 1-3 г/л |
| α2-Глобулины | 9-15 % | 6-10 г/л |
| β-Глобулины | 8-18 % | 7-11 г/л |
| γ-Глобулины | 15-25 % | 8-16 г/л |
Особенности содержания белков в крови у детей
У новорожденных содержание общего белка в сыворотке крови значительно ниже, чем у взрослых, и становится минимальным к концу первого месяца жизни (до 48 г/л). Ко второму-третьему годам жизни общий белок повышается до уровня взрослых.
В течение первых месяцев жизни концентрация глобулиновых фракций низка, что приводит к относительной гиперальбуминемии до 66-76%. В периоде между 2-м и 12-м месяцами концентрация α2-глобулинов временно превышает взрослый уровень.
Количество фибриногена при рождении гораздо ниже, чем у взрослых (около 2,0 г/л), но к концу первого месяца достигает обычной нормы (4,0 г/л).
Типы протеинограмм
В клинической практике для сыворотки выделяют 10 типов электрофореграмм (протеинограмм), соответствующих различным патологическим состояниям.
| Тип протеинограммы | Альбумины | Фракции глобулинов | Примеры заболеваний | |||
| α1 | α2 | β | γ | |||
| Острые воспаления | ↓↓ | ↑ | ↑ | — | ↑ | Начальные стадии пневмоний, острые полиартриты, экссудативный туберкулез легких, острые инфекционные заболевания, сепсис, инфаркт миокарда |
| Хронические воспаления | ↓ | — | ↑↑ | — | ↑↑ | Поздние стадии пневмоний, хронический туберкулез легких, хронический эндокардит, холецистит, цистит и пиелит |
| Нарушения почечного фильтра | ↓↓ | — | ↑ | ↑ | ↓ | Генуинный, липоидный или амилоидный нефроз, нефрит, нефросклероз, токсикоз беременности, терминальные стадии туберкулеза легких, кахексии |
| Злокачественные опухоли | ↓↓ | ↑↑ | ↑↑ | ↑↑↑ | ↑↑ | Метастатические новообразования с различной локализацией первичной опухоли |
| Гепатиты | ↓ | — | — | ↑ | ↑↑ | Последствия токсического повреждения печени, гепатиты, гемолитические процессы, лейкемии, злокачественные новообразования кроветворного и лимфатического аппарата, некоторые формы полиартрита, дерматозы |
| Некроз печени | ↓↓ | — | ↓ | ↑ | ↑↑ | Цирроз печени, тяжелые формы индуративного туберкулеза легких, некоторые формы хронического полиартрита и коллагенозов |
| Механические желтухи | ↓ | — | ↑ | ↑ | ↑ | Обтурационная желтуха, желтухи, вызванные развитием рака желчевыводящих путей и головки поджелудочной железы |
| α2-глобулиновые плазмоцитомы | ↓ | ↓ | ↑↑ | ↓ | ↓ | α2-Плазмоцитомы |
| β-глобулиновые плазмоцитомы | ↓ | ↓ | ↓ | ↑↑ | ↓ | β1-Плазмоцитомы, β1-плазмоклеточная лейкемия и макроглобулинемия Вальденштрема |
| γ-глобулиновые плазмоцитомы | ↓ | ↓ | ↓ | ↓ | ↑↑ | γ-Плазмоцитомы, макроглобулинемия и некоторые ретикулезы |
Белки крови выполняют серьезные задачи
Функции белков плазмы крови
Многообразие белков крови приводит к тому, что они обладают многочисленными функциями:
· поддерживают постоянство коллоидно-осмотического давления крови – в первую очередь, альбумины,;
· участвуют в регуляции кислотно-основного состояния – альбумины, гемоглобин,
· удерживают в связанном состоянии и транспортируют ионы кальция, магния, железа, меди и другие ионы, препятствуя их потере с мочой – альбумины и специфические транспортные белки,
· связываюти транспортируют органические вещества (углеводы, липиды, гормоны, лекарства, витамины, токсины) – альбумины и другие белки,
· определяют вязкость крови и сохраняют устойчивость эритроцитов и лейкоцитов в кровотоке, обеспечивают нормальный кровоток в капиллярах (реологические свойства крови) – белки свертывающей системы,
· специализированные белки, участвующие в свертывании крови (фибриноген, протромбин, антигемофильный глобулин и др.),
· обеспечивают иммунную защиту организма – иммуноглобулины, факторы системы комплемента, трансферрин и пропердин,
· обеспечивают неспецифическую защиту организма при повреждении тканей – белки острой фазы.
Общая биохимияБиохимия азотистых веществ кровиБелки острой фазы — быстро реагирующие белки
Белки острой фазы — быстро реагирующие белки
Белки острой фазы – большая группа белков сыворотки крови (в основном α-глобулинов) с молекулярной массой от 12 кДа до 340 кДа и различными функциями, объединенных по общему признаку – быстрое изначительное увеличение концентрации при бактериальной, вирусной, паразитарной инфекции, физической или химической травме, токсической или аутоиммунной реакции, злокачественныхновообразованиях. Смысл данного увеличения заключается в повышении резистентности клеток к окислению, в ограничении повреждения тканей, в подавлении скорости размножения бактерий.
Синтезбелков острой фазы осуществляется печенью, моноцитами, лимфоцитами, нейтрофилами. Их концентрация зависят от стадии заболевания и/или от масштабов повреждений. Синтез белков включается и регулируется рядом медиаторов, среди которых цитокины, анафилотоксины и глюкокортикоиды.
К белкам острой фазы относят С-реактивный белок, сывороточный амилоид А, гаптоглобин, α2-макроглобулин, церулоплазмин, α1-гликопротеин, α1-антитрипсин, орозомукоид, компоненты комплементаС1-С4, С9. Трансферринтакже относят к белкам острой фазы, но его концентрация при воспалениях снижается – его называют негативнымбелком острой фазы.
Увеличение концентрации белков острой фазы в крови является хорошим индикатором не только явного, но и скрытого воспаления (например, атеросклероз).
Альбумин — основной белок крови
Белок синтезируется почти исключительно в печени. Хотя по классификации его относят к простым белкам, отмечается широкая микрогетерогенность молекул альбумина, что связано с количеством и качеством агрегированных с альбумином молекул.
Значение альбумина в крови заключается:
1. В поддержании коллоидно-осмотического давления;
2. Он является богатым и быстро реализуемым резервом белка;
3. Транспортная– альбумин переносит
· длинноцепочечные жирные кислоты – основная физиологическая функция сывороточного альбумина.
· пигменты (билирубин),
· катионы(например, Ca2+ и Mg2+), анионы (Cl–),
· желчные кислоты,
· витамины,
· гормоны (альдостерон, прогестерон, гидрокортизон),
· органические красители,
· лекарственные вещества (дигоксин, барбитураты, пенициллин, ацетилсалициловая кислота, сердечные гликозиды).
Изменения количества белка в крови могут иметь как абсолютный (истинный), так и относительныйхарактер. Сдвиги абсолютного характера являются следствием колебаний содержания белка в крови. В свою очередь, относительные изменения зависят от объема крови, т.е. наблюдаются при обезвоживании или гипергидратации.
Гиперальбуминемия
Истинноеповышение концентрации белка в крови обычно не наблюдается.
Относительная гиперальбуминемия вызывается потерями внутрисосудистой жидкости в результате профузных поносов (например, холере), усиленном потоотделении, неукротимой рвоте, несахарном диабете, при тяжелых и обширных ожогах и генерализованных перитонитах.
Гипоальбуминемия
Истинная (абсолютная) гипоальбуминемия связана:
· с недостаточным потреблением белка с пищей – заболевания желудочно-кишечного тракта, сужение пищевода при опухолях, частичное или полное голодание;
· со снижением синтеза белка в печени – несбалансированный аминокислотный состав пищи, хронические паренхиматозные гепатиты, интоксикации, злокачественные новообразования, лечение кортикостероидами;
· с усиленным распадом белка – кахексия, тяжелые инфекции, длительные воспалительные процессы, лихорадочные состояния, тиреотоксикозы;
· с потерей белка – нарушения проницаемости капиллярных стенок, кровоизлияния, ожоги, острые и хронические кровотечения, нефротический синдром.
Относительная гипоальбуминемия связана с нарушением водного баланса – гипергидратация при гиперальдостеронизме, при почечной недостаточности со снижением экскреции солей, при использовании для питья морской воды, при неадекватных инфузиях солевых растворов.
Рекомендуемые страницы:
Типы электрофореза — Наука и Техника — Каталог статей
Электрофорез — это способ разделения биологических молекул в электрическом поле, основанный на том факте, что разные молекулы имеют разные естественные электрические заряды, связанные с ними. Это заставляет различные компоненты вещества двигаться с разными скоростями под воздействием электрического поля. Представьте себе, что на подносе есть коллекция маленьких кусочков разных металлов, и на один конец подноса положили магнит. Различные куски металла (эквивалентные «молекулам») будут притягиваться к магниту в разной степени в зависимости от их удельных зарядов. По сути, это то, что происходит при электрофорезе, за исключением того, что молекулы изначально не разделены.
Различные виды электрофореза сегодня практикуются.
Принцип электрофореза
Причиной работы электрофореза является одно из фундаментальных уравнений физики электромагнетизма: сила равна электрическому заряду, умноженному на напряженность поля в этой точке. Это принимает форму:
F = qE
Где F = сила, q = электрический заряд и E = напряженность электрического поля.
Это уравнение подразумевает, что чем выше заряд на частице, тем сильнее сила, возникающая в результате приложения данного электрического поля. Это означает, что две частицы с одинаковой массой, но разными зарядами будут двигаться с разной скоростью через поле. Кроме того, скорость, с которой движется любая заряженная молекула, зависит от ее отношения заряда к массе. Вместе эти свойства и отношения позволяют ученым разделить компоненты критических биомолекул, таких как нуклеиновые кислоты, на их более мелкие компоненты.
Гель-электрофорез
Используются три основных типа гель-электрофореза. Электрофорез крахмального геля, который использует гранулы картофельного крахмала, является чем-то вроде реликвии. При электрофорезе в агарозном геле в качестве среды используется очищенный полисахарид с большой молекулярной массой; это обычно используется для больших молекул ДНК. Электрофорез в полиакриламидном геле является наиболее распространенным типом, потому что он чрезвычайно стабилен и работает в широком диапазоне концентраций молекул.
Менее распространенные виды электрофореза
Гель-электрофорез в некотором роде предпочтителен в большинстве экспериментальных ситуаций. Другие распространенные методы включают электрофорез высокого разрешения, капиллярный электрофорез, изоэлектрическое фокусирование, иммунохимический электрофорез, двумерный электрофорез и электрофорез в импульсном поле.
Типы установок электрофореза
Инструменты электрофореза имеют такое же большое значение, как и конкретная используемая среда. В старые времена пограничный электрофорез был стандартом. В этой экспериментальной установке измеряется скорость движения всей границы мигрирующих молекул. Сегодня зональный электрофорез является более распространенным явлением, когда молекулы мигрируют в разные области или зоны на небольшом участке бумаги. Это более целенаправленный подход, чем пограничный электрофорез. Наконец, бумажный электрофорез иногда используется для небольших молекул.
Электрофореграмма — Справочник химика 21
Нингидрин, 0,5%-ный раствор в ацетоне. Для окрашивания электрофореграмм применяют смесь из 95 частей этого раствора и 5 частей дистиллированной воды. [c.150]Проявив электрофореграмму, по окраске пятен судят [c.126]
Белковые смеси анализируют электрофорезом на бумаге. Хроматографическую бумагу пропитывают буферным раствором, поддерживая тем самым необходимое значение pH. Наносят анализируемую смесь и создают электрическое напряжение. По истечении определенного времени (оно зависит от свойств разделяемых белков, носителя и приложенной разности потенциалов) проявляют электрофореграммы химическими и биохимическими методами. [c.216]
Электрофорез применяют для очистки различных фармацевтических препаратов. В Фармакопее СССР (изд. 10) предусмотрено установление степени чистоты по электрофоретической однородности ряда антибиотиков, витаминов и других веществ. Электрофорез (ионофорез) является одним из методов введения лечебных препаратов в организм человека. Широкое применение как аналитический и препаративный метод разделения и выделения различных лекарственных веществ и биологически активных соединений нашел электрофорез на бумаге, а также в агаровом или крахмальном геле. Эти методы применяют также при диагностике ряда заболеваний путем сравнения фракционного состава (по числу и интенсивности зон на электрофореграмме) нормальных и патологических биологических жидкостей. [c.408]
Так как различные аминокислоты в данном буферном растворе могут обладать разным по величине и знаку зарядом, то скорость и направление их перемещения в электрическом поле также будут отличаться. Благодаря этому смесь аминокислот можно разделить на отдельные компоненты. Число компонентов и их соотношение в смеси определяют после специальной обработки бумажных полосок, на которых проводится разделение (электрофореграмм). В результате обработки на электрофореграмме появляются окрашенные полосы, каждая из которых соответствует определенному компоненту. [c.148]
Определение соотношения количеств аминокислот основано на измерении оптической плотности растворов медного производного, полученных при обработке отдельных участков электрофореграмм спиртовым раствором сульфата меди. Измерения следует проводить в достаточно разбавленных растворах, чтобы соблюдалась линейная зависимость между содержанием аминокислоты и оптической плотностью раствора. Оптимальные для колориметрических определений концентрации аминокислоты находятся в пределах 0,05— [c.149]
Белки, обработанные концентрированным раствором додецилсуль-фата натрия в присутствии р-меркаптоэтанола, распадаются на отдельные полипептидные цепи и приобретают отрицательный заряд, значительно превышающий собственный заряд белковой молекулы. При последующем разделении с помощью диск-электрофореза в полиакриламидном геле белковые зоны распределяются на электрофореграммах таким образом, что подвижность белковой зоны обратно пропорциональна логарифму молекулярной массы. Метод дает возможность определять молекулярные массы субъединиц олигомерных белков. Электрофоретическое разделение можно проводить различными методами. Ниже описаны два из них метод Вебера и Осборн, а также метод, предложенный Лэммли. [c.119]
| Рис. 84. Электрофореграмма плазмы крови а—в но ме б — прн нефрите |
Абсцисса каждого пика дает значение VI, характерное для данного компонента и позволяющее провести идентификацию площадь под пиком пропорциональна С1. Таким образом, электрофореграммы позволяют осуществить не только качественный, но и количественный анализ в сравнительно мягких условиях, поскольку в слабом электрическом поле, в отличие от условий других методов анализа (например, химических), не происходит денатурации белков. [c.215]
Растворы для отмывания электрофореграмм от несвязавшейся с белком краски и закрепления красителя на белке [c.90]
Участки хроматограммы или электрофореграммы, поглощающие в ультрафиолетовой области спектра, вырезают, измельчают и элюируют 0,01 н. раствором НС1 в течение 4 ч. В элюате определяют оптическую плотность при 260 нм. Для учета содержания примесей, имеющих поглощение в той же области спектра, определяют оптическую плотность при 290 нм и по разности (Лги—> 290) рассчитывают содержание адениловых нуклеотидов (с. 499). [c.187]
Электрофореграммы плазмы крови в. норме у всех людей дают почти одну и ту же картину (рнс. 84, а). Для патологии характерна совершенно иная и специфическая для каждого заболевания картина (рис. 84,6). Следовательно, электрофореграммы могут быть успешно использованы как для диагноза, так и для контроля за ходом болезни и нормализацией белкового состава крови. Метод широко используют также для разделения аминокислот, антибиотиков, ферментов, антител и других объектов. [c.215]
Использование сложных оптических схем с разверткой позволяет получить на выходе э л е кт р о ф о р е г р а м м у — кривую с отдельными пиками. Абсцисса каждого пика дает значение характерное для данного компонента и позволяющее провести идентификацию площадь под пиком пропорциональна с,-. Таким образом, методом электрофореграмм можно вести не только качественный, но и количественный анализ в сравнительно мягких условиях, поскольку в слабом электрическом поле, в отличие от условий других методов анализа (например, химических), не происходит денатурации белков. [c.199]
Рис 9 Электрофореграмма сыворотки крови человека (А) и кривая распределения белковых фракций на электрофореграмме (Б) [c.92]
| Рис. ХП.15. Электрофореграмма плазмы крови |
Для приготовления агаровых пластинок используют предметные стекла. Предварительно их обезжиривают, тщательно промывают водой и высушивают. Стекла нумеруют, укладывают на строго горизонтальную поверхность и на каждое осторо