показание к проведению, как делается, что показывает – МЕДСИ
Оглавление
Ультразвуковое исследование (УЗИ) — процедура, безопасная для ребенка любого возраста. Она позволяет провести точную диагностику быстро и безболезненно. При этом не применяется рентгеновское излучение, которое вредно для детского организма. В основе принципа его действия лежит эффект различного отражения звуковых волн высокой частоты от разных типов органов и тканей.
Что из себя представляет вилочковая железа?
Вилочковая железа (тимус) является важной частью организма, отвечающей за выработку Т-лимфоцитов для иммунитета человека. Она размещается в верхней области грудной клетки (в верхнем средостении).
Размеры и масса железы меняются на протяжении всей жизни человека:
- В момент рождения она весит 15 грамм и составляет около 5 см в длину
- К окончанию полового созревания и на протяжении основного периода взрослой жизни ее масса составляет 20–37 грамм, а длина — 7,5–16 см
- К старости (порядка 75-ти лет) ее вес уменьшается до 6 грамм
Вилочковая железа имеет серо-розовый цвет тканей, а в пожилом возрасте — желтоватый.
С какой целью проводят УЗИ тимуса?
Врач назначает УЗИ вилочковой железы для детей в случае, когда имеются жалобы на постоянные болезни ребенка (простуды, ОРЗ и др.) и низкий иммунитет. Это необходимо, чтобы определить причины возникновения регулярных недомоганий.
Ультразвуковое исследование позволяет выявить патологическое увеличение размеров тимуса — тимомегалию. В результате ее появления ослабляется иммунитет, и ребенок начинает регулярно заражаться различными болезнями от других детей и взрослых. В таком случае на фоне обычной простуды может возникнуть аллергия, расстройство ЖКТ, появляется высокая температура.
Показания к проведению
УЗИ тимуса назначается при таких симптомах, как:
- Ребенок регулярно заболевает (до 10-ти раз в год)
- Обычная простуда часто приобретает более тяжелую форму и сопровождается осложнениями (пневмония, бронхит, синусит)
- Температура часто поднимается до 37,5 и держится длительное время
- Обильное срыгивание, слишком частое и тяжелое дыхание
- Появление бронхиальной астмы, аллергических реакций, которые не устраняются даже при более правильной диете
- При общей слабости, хронической утомляемости, болях в груди
- Если сетка сосудов на груди четко отображается
- При нарушении сердечного ритма (аритмия)
- При увеличении лимфоузлов, миндалин или аденоидов
Что может выявить УЗИ?
УЗИ вилочковой железы у детей помогает выявить следующие виды заболеваний и нарушений:
- Тимомегалия
- Патологии развития тимуса
- Аплазия (недоразвитость железы)
- Новообразования (доброкачественные и злокачественные)
- Синдром Бернара-Горнера (аутосомное заболевание)
- Синдром Незелофа (появляется из-за того, что вилочковая железа не справляется со своими функциями)
- Синдром Ди Джорджи (характеризуется низким производством Т-лимфоцитов)
Также ультразвуковое исследование позволит определить такие параметры, как:
- Изменение размера (он должен меняться в пределах возрастных норм)
- Правильность структуры тканей органа
- Контуры (в норме должны быть четкими и однородными)
Как проводится?
Процесс проведения УЗИ вилочковой железы довольно прост:
- Ребенок принимает необходимое для исследования положение тела:
- В возрасте до года он должен находиться на руках у родителей
- От года — он садится или ложится на кушетку
- Если ребенок — подросток, то он должен стоять
- С верхней части тела снимается одежда
- На грудь наносится гель для улучшения проводимости звука
- Врач водит датчиком по верхней части груди
- Изображение отображается на экране, и по нему специалист делает выводы о состоянии органа
Вся процедура занимает порядка 10–15 минут.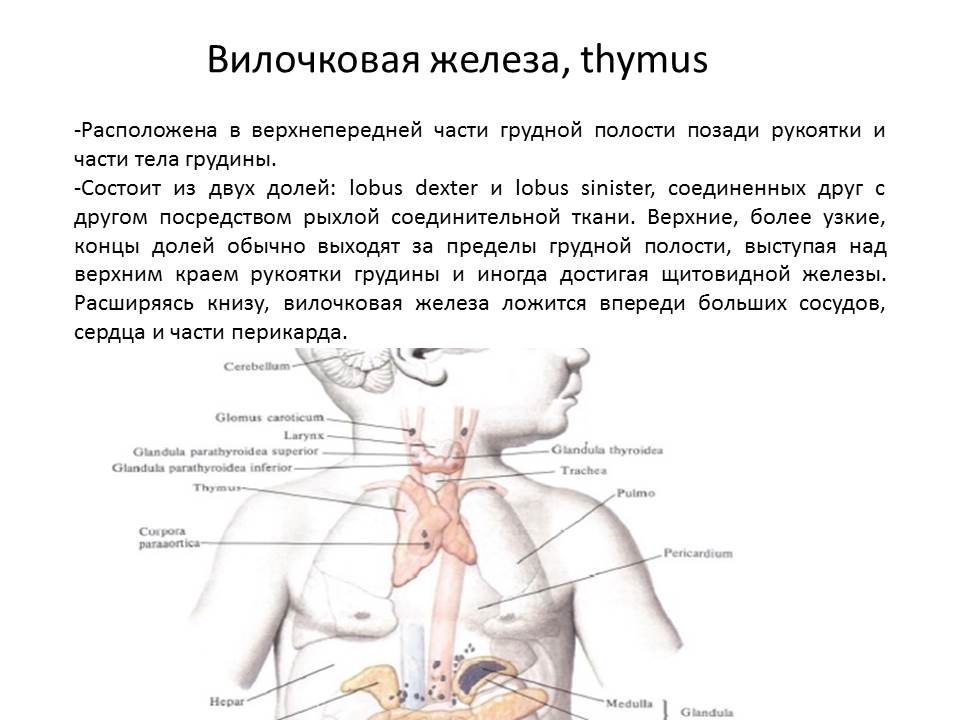
Подготовка
Перед проведением ультразвукового исследования вилочковой железы не требуется сложной подготовки:
- Необходимо предупредить врача, если принимаются различные лекарственные препараты
- Следует узнать точный вес ребенка и сообщить его доктору
- Одежду необходимо подобрать такую, которую будет легко снять перед процедурой
Расшифровка результатов
Для расшифровки результатов врач должен знать точную массу тела ребенка, поскольку от этого значения зависит определение нормального объема и веса вилочковой железы (их соответствия возрастным нормам).
В норме масса железы составляет 0,3 % от общей массы тела. При превышении данного значения ставится диагноз «тимомегалия». Она бывает трех степеней, а ее значение измеряется особым индексом КТТИ:
- I — при значении индекса КТТИ от 0,33 до 0,37 %
- II — при значении КТТИ от 0,37 до 0,42 %
- III — при значении индекса более 0,42 %
Также на сонограмме (результате УЗИ) могут быть обнаружены и такие изменения железы, как: опухоль, чрезмерное разрастание тканей и др.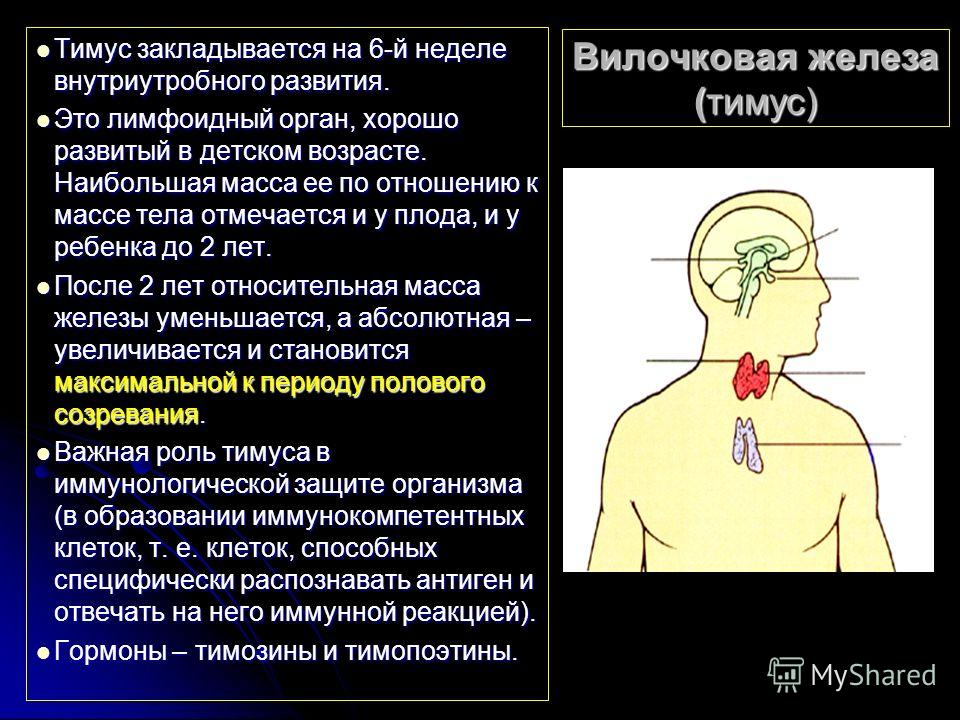
Можно ли исследовать тимус другими способами
УЗИ вилочковой железы как методика используется относительно недавно. Ранее для целей выявления нарушений в работе и строении вилочковой железы использовали рентгенологическое исследование. Но такой анализ нельзя проводить часто, в отличие от УЗИ, поскольку рентген-облучение является вредным для детского организма.Если результаты УЗИ тимуса оказались недостаточно однозначными или контрастными, врач может назначить дополнительные виды обследования:
- Электрокардиограмму (ЭКГ)
- Сканирование сердца
- Анализы крови (общий и биохимический) и мочи
- Сканирование забрюшинного пространства
Преимущества проведения процедуры в МЕДСИ
- В сети клиник МЕДСИ проводится более пятидесяти различных видов ультразвуковых исследований при помощи современных аппаратов экспертного уровня (модели Pro Focus 2202, Philips iU22)
- Расшифровку результатов обследования делают опытные специалисты, имеющие высокие квалификационные категории и регулярно повышающие квалификацию на крупных научных конференциях и семинарах
- Чтобы записаться на консультацию к специалисту, необходимо позвонить по телефону 8 (495) 7-800-500
- В Москве расположено более 20-ти клиник, поэтому подобрать удобное место для обследования легко
- Клиники МЕДСИ располагают комфортными зонами ожидания для детей и родителей
Тимус – что это? Роль тимуса на первому году жизни ребенка
Тимус (вилочковая железа) – важный орган иммунной системы детей.
Он расположен в верхнем отделе грудной клетки и состоит из двух долей, соединяющихся в передней части трахеи. Железа растет до наступления половой зрелости, достигая массы 30–40 грамм, затем постепенно уменьшается (обратное развитие).
Она играет доминирующую роль в иммунной, эндокринной системе. Тимус продуцирует тимозин, тимопоэтин, стимулирующие выработку антител, а также производит Т-лимфоциты – белые клетки крови, уничтожающие аномальные клетки с чужеродными антигенами. Другая функция вилочковой железы – предотвращение патологического роста клеток и предупреждение рака. Следует отметить, что тимус играет ведущую роль в иммунитете ребенка до трех лет.
Роль тимуса в жизни ребёнка
До рождения и в детстве тимус ответственен за производство плюс созревание Т-лимфоцитов, защищающих организм от определенных угроз, включая вирусы, бактерии. Тимус является крупнейшим лимфоидным органом у новорожденных, так как активнее других тканей продуцирует лимфоциты.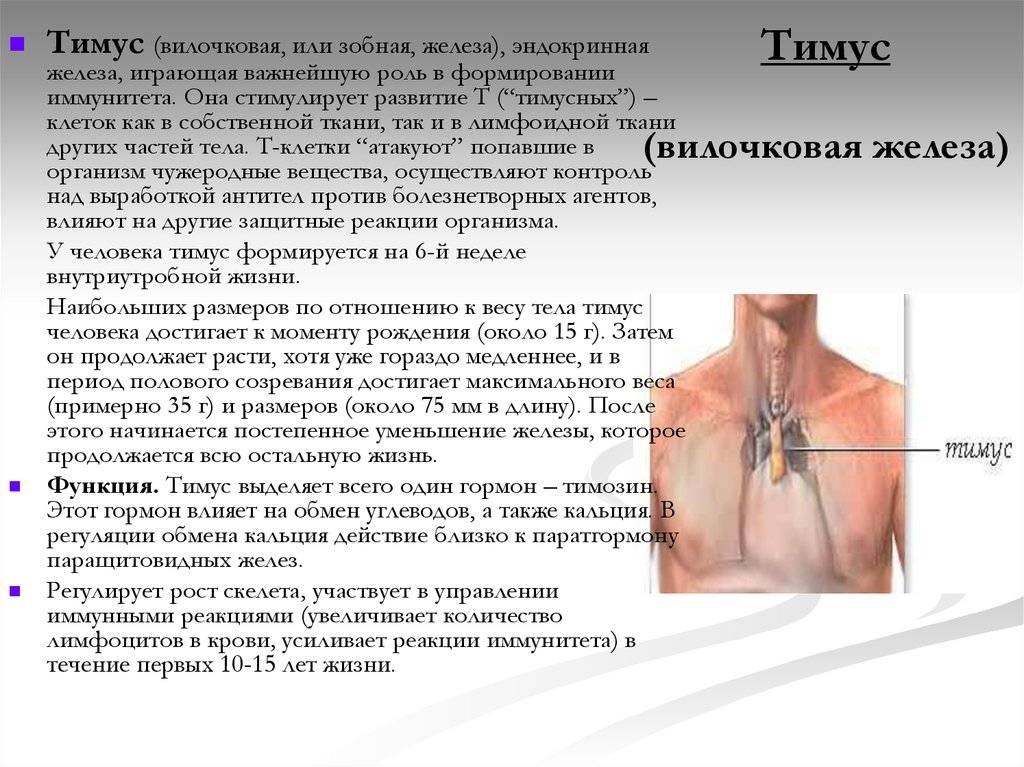 Железа выступает «первой скрипкой» в развитии и улучшении иммунной системы ребенка.
Железа выступает «первой скрипкой» в развитии и улучшении иммунной системы ребенка.
Тимус производит и секретирует тимозин – гормон, необходимый для выработки Т-клеток. После «созревания» в железе они поступают в кровь и мигрируют в лимфоузлы и селезенку, где помогают иммунной системе бороться с болезнью.
В некоторых случаях функции вилочковой железы снижены, что ослабляет иммунную систему, увеличивая склонность к инфекциям и аллергии. Ребенок страдает затяжными ОРВИ, патология легко переходит в хроническую. Недостаток Т-лимфоцитов в организме может привести к иммунодефицитным заболеваниям, характеризующимися сильной потливостью, отечностью и/или болезненностью горла, припухлостью лимфатических узлов, депрессией.
Недоедание и дефицит белка в раннем возрасте обусловливает медленный или ограниченный рост тимуса, «подрывая» тем самым нормальное функционирование лимфоцитов. Вот почему важно сбалансированное питание с достаточным количеством белка.
Доктора данного направления
Патология тимуса
Основные виды патологии тимуса:
- Аплазия – отсутствие или недоразвитие вилочковой железы
- Гипо- и дисплазия – недоразвитие тимуса
- Акцидентальная инволюция – уменьшение вилочковой железы, под влиянием гормонального дисбаланса, стресса, инфекции
- Атрофия – уменьшение, замещение железистой ткани соединительной, прекращение функционирования
- Тимомегалия – увеличение массы и объема паренхимы вилочковой железы выше возрастной нормы при сохранении ее нормального строения
- Гиперплазия – увеличение железистой ткани, с нарушением выработки иммунных клеток и функционирования тимуса.

- Тимома – опухоль вилочковой железы.
- Киста тимуса – жидкостное образование вилочковой железы.
- Патология тимуса (вилочковой железы) может вызывать: развитие ряда иммунодефицитных синдромов, аутоиммунных заболеваний и некоторых эндокринных нарушений.
Увеличение тимуса у детей
Отклонение в размере тимуса в большую сторону и снижение его функции обозначают термином «синдром увеличенной вилочковой железы» (СУВЖ) у детей. Проблему увеличенного тимуса чаще рассматривают в свете дифференциальной диагностики с плевритом, перикардитом, опухолями средостения, другими патологиями.
Ошибочно считают, что увеличенный тимус у детей грудного или раннего возраста является физиологическим состоянием. Особенности протекания инфекционных заболеваний у маленьких пациентов с СУВЖ заставляют классифицировать синдром, как патологию. Дети с СУВЖ имеют большую вероятность развития дисбаланса нейроэндокринной плюс иммунной систем. Поэтому пациенты с выявленным увеличением тимуса требуют полного обследования и диспансерного наблюдения у эндокринолога, иммунолога.
Симптомы заболевания или нарушения развития вилочкой железы
Для того, что бы вовремя выявить патологию тимуса, родителям стоит обратить внимание на отклонения, имеющие различную степень выраженности, которые могут свидетельствовать о заболевании или нарушении развития вилочковой железы:
- Частая заболеваемость ребенка простудными заболеваниями.
- Затяжное течение различных заболеваний, с частыми осложнениями.
- Увеличение лимфоидной ткани – лимфатических узлов, миндалин, аденоидов, ткани на задней поверхности глотки.
- Бледность и/или мраморный рисунок на коже ребёнка.
- Большой вес ребёнка при рождении.
- Ребёнок быстро теряет и быстро набирает вес.
- Кашель вне простудного заболевания, который усиливается в положении ребёнка горизонтально.
- Потливость, субфебрильная температура длительное время вне простудных заболеваний.
- Гипергидроз, холодные конечности.
- Видимая венозная сеточка на груди малыша.

- Цианоз (посинение) носогубного треугольника при нагрузках (плач, бег)
- Частые срыгивания, икоты, отрыжки
- Одышка
- Нарушение сердечного ритма
При возникновении подозрений на патологию тимуса, врач может назначить дополнительные методы обследования:
- УЗИ вилочковой железы,
- КТ,
- МРТ,
- рентген,
- общий анализ крови,
- иммунограмму,
- биохимический анализ крови,
- кровь на гормоны.
Тимическая недостаточность поддается иммунокорекции, которая индивидуально подбирается врачом аллергологом-иммунологом. Стоит обратить внимание, что своевременная диагностика патологии вилочковой железы особенно актуальна на первом году жизни ребенка, когда ребенку начинают проводить вакцинацию.
Для получения подробных консультаций о роли тимуса в жизни ребёнка на первом году жизни обращайтесь к педиатрам медицинских центров «Президент-Мед»
Смотрите так же по теме:Автор: Мамунц Цовинар Алексеевна
Главный врач Президент-Мед г. Видное
Видное
Высшее медицинское, Пермский государственный медицинский институт, лечебный факультет, специальность-лечебное дело
Записаться к врачу
Вопросы педиатру — статьи от специалистов клиники «Мать и дитя»
Дочке 6 месяцев. Пару недель назад ее нижнее веко стало западать вовнутрь. Ресничек у внутреннего угла глаза не видно. Гиперемии, зуда и выделений нет. Похоже на легкий отек, который иногда немного спадает, и реснички становятся видны. Какому врачу следует показать ребенка?
– Скорее всего, у ребенка энтропион – заворот века по направлению к глазному яблоку. Ресницы при этом могут травмировать конъюнктиву глаза, и она из-за этого раздражается. Чаще всего возникает так называемый спастической энтропион нижнего века – он появляется в результате спазма круговой мышцы глаза. Еще энтропион может развиваться в результате рубцовых изменений выстилающей веко мембраны (конъюнктивы). В любом случае надо показать ребенка офтальмологу – врач выявит причину энтропиона и назначит нужное лечение.
Еще энтропион может развиваться в результате рубцовых изменений выстилающей веко мембраны (конъюнктивы). В любом случае надо показать ребенка офтальмологу – врач выявит причину энтропиона и назначит нужное лечение.
Врачи говорят, что у моего ребенка ослаблен иммунитет и увеличена вилочковая железа, поэтому некоторые прививки нам запрещены. Так ли это?
– Тимомегалия – увеличение вилочковой железы – встречается у маленьких детей довольно часто. Точный диагноз можно поставить, сделав рентгенографическое исследование или УЗИ. Если есть тимомегалия I и II степени, то прививки делать можно, главное – на время вакцинации соблюдать гипоаллергенную диету и принимать гипосенсибилизирующие препараты. А вот малышам с тимомегалией III степени вакцинацию не делают, у них есть так называемый медицинский отвод от профилактических прививок (кроме полиомиелита) до 6 месяцев. Все это время их наблюдает педиатр, невролог и иммунолог.
Вчера после купания и кормления сын (ему 2 недели) срыгнул прямо фонтаном, утром после кормления все повторилось. Теперь я боюсь его кормить. Что это было и стоит ли волноваться?
Теперь я боюсь его кормить. Что это было и стоит ли волноваться?
– Срыгивание – совершенно обычное явление у маленьких детей. Дело в том, что желудок у грудного ребенка еще очень мал, он не готов сразу принять и переварить большой объем пищи. Поэтому если ребенок съел больше, чем может поместиться в желудок, – будет срыгивание. Кроме того, почти 70% срыгиваний происходит из-за неверной техники вскармливания: во время кормления грудничок подсасывает воздух, он попадает в желудок, там образуется газовый пузырь, ребенок хочет от него избавиться и вместе с ним срыгивает пищу. Иногда частое срыгивание бывает у сверхвозбудимых детей. Как бы то ни было, в возрасте 1–4 месяца после каждого кормления ребенок может срыгивать до двух столовых ложек молока или однократно срыгивать в день более трех ложек. И это будет нормой. А вот если малыш срыгивает постоянно плюс плохо прибавляет в весе или если каждое срыгивание представляет собой фонтанирующую рвоту, ребенка следует срочно показать врачу.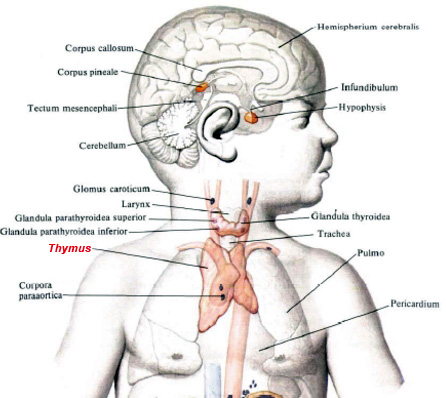
Что дать ребенку в качестве первого прикорма? Педиатр советует начать с овощного пюре, но я не могу понять, с какого овоща начать и как его надо приготовить?
– Действительно, большинство педиатров советуют начинать первый прикорм с овощного пюре: в нем много витаминов и микроэлементов, а главное – в овощном пюре есть растительные волокна и пектины, которые нормализуют микрофлору кишечника. Примерная последовательность введения овощей может быть такой: кабачок, цветная капуста, брокколи, картофель, сладкий картофель, морковь, тыква. Можно начать комбинировать вышеперечисленные овощи, если вы убеждены, что все компоненты хорошо переносятся ребенком. Первый прикорм дают в виде пюре. Чтобы его приготовить, овощи надо отварить, а потом измельчить. Делать это надо правильно. Поэтому, чтобы сохранить в овощах все витамины и микроэлементы, а также их натуральный вкус и цвет, лучше готовить их в специальных пароварках, например Babycook компании Beaba. Они также позволят измельчить пюре, выбрав подходящую для малыша по возрасту консистенцию.
Дочке 3 месяца. С рождения у нее между бровями и на левом веке следы от лопнувших сосудов (маленькие красные полосочки и точки) Все это уже стало бледнее, но не исчезло совсем. Отчего такое бывает? Что посоветуете сделать?
– Иногда на лбу, переносице, веках или затылке ребенка после рождения образуются пятна розовато-красноватого цвета с синюшным оттенком, несколько выпячивающиеся над поверхностью кожи. Некоторые из них бывают очень большого размера, особенно на затылке. Если ребенок кричит или тужится, эти пятнышки проступают ярче, чем пугают мам. Это телеангиэктазия – стойкое расширение поверхностных сосудов кожи и слизистых оболочек. Такое расширение сосудов появляется в результате сдавления, когда ребенок идет по родовым путям. К году эти пятна исчезают бесследно, но вот пятно сзади на границе головы и шеи может остаться надолго. Правда, со временем тоже значительно бледнее, к тому же под волосами его вообще не видно.
Как только мы с ребенком выходим на улицу, он начинает есть песок, землю, а еще все время тянет в рот любой мусор, который лежит под ногами. И оторвать его от этой процедуры очень сложно! Что с этим делать? Вообще, это нормальное поведение?
И оторвать его от этой процедуры очень сложно! Что с этим делать? Вообще, это нормальное поведение?
– Да, это совершенно нормально. То, что делает ваш ребенок, делают многие дети, и дело здесь не в плохих привычках или дурных наклонностях – это один из этапов развития, новая игра, которая дает ребенку новую информацию. Конечно, никто не хочет, чтобы малыш тащил в рот всякую гадость, поэтому его надо отвлекать от такого занятия. На прогулке можно давать ребенку соску (если он ее сосет) или печенье – тогда рот малыша будет занят и в него ничего не попадет. Но лучше выработать у ребенка отрицательную реакцию на слова «мусор», «грязь». То есть, если ребенок берет в руку какую-то гадость, то надо ему сообщить что это «мусор» и попросить его выбросить то, что он поднял. Первое время можно с собой носить специальный пакет и бросать в него поднятые предметы. Одновременно можно рассказывать малышу, что нельзя брать мусор, так как потом нужно мыть руки, а воды на улице нет. Надо постоянно отвлекать ребенка от этой привычки, предлагая ему новые ощущения: дать новую игрушку, пойти на новую площадку с новыми детьми, что-то новое показать.
УЗИ вилочковой железы детям
directions
Вилочковая железа (тимус) — один из важнейших органов иммунной системы, отвечающий за защиту организма от инфекций и вирусов, формирование иммунитета и развитие организма в целом.
Вилочковая железа у детей формируется в утробе матери на шестой неделе беременности и растет вплоть до подросткового возраста. У новорожденных и детей младшего возраста вилочковая железа работает очень активно, вырабатывая Т-лимфоциты, которые, являясь клетками иммунной системы, защищают и оберегают детский организм от заболеваний, бактерий, инфекций. К 12-13 годам функции вилочковой железы у подростков постепенно ослабевают, и организм самостоятельно вырабатывает защиту от болезней.
Врачи-специалисты
Врач ультразвуковой диагностики
В настоящее время на сайте ведутся работы по изменению прайс-листа, актуальную информацию уточняйте по тел: 640-55-25 или оставьте заявку, с Вами свяжется оператор.
Цены на услуги
- Ультразвуковое исследование (УЗИ) вилочковой железы 1100a
Информация и цены, представленные на сайте, являются справочными и не являются публичной офертой.
Наши клиники в Санкт-Петербурге
Медицентр Юго-ЗападПр.Маршала Жукова 28к2
Кировский район
- Автово
- Проспект Ветеранов
- Ленинский проспект
Получить подробную информацию и записаться на прием Вы можете по телефону +7 (812) 640-55-25
При аномалиях развития, увеличении вилочковой железы у детей, организм становится менее защищенным и восприимчивым к заболеваниям различного характера и аллергиям.
Как правило, нарушения в работе вилочковой железы, патологии ее развития можно выявить во время УЗ диагностики.
Если Вы ищете грамотного детского специалиста и хорошего диагноста, можете обратиться в медицинский центр «Медицентр», где ведут прием квалифицированные детские врачи, имеющие многолетний опыт работы с детьми различных возрастов. В «Медицентр» обращаются с детьми с первых дней рождения.
Изменения в работе вилочковой железы могут возникнуть в любом детском возрасте, начиная с грудничкового периода.
Показания к УЗИ вилочковой железы у детей:
- частые простудные заболевания у ребенка;
- увеличение, воспаление аденоидов, миндалин, лимфатических узлов;
- увеличение веса у ребенка, слишком большой вес при рождении;
- затрудненное дыхание;
- повышенное потоотделение;
- частые срыгивания у младенцев;
- почечная недостаточность;
- бледность кожи;
- нарушения ритма сердца;
- усиливающийся при лежании кашель;
- отеки;
- повышенный/пониженный мышечный тонус;
- аллергия неизвестного происхождения;
- перенесенные тяжелые инфекционные заболевания.

Если Вы заметили схожие симптомы у Вашего ребенка, необходимо срочно обратиться к детскому специалисту, который направит на УЗИ вилочковой железы, а после получения результатов назначит лечение.
Увеличение вилочковой железы у детей важно диагностировать на ранних сроках, т.к. ее изменения влияют на самочувствие ребенка в целом. Он больше устает, невнимателен, чаще и тяжелее других детей болеет, неусидчив и с трудом концентрирует внимание. Как правило, в подобных случаях детский врач назначает прием иммунологических препаратов ребенку, чтобы его организм смог справиться с недугом. Также при этом заболевании ребенку необходим здоровый образ жизни в физическом и эмоциональном плане, минимальное пребывание на солнце, длительный сон, прогулки на свежем воздухе, но не в местах большого скопления людей и во время вспышек ОРВИ и гриппа. В особо тяжелых случаях может понадобиться хирургическое вмешательство.
Подготовка к УЗИ вилочковой железы у ребенка
Обследование не требует специальной подготовке, необходимо только знать вес и рост ребенка на момент проведения процедуры.
756,845,941,1318,1262,827
Здравствуйте. Благодарю за слаженную работу персонал Медицентра. Обратилась с признаками ОРЗ. 1. На ресепнш достаточно подробно описали правила прикрепления и уловия приема при остутствии прикрепления по полису ОМС. 2. Прекрасная работа процедурного кабинета, а также м/брата, который осуществляет забор мазков на дому. 3. Мои терапевты: Половодова Е.А. и Артюх Л.Ю.Спасибо за все! 4. Отличная работа сall-центра и личный кабинет просто СУПЕР! Очень хотелось бы, чтобы отзыв нашел всех, кто упомянут. Спасибо!
Ефремова Елена 07.11.2020 17:21medi-center.ru
Сердечно благодарим доктора Попову К.Е. за высокий профессионализм, внимательность и отзывчивость при домашнем визите и рекомендациях по лечению. Спасибо Вам большое!
Спасибо Вам большое!
medi-center.ru
Выражаю огромную благодарность травматологу Джораеву Агамурату Оразмамедовичу, вправившему мне плечо, несмотря на то, что вывих не был виден на рентгене! Профи! Спасибо!
добрый день! хочу сердечно поблагодарить гастроэнтеролога Банникову Татьяну Петровну за профессиональный прием. Я обратилась с болью, думая, что у меня проблемы с желчным пузырем, даже принимала соотвествующие лекарства, но после опроса симптоматики и осмотра мне был поставлен другой диагноз и назначено соотвествующее лечение. Очень чуткий и внимательный доктор! Спасибо!
Ваше имя: Валентина.
Дата события: 25 апреля
Специализация врача: Гастроэнтеролог Банникова Т. П.
Обследование: первичный прием с жалобами на боль в боку.
П.
Обследование: первичный прием с жалобами на боль в боку.
Я лечусь в клинике на Охтинской аллее . Очень приятный , вежливый персонал , все чисто , аккуратно … врач у которого я лечусь , очень внимательный , «не разводит». Могу смело советовать эту клинику!!!
Выражаю благодарность Сидоркину Владимиру Александровичу (ЛОР). Благодаря профессионализму и опыту, врач смог диагностировать воспаление тройничного нерва, хотя изначально предполагал фарингит, т.к. боль была в районе лобных пазух. Верный диагноз доктор поставил после просмотра диска с рентгеновским снимком. Невролог подтвердил диагноз. Убедительная просьба, обеспечить ЛОР-врача возможностью просматривать рентгеновские снимки на цифровых носителях (диски), чтобы врач не бегал по клинике в поисках ПК с дисководом.
Тимомегалия– увеличение вилочковой железы — Новости Сургутского района
Тимомегалия (лат. thymus — тимус; megalia — увеличение) — это состояние, при котором отмечается значительное увеличение размеров центрального органа иммунной системы — вилочковой железы, часто встречающееся у детей раннего возраста.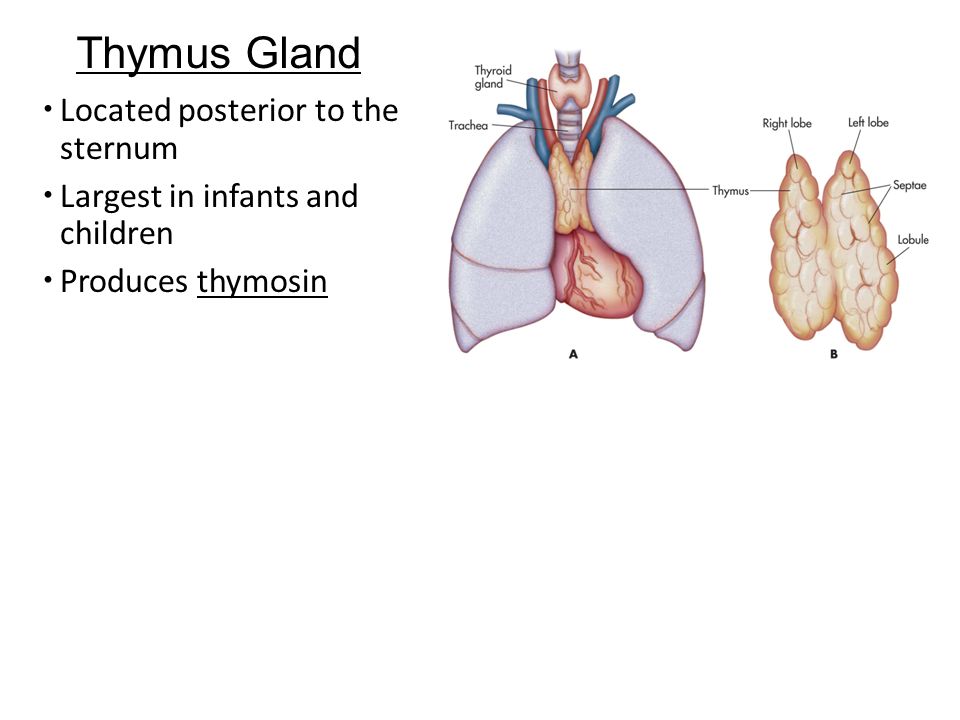
К формированию данного состояния могут приводить как внешние, так и внутренние факторы или их сочетание. Доказана и важная роль неблагоприятных факторов в дородовом периоде (гестозы I и II половины беременности, нефропатии, инфекционные заболевания у матери, воздействие неблагоприятных факторов внешней среды, поздняя беременность).
Проявления тимомегалии. Проявления синдрома увеличения тимуса бывают только при его выраженном и резком увеличении — незначительные стадии увеличения никаких симптомов не дают и могут быть обнаружены только при рентгенологическом или ультразвуковом обследовании. Если же он увеличен сильно, то у каждого ребёнка набор симптомов будет своеобразным, но всё же можно выделить четыре основных формы клинических проявлений этого нарушения: синдром сдавления жизненно важных органов; синдром нарушения иммунитета; лимфопролиферативный и синдром эндокринно-обменных нарушений.
ДАВАЙТЕ РАЗБЕРЁМ ИХ КАЖДЫЙ В ПОДРОБНОСТЯХ.
Итак, при сдавлении тимусом жизненно важных органов могут затрагиваться трахея, блуждающий нерв, верхняя полая вена, сосудистый пучок и вследствие этого будут возникать различного рода проявления.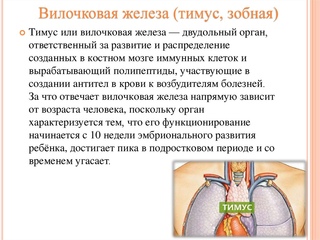 Если сдавилась трахея, могут возникать следующие признаки: одышка, шум при дыхании, особенно в возбуждённом состоянии, храпение, коклюшеподобный кашель, приступы тимусовой астмы, асфиксии или спадение участков лёгких. При сдавливании сосудистого пучка появляются расширенные вены на передней поверхности груди, набухают шейные вены, а шея выглядит отёчной, появляется шум в сосудах шеи.
Если сдавилась трахея, могут возникать следующие признаки: одышка, шум при дыхании, особенно в возбуждённом состоянии, храпение, коклюшеподобный кашель, приступы тимусовой астмы, асфиксии или спадение участков лёгких. При сдавливании сосудистого пучка появляются расширенные вены на передней поверхности груди, набухают шейные вены, а шея выглядит отёчной, появляется шум в сосудах шеи.
При раздражении блуждающего нерва и сопутствующей этому недостаточности надпочечников появляется замедление ритма сердца, осиплость голоса, могут быть падения давления (коллапсы), «петушиный» крик, срыгивания или рвота, расстройства стула. У ребёнка возникают также защитные симптомы -сон на животе и резкое запрокидывание головы назад.
Синдром лимфопролиферации -это сопутствующие увеличению тимуса увеличенные лимфоузлы, разрастание фолликулов у корня языка, увеличение миндалин, селезёнки, а в крови — увеличение числа лимфоцитов. Это происходит из-за избытка гормонов, которые влияют ни тимус и надпочечник.
Нарушения в эндокринной системе и обмене веществ проявляются обычно в ожирении, нарушении аппетита, увеличенной печени, потемнении от пигмента пальцев на ногах и руках (как загорелые), снижении давления, проявлении признаков, похожих на рахит; страдает сердце. При этом при исследовании выявляется дисбаланс в гормонах надпочечника, нарушения в щитовидной железе и гипофизе. Все эти проявления должны выявляться как минимум 4 месяца подряд и более, они же должны сочетаться с рентгенологическими признаками увеличения тимуса, тогда устанавливается диагноз тимомегалии с расстройством функции.
Особенности течения болезни у таких детей. Дети с увеличением тимуса болеют по-особенному, у них отличается течение многих часто встречающихся заболеваний. Например, всем известные ОРЗ и ОРВИ у таких детей протекают в первые два-три дня с нормальной температурой или незначительным её повышением. Но затем она резко повышается до высоких цифр, проявления становятся сильными и выраженными, особенно сильно поражаются верхние дыхательные пути и бронхи с лёгкими, что может приводить к затяжному характеру болезни. При тимомегалии симптомы простуды проявляются сильнее обычного — если это кашель, он становится коклюшеобразным, с приступами, сухим и навязчивым, часто возникают признаки обструкции бронхов, ложный круп с отёком гортани. Улучшение идёт медленно, кашель зачастую остаётся надолго, на месяц и более. У части детей заболевание осложняется отитами, у половины при простудах наблюдается жидкий стул и боли в животе. Имеют отличительные особенности и пневмонии, они обычно возникают постепенно, не проявляются остро, температура при них редко бывает высокой, поэтому диагноз ставят поздно и с трудом.
При тимомегалии симптомы простуды проявляются сильнее обычного — если это кашель, он становится коклюшеобразным, с приступами, сухим и навязчивым, часто возникают признаки обструкции бронхов, ложный круп с отёком гортани. Улучшение идёт медленно, кашель зачастую остаётся надолго, на месяц и более. У части детей заболевание осложняется отитами, у половины при простудах наблюдается жидкий стул и боли в животе. Имеют отличительные особенности и пневмонии, они обычно возникают постепенно, не проявляются остро, температура при них редко бывает высокой, поэтому диагноз ставят поздно и с трудом.
Как ставят диагноз тимомегалия?
Самым основным диагностическим способом увидеть увеличенный тимус всё ещё остаётся рентген. На нём можно увидеть признаки увеличения тимуса от первой до третьей степени. Однако не всегда увеличение бывает типичным, и требуются дополнительные снимки, кроме обзорного рентгена грудной клетки.
Как это лечат?
В первую очередь немедикаментозными средствами — это, прежде всего, строгие режимные мероприятия, диета, а уж потом, на крайний случай, медикаментозная терапия. Режим у ребёнка должен быть обычный, как у всех детей, но с некоторыми оговорками -оградите такого малыша от сильных стрессовых раздражителей: переездов, ремонтов, разводов, истерик. В основе диеты — ограничение лёгких углеводов и животных жиров, а для детей на первом году жизни самым лучшим питанием и профилактикой инфекций и разрастания тимуса является кормление грудью. Если же этой возможности нет, надо выбирать для кормления детей высоко адаптированные, гипоаллергенные и кисломолочные смеси. До трёх лет не стоит давать детям яйца, шоколад, какао или мёд, а питание необходимо дополнительно обогащать витаминами. Если у ребёнка возникают эпизоды диареи, необходимо вообще резко снизить потребление жиров. Медикаментозную терапию назначают детям с сильно выраженными признаками болезни, курсами два или три раза в год, чаще всего это делают осенью и весной либо ещё зимой. Объём терапии определяет врач.
Режим у ребёнка должен быть обычный, как у всех детей, но с некоторыми оговорками -оградите такого малыша от сильных стрессовых раздражителей: переездов, ремонтов, разводов, истерик. В основе диеты — ограничение лёгких углеводов и животных жиров, а для детей на первом году жизни самым лучшим питанием и профилактикой инфекций и разрастания тимуса является кормление грудью. Если же этой возможности нет, надо выбирать для кормления детей высоко адаптированные, гипоаллергенные и кисломолочные смеси. До трёх лет не стоит давать детям яйца, шоколад, какао или мёд, а питание необходимо дополнительно обогащать витаминами. Если у ребёнка возникают эпизоды диареи, необходимо вообще резко снизить потребление жиров. Медикаментозную терапию назначают детям с сильно выраженными признаками болезни, курсами два или три раза в год, чаще всего это делают осенью и весной либо ещё зимой. Объём терапии определяет врач.
Вакцинация: тимомегалия 1 и 2 степени не является противопоказанием к вакцинации при условии клинического здоровья.
Наблюдение детей с синдромом увеличения вилочковой железы. Диспансерное наблюдение детей с тимомегалией проводится участковым врачом, который при необходимости назначит консультации специалистов. Требуются охранительные мероприятия, правильное питание, соответствующее возрасту.
К.В. ГЕРБСТ, врач аллерголог-иммунолог отделения клинической иммунологии и аллергологии Окружного кардиологического диспансера «Центр диагностики и сердечно-сосудистой хирургии» г. Сургута.
К вопросу о тимомегалии у детей раннего возраста
Тимус (вилочковая железа) относится к центральным органам иммунной системы. Физиологическая роль тимуса заключается в дифференцировке и клональной селекции Т-лимфоцитов. В результате длительного (3-4 недели) поэтапного процесса «обучения» в тиму- се созревают аутотолерантные Т-лимфоциты (менее 10%) способные к взаимодействию с клетками иммунной системы, которые, попадая в общий кровоток, заселяют периферические органы иммунной системы (т. н.положительная селекция).
н.положительная селекция).
Остальные лимфоциты, не распознающие собственные ГКГС-белки и аутореактивные, подвергаются апоптозу и уничтожаются собственными макрофагами (отрицательная селекция).
Исследованиями последних лет выделено и охарактеризовано более 40 биорегуляторов пептидной, гликопротеидной и стероидной природы, вырабатываемых клетками тимуса. Большинство из них являются цитокинами паракринного действия. Однако, 8 субстанций действуют системно и могут считаться специфическими тимическими гормонами.Системное влияние тимических гормонов на нейроэндокринную систему проявляется через регуляцию адренокортикарных функций. Особенно важно, что указанное воздействие проявляется еще в преиммунном ответе. В свою очередь, активация тимуса осуществляется по цепочке гипоталямус- гипофиз –соматотропин, а также, тиреоидными гормонами.
Таким образом, тимус является важнейшим связующим звеном и как бы коммутатором взаимоотношений нейроэндокринной и иммунной систем организма. Все это свидетельствует о многогранных функциях тимуса как эндокриннолимфоидного органа и широте его воздействия на различные обменные процессы в физиологических и патологических условиях.
Формирование иммунного ответа начинается во 2-й половине внутриутробного развития. Эмбриональные лимфоциты вследствие воздействия плацентарных цитокинов и гормонов, а возможно и аллергенов смещаются в сторону Тh3 профиля ответа. Такой сдвиг в сторону Тh3 системы «мать-плод» во время беременности обеспечивает благоприятное течение внутриутробного периода.
В постнатальный период, вследствие стимуляции иммунной системы компонентами инфекционных агентов, у большинства детей происходит переключение с Тh3 типа на Тh2 тип. Програмирование двух противоположных типов аллерген-специфических клеток, продуцирующих цитокины Тh2 и Тh3, начинается в раннем детском возрасте в незрелой иммунной системе. К 2-летнему возрасту формируются основные механизмы определяющие характер, интенсивность и эффективность Т-клеточной реакции на аллергены, в пер-вую очередь, окружающей среды. Окончательное формирование фенотипа происходит к 5-6 годам.
На процесс формирования фенотипа Т-клеточной реакции влияют многочисленные факторы, причем генетические факторы имеют важное, но не решающее значение. Немаловажную роль в этом процессе играет морфо-функциональное состояние тимуса.
Немаловажную роль в этом процессе играет морфо-функциональное состояние тимуса.
При рождении тимус весит 15 г, к пубертату достигает максимальной массы в 50 г. Однако,если измерять массу паренхимы тимуса без учета жировой ткани, то максимум в 38 г. достигается уже в возрасте 2-5 лет, далее идет прогрессивное ее уменьшение.Очевидно, что максимальной функциональной массы тимус достигает в период оформившегося Т-лимфоцитарного иммунного ответа. Одновременно с прибавкой массы паренхимы происходит дальнейшая дифференцировка и усовершенствование собственно функциональных регуляторных механизмов тимуса.
Патология тимуса формируется в виде гипопластических, гиперпластических или диспластических процессов. В детском возрасте наиболее часто встречаются гиперпластические процессы приводящие к увеличению массы органа-тимомегалии.
Актуальность проблемы обусловлена высокой распространенностью тимомегалии у детей с постоянным ростом ее частоты, большей подверженностью этих детей инфекционным и аллергическим заболеваниям, особенно в раннем возрасте, осложненным их течением, заканчивающихся иногда неожиданным летальным исходом.
Раскрытие патогенеза тимомегалии имеет большое теоретическое значение как для понимания механизмов развития иммунной и нейроэндокринной систем и, соответственно, различных обменных процессов в раннем детском возрасте, так и механизмов их возможных отклонений. Оно важно и в клиническом аспекте в каждом конкретном случае, так как увеличение тимуса является неблагоприятным фактором преморбитного состояния, с возможными ближайшими и отдаленными последствиями.
Регуляция функциональной активности тимуса, в первую очередь, осуществляется непосредственно антигенами и различными цитокинами. Способность реагировать на антигенную стимуляцию тимус приобретает примерно с 20 нед. внутриутробного периода. Поэтому, при отягощеной беременности различной этиологии, при внутриутробных инфекциях,в условиях нарушения плацентарной проницаемости, особенно в сочетании с хронической гипоксией, в большинстве случаев развивается внутриутробная тимомегалия.
В постнатальном периоде антигенная нагрузка тимуса резко возрастает. Антигены поступают во внутреннюю среду через кожу и слизистые, из коих важнейшей является слизистая ЖКТ.
Антигены поступают во внутреннюю среду через кожу и слизистые, из коих важнейшей является слизистая ЖКТ.
Поток антигенов и токсинов из ЖКТ зависит от факторов питания, микробиоциноза кишечника и морфофункционального состояния слизистой. Заселение кишечника микрофлорой начинается автоматически с момента прохождении через родовые пути матери. Принципиально важно какие микробы первыми попадают и размножаются в тракте. Колонизация бифидо и лактобактериями является физиологической и способствует становлению процессов нормального пищеварения и интенсивного морфофункционого развития слизистой кишечника уже в периоде адаптации организма новорожденного. При первоначальном росте условно и патогенной микрофлоры указанные процессы, особенно развитие и целостность слизистой, нарушаются.
Поэтому, первоначальная колонизация кишечника является для иммунной системы и организма в целом событием, которое нужно расценивать как одно из ключевых событий за всю жизнь.
И не случайно природа предопределила питание в первые дни жизни такой универсальной пищей, каковой является молозиво. Оно содержит все необходимые пищевые ингридиенты в таком химическом виде, что большинство из них почти без расщепления попадают во внутреннюю среду организма ребенка. Кроме того, оно содержит многочисленные факторы играющие важную роль в защите ЖКТ, активизации местного и общего иммунитета, стимуляции роста бифидо и лактобактерий. Поэтому, принципиально важно раннее прикладывание новорожденного к груди, состояние матери и ребенка, совместное их пребывание.
Оно содержит все необходимые пищевые ингридиенты в таком химическом виде, что большинство из них почти без расщепления попадают во внутреннюю среду организма ребенка. Кроме того, оно содержит многочисленные факторы играющие важную роль в защите ЖКТ, активизации местного и общего иммунитета, стимуляции роста бифидо и лактобактерий. Поэтому, принципиально важно раннее прикладывание новорожденного к груди, состояние матери и ребенка, совместное их пребывание.
В наши дни в связи с урбанизацией увеличивается число новорожденных с нарушением
процесса первичной колонизации слизистой кишечника за счет снижения количества бифидо и лактобактерий и нарушения взаимообмена микробами между матерью и ребенком. Неблагоприятным фактором для процесса первичной колонизации является широкое, зачастую необоснованное применение антибиотиков у новорожденных. Отрицательно сказывается на этом процессе и кесарево сечение у большинства таких детей развиваются стойкие дисбиотические изменения флоры кишечника.
Другим важным фактором влияющим на состояние тимуса являются роды.Тяжелая гипоксия головного мозга ребенка, особенно гипоталямической области, в родах и в послеродовый период зачастую приводят или усиливают развитие тимомегалии.
Впоследствии увеличение тимуса развивается и прогрессирует вследствии постоянного повышенного его раздражения антигенами и цитокинами поступающими, в основном, из ЖКТ. Ответная реакция тимуса и всей иммунной системы зависят как от дозы и типа антигенов и цитокинов, времени их экспозиции, так и от генетических вариаций индивидуальной способности к ответу. Не случайно, наиболее часто тимомегалия встречается у детей с экссудативно-катаральным и, особенно, лимфогипопластическим диатезами.
Этот факт обьясняет и генетическую предрасположенность к тимомегалии, особенно II и III степени. Принципиально важно, что все эти процессы происходят в период становления и дифференцировки функций незрелой иммунной системы с окончательным развитием фенотипа.
Таким образом, увеличение тимуса – тимомегалию у детей раннего возраста следует рассматривать как результат длительного, с периодами обострения, антигенного и токсического стресса в период становления и интенсивного развития незрелой иммунной системы в частности и организма в целом. Независимо от причин, тимомегалия — тревожный сигнал об иммунологических, эндокринных и обменных нарушениях и напряжении защитно-адаптационных механизмов.
Независимо от причин, тимомегалия — тревожный сигнал об иммунологических, эндокринных и обменных нарушениях и напряжении защитно-адаптационных механизмов.
Увеличение тимуса наиболее достоверно определяется при рентгенологическом и ультразвуковом обследовании грудной клетки с помощью тимико-торакального индекса (ТТИ). В норме ТТИ у детей до года равен 0.260, от 1 до3 лет -0,231, от 3 до 6 лет -0,220.
У детей до года c 10 увеличения тимуса ТТИ равен 0,367, II0 – 0,445, III0– 0,572, у детей 2-3 лет, соответственно, – 0,331, 0,440 и 0,560, детей 3-6 лет I0– 0,308 , II0 – 0,430.
Размеры тимуса в определенной степени обьективно согласуются с его функциональным состоянием. Так, с большой вероятностью можно предположить, что при 10 тимомегалии функции тимуса компенсированы, при II0 – уже развивается стадия суб, а при III0 – стадия декомпенсации. Поэтому, видимо следует согласиться с П.Д.Вагановым, который классифицировал 10 тимомегалии как синдром увеличенной вилочковой железы, а II и III0 – как собственно тимомегалию.
Морфологические изменения тимуса разнообраны и, в какой то мере, соответствуют степени увеличения органа. В начальной стадии отмечается увеличение количества и активности тимоцитов, кровенаполнения, в первую очередь артериального, что следует расценивать как физиологическую реакцию на повышенную антигенную нагрузку организма. Дальнейшее течение процесса характеризуется уменьшением числа тимоцитов, тимические тельца немногочисленны, мелкие, в корковой зоне определяется пролиферация макрофагов и лимфоцитов. Скопления лимфоцитов, отсутствующие в норме, могут развиваться в виде фолликул. Увеличивается доля жировой ткани и соединительнотканных элементов.
Соответствующие изменения развиваются в железах эндокринной системы и периферических лимфатических образованиях. Особенно значимы с патогенетической и клинической точек зрения морфофункциональные изменения надпочечников, проявляющихся в виде гипокортицизма, гипоадренализма. Нарушены, также, функции щитовидной железы.
Изменения происходят и в иммунном ответе как в Т- зависимом, так , и в Т- независимом форматах. На характер нарушений Т-зависимого иммунного ответа, в первую очередь, влияет формируемый баланс Тh2 /Тh3 типов ответа. При нормальном соотношении или преобладании Тh2 типа отмечаются нарушения преимущественно клеточного и, наоборот при преобладании Тh3 типа – гуморального иммунитета. Развиваются нарушения и в Т-независимом формате иммунных механизмов. Они проявляются уже в преиммунном ответе. Снижается активность факторов неспецифической защиты, в частности сывороточного лизоцима и комплемента. Нарушается фагоцитарная активность: показатель фагоцитоза (количество нейтрофилов участвующих в фагоцитозе), индекс фагоцитоза (поглотительная функция нейтрофилов) и показатель завершенности фагоцитоза.
На характер нарушений Т-зависимого иммунного ответа, в первую очередь, влияет формируемый баланс Тh2 /Тh3 типов ответа. При нормальном соотношении или преобладании Тh2 типа отмечаются нарушения преимущественно клеточного и, наоборот при преобладании Тh3 типа – гуморального иммунитета. Развиваются нарушения и в Т-независимом формате иммунных механизмов. Они проявляются уже в преиммунном ответе. Снижается активность факторов неспецифической защиты, в частности сывороточного лизоцима и комплемента. Нарушается фагоцитарная активность: показатель фагоцитоза (количество нейтрофилов участвующих в фагоцитозе), индекс фагоцитоза (поглотительная функция нейтрофилов) и показатель завершенности фагоцитоза.
Указанные изменения в системе неспецифической защиты и фагоцитоза усугубляют дисбаланс в иммунной системе. Дети с увеличенной массой тимуса подвержены частым инфекционно-воспалительным заболеваниям со склонностью к затяжному течению. У части из них достоверно выше склонность к различным аллергическим реакциям .
Таким образом, у детей с тимомегалией в периоде становления и интенсивного развития незрелой иммунной системы, в условиях генетически детерменированных и индивидуальных особенностей формирующегося фенотипа, возможны вариации как иммунного отве –та в частности, так и организма в целом на различные антигены.В одном случае, на фоне плохо отрегулированного и усиленного иммунного ответа, происходит усиленный (гипер-ергический) и плохо отрегулированный процесс воспаления с выраженным аллергическим компонентом. И, наоборот, на фоне плохо отрегулированного и слабого ответа развивается слабый и плохо регулируемый процесс воспаления со склонностью к затяжному течению.
Степень увеличения тимуса, полиморфизм и степень клинических проявлений в каждом конкретном случае зависят от совокупности действия и времени многих факторов, в первую очередь, антигенной нагрузки.
По нашим наблюдениям и по литературным данным наиболее часто (до 85-90% случаев) увеличение тимуса наблюдается у детей раннего возраста, причем около половины из них оно отмечается у детей до 1 года. I0 увеличения тимуса выявляется чаще (до 80%), II0 от15 до 20%, а Ш 0 — в 1-3% случаев. С возрастом степень увеличения тимуса уменьшается. Так, у детей старше 1 года преобладает 10, а Ш0 степень не встречается уже с 2-3 летнего возраста.
I0 увеличения тимуса выявляется чаще (до 80%), II0 от15 до 20%, а Ш 0 — в 1-3% случаев. С возрастом степень увеличения тимуса уменьшается. Так, у детей старше 1 года преобладает 10, а Ш0 степень не встречается уже с 2-3 летнего возраста.
У большинства новорожденных детей поступивших в стационар с различной патологией выявлено увеличение тимуса в основном 10 . Анамнестические данные выявили у них в 70% случаев различные патологии течения беременности и родов.
Фактором риска увеличения тимуса у детей до 6 мес. является раннее искусственное вскармливание. Увеличение тимуса обнаружено и у впервые заболевших детей находившихся на грудном вскармливании. У 70% их матерей были выявлеы симптомы нерезко выраженного нарушения пищеварения (метеоризм, неустойчивый стул, чаще в виде запоров, дискомфорт и боли в животе), анемия, признаки полигиповитаминоза.
Дети с увеличением тимуса уже на первом году жизни чаще болеют ОРВИ, острыми и хроническими нарушениями пищеварения и питания, рахитом, анемией, у них чаще развиваются аллергические проявления. В возрасте до 3 лет более половины детей с увеличенным тимусом относятся к группе часто болеющих детей, с более тяжелым и длительным течением ОРИ (обструктивный бронхит, пневмонии, отиты, фебрильные судороги, кишечный синдром). Эта группа детей отличается и высокой частотой развития ЛОР патологии: аденоидные вегетации и гиперплазия небных миндалин с последующим развитием хронического тонзиллита. Эти дети отличаются лабильностью и возбудимостью ЦНС, у них чаще отмечаются стоматиты, признаки полигиповитаминоза, особенно гиповитаминоза А, сидеропенический синдром.
В возрасте до 3 лет более половины детей с увеличенным тимусом относятся к группе часто болеющих детей, с более тяжелым и длительным течением ОРИ (обструктивный бронхит, пневмонии, отиты, фебрильные судороги, кишечный синдром). Эта группа детей отличается и высокой частотой развития ЛОР патологии: аденоидные вегетации и гиперплазия небных миндалин с последующим развитием хронического тонзиллита. Эти дети отличаются лабильностью и возбудимостью ЦНС, у них чаще отмечаются стоматиты, признаки полигиповитаминоза, особенно гиповитаминоза А, сидеропенический синдром.
Полиморфизм клинико — лабораторных проявлений при отсутствии специфических симптомов, особенно у часто болеющих детей раннего возраста, являются причиной того, что в 85-90% случаев увеличение тимуса обнаруживается при рентгенографии по поводу различных заболеваний детей.
По мнению проф. П.Д. Ваганова раннему выявлению синдрома увеличения вилочковой железы подлежат дети:
1. имеющие в анамнезе отягощенные антенатальные факторы и перинатальное поражение ЦНС,
2. рожденные от матерей, у которых в детстве было выявлено увеличение тимуса,
рожденные от матерей, у которых в детстве было выявлено увеличение тимуса,
3. имеющие затрудненное дыхание при отсутствии катаральных явлений,
4.с высоким инфекционным индексом.
Этим детям рекомендуется провести УЗИ тимуса с определением ее массы в граммах.
При выявлении увеличения тимуса необходимо провести тщательный сбор анамнеза и обследование ребенка с целью выявления причин длительной антигенной и токсической нагрузки организма больного ребенка.
Лечебные мероприятия включают в себя коррекцию питания, обменных и гормональных нарушений, иммунологического статуса, лечения сопутствующих заболеваний.
Коррекция питания является принципиально важной задачей лечения. У детей находящихся на грудном вскармливании зачастую необходимо провести коррекцию питания матери. Диета матери должна быть сбалансированной, содержать достаточное количество белка, овощей и фруктов, богатой витаминами и микроэлементами. При выявлении заболеваний у матери следует провести их лечение. Детям на искусственном вскармливании и старше 6 мес. следует назначить питание не столько по возрасту, сколько исходя из функционального состояния ЖКТ. Питание этих детей должно быть как полноценным, так и наиболее легкоперевариваемым и способствующим перистальтике кишечника, назначается дробно, относительно малыми порциями, чаще. При необходимости следует назначить эти пробиотики, ферментативные препараты.
Детям на искусственном вскармливании и старше 6 мес. следует назначить питание не столько по возрасту, сколько исходя из функционального состояния ЖКТ. Питание этих детей должно быть как полноценным, так и наиболее легкоперевариваемым и способствующим перистальтике кишечника, назначается дробно, относительно малыми порциями, чаще. При необходимости следует назначить эти пробиотики, ферментативные препараты.
С целью улучшения обменных процессов назначается комплекс витаминов:
А, Е, Д, В-комплекс, препараты кальция. При сидеропенических проявлениях после определения ферритина крови препараты железа. Витаминотерапия проводится не менее 1 мес., препараты железа и кальция – 1,5-2 мес. и более. При необходимости назначаюся гепатопротекторы коротким курсом.
При 10 увеличения тимуса лечение лечение ограничиваеся коррекцией питания, назначением эубиотиков, реже – короткого курса витаминотерапии. При увеличении тимуса II-Ш0, помимо вышеуказанных задач возникает необходимость иммуннокорегирующей терапии ( тактивин, реже элеутерококк ). Тактивин назначается в дозе 2 мкг/кг, подкожно, курс 5-7 иньекций.
Тактивин назначается в дозе 2 мкг/кг, подкожно, курс 5-7 иньекций.
Особую актуальность в практике педиатра приобретает проведение профпрививок детям с увеличенным тимусом. При проведении прививок этим детям следует учитывать степень увеличения тимуса, анамнез, характер питания и индивидуальные особенности организма ребенка.
Дети с увеличенным тимусом 10 чаще переносят прививки бессимптомно и без особых отклонений от инструкций по проведению прививок здоровым детям (по частоте местных и общих реакций). Детям с увеличением тимуса II0 рекомендуется проводить вакцинацию на фоне гипоаллергенной диеты, курса витаминотерапии,. приема эубиотиков. Назначение гипосенсибилизирующей терапии решается индивидуально с учетом аллергического фона организма ребенка. Практически все дети с увеличением 10 и большая часть II0 имеют теже показания и противопоказания профпрививок что здоровые дети при условии клинического здоровья.
При тимомегалии Ш0 рекомендуется отложить проведение прививок до 6 мес. при условии назначения коррегирующего лечения.
при условии назначения коррегирующего лечения.
Нарушения гормонального статуса у детей с тимомегалией II и, особенно, Ш0 зачастую сопровождаюся осложненным, тяжелым течением острых заболеваний, что диктует необходимость назначения глюкокортикоидов (дексаметазон, преднизолон) в течении всего периода тяжелого состояния ребенка – обычно не более 3-5 дней.
Таким образом, дети с увеличением тимуса, особенно II и Ш0 .отличающиеся определенными изменениями и нарушениями иммунной и нейроэндокринной систем, относятся к детям группы риска. Этим и определяется необходимость проведения дифференцированного подхода к проведению лечебно-оздоровительных и профилактических мероприятий в каждом конкретном случае.
З. Б. Мелконян
кафедра педиатрии ЕрГМУ
Ультразвуковое исследование (УЗИ) вилочковой железы у детей.
30/09/17
Несмотря на маленький размер вилочковая железа (еще ее называют тимусом) играет огромную роль в здоровье ребенка.
Если ребенок болеет часто и долго, то рекомендуется проводить исследование вилочковой железы.
Основными показаниями к исследованию вилочковой железы:
1. Частые простудные заболевания.
2. Перенесенные более серьёзные заболевания такие как: синуситы, воспаления легких — пневмонии, бронхиты.
3. Если ребенок склонен к аллергическим проявлениям таким как: диатез, крапивница, поллиноз, бронхиальная астма и т.д.
4. При увеличении лимфатических узлов, особенно длительно существующих и слабо поддающиеся лечению.
5. Если у ребенка длительное время держится температура 37,5 С.
Подготовка к УЗИ исследованию: специальная подготовка не требуется. На исследовании необходимо знать вес ребенка.
В раннем возрасте при возникновении необходимости исследования вилочковой железы у ребенка необходимо проведение именно УЗИ, а не рентгенографии:
1. УЗИ не «вредный» метод исследования,т.е. не несёт никакой лучевой нагрузки, в отличии от рентгенографии.
2. Только с помощью УЗИ возможно определение структуры паренхимы вилочковой железы (определения различных образований в ткани тимуса), что невозможно определить на рентгенографии.
3. С помощью УЗИ исследования можно рассчитать объем вилочковой железы по отношению к массе тела ребенка ( у каждого ребенка он различен), что более качественно отображает размер органа.
УЗИ вилочковой железы возможно провести только пока не произошло окостенения грудины, поэтому , чем младше ребенок, тем лучше мы может оценить орган.
Вилочковая железа в большинстве своем имеет двудолевое строение, но встречается и однодолевое. При однодолевом строении железы, так же, как и при типичном двудолевом, возможно как симметричное, так и асимметричное расположение органа. Асимметрия размеров долей железы при нормальном суммарном объеме органа не имеет принципиального клинического значения.
Бывает и такое распложение железы, что часть ткани может через яремную вырезку смещается на шею, достигая нижнего края щитовидной железы. Это является вариантом возрастной нормы и, при отсутствии других изменений, не должно расцениваться как патология.
Это является вариантом возрастной нормы и, при отсутствии других изменений, не должно расцениваться как патология.
Наиболее частой патологией является ТИМОМЕГАЛИЯ— увеличение объема вилочковой железы без нарушения структуры ткани. Это часто встречается у детей с измененным аллергическим фоном, часто причина тимомегалии и неясна. Клиническое значение тимомегалии состоит в повышенной настороженности относительно проведения плановых прививок и плановых оперативных вмешательств этим детям.
Возможно так же и уменьшения в размере вилочковой железы, что в дальнейшем требует специального обследования у иммунолога.
Нередко в детском возрасте стали встречаться и различные очаговые образования (кистозного и опухолевидного характера).
Если при ультразвуковом исследовании выявляется очаговое образование в паренхиме вилочковой железы, то необходима консультация онколога.
Ультразвуковой метод диагностики считается первым методом исследования при различный патологических состояниях или при их подозрении со стороны вилочковой железы у детей младшего возраста.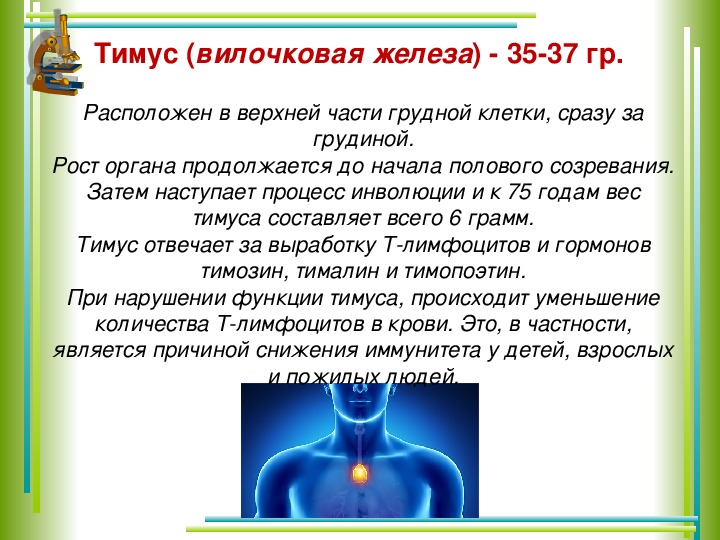
Автор: врач УЗИ Саркисова Н.Л.
Выброшенная ткань тимуса обеспечивает жизнь младенцам с синдромом ДиДжорджи — ScienceDaily
Дюрхэм, Северная Каролина — Используя ткань тимуса, которая обычно выбрасывается после детской операции на сердце, врачи Медицинского центра Университета Дьюка создали новую Т-клеточную иммунную систему для двух детей. кто иначе умер бы.
Дети страдали синдромом Ди Джорджи, редким заболеванием, характеризующимся либо дефектом вилочковой железы, либо отсутствием вилочковой железы вообще, как в случае этих двух детей.Чтобы помочь им, врачи имплантировали тонкие полоски ткани вилочковой железы им в бедра, когда они были младенцами. Детям сейчас полтора и шесть лет, и их новая железа обеспечивает нормально функционирующую иммунную систему, которая не требует долгосрочной лекарственной поддержки или клинической помощи, сообщили исследователи в выпуске журнала New England Journal of за 14 октября. Медицина.
Исследователи заявили, что даже несмотря на то, что ткань была имплантирована от неродственного донора, она не может быть отвергнута у пациентов, у которых отсутствует вилочковая железа, потому что именно вилочковая железа производит иммунные клетки, которые отторгают чужеродную ткань. После процедуры трансплантации новая донорская ткань вилочковой железы в бедрах этих детей вела себя так же, как их собственный орган вилочковой железы.
После процедуры трансплантации новая донорская ткань вилочковой железы в бедрах этих детей вела себя так же, как их собственный орган вилочковой железы.
«По крайней мере, для этих детей трансплантат был лекарством», — сказала в интервью ведущий исследователь, детский иммунолог доктор Луиза Маркерт. «Ранняя трансплантация тимуса до развития инфекционных осложнений может эффективно восстановить иммунную функцию у этих пациентов.
«Этот метод не только обещает некоторым детям, рожденным без вилочковой железы, он демонстрирует, что медицина теперь способна восстановить иммунную систему тем, у кого он истощен», — сказала она.«Сегодня у нас есть инструменты, позволяющие заставить эту технику работать. Мы можем разрезать ткань тимуса, достаточно тонкую для успешной имплантации, и мы можем точно измерить иммунный ответ».
Трое других детей, которым была пересажена ткань тимуса, позже умерли, сказали исследователи. Двое из них находились на ИВЛ во время лечения, а третьему потребовалась ИВЛ вскоре после трансплантации. По словам Маркерт, у всех у них развилась инфекция в легких, которая не могла вылечиться. Даже в этом случае Т-клеточные ответы наблюдались у двух из трех умерших пациентов.
По словам Маркерт, у всех у них развилась инфекция в легких, которая не могла вылечиться. Даже в этом случае Т-клеточные ответы наблюдались у двух из трех умерших пациентов.
Синдром ДиДжорджи — это в первую очередь генетическое заболевание, которое возникает до рождения и может поражать три органа, которые развиваются в непосредственной близости друг от друга — сердце, вилочковую железу и паращитовидную железу, которая регулирует использование организмом кальция. У детей с диагнозом ДиДжорджи может наблюдаться целый ряд заболеваний, от сердечных заболеваний до нарушения функции тимуса, но Маркерт и ее команда использовали метод трансплантации только для детей, рожденных без ткани вилочковой железы.
«Мы не хотим трансплантировать ткань, которая будет генерировать свои собственные Т-клетки, младенцам, у которых достаточно собственной вилочковой железы, чтобы вступить в битву, которая приведет к отторжению», — сказала она.
Хотя каждый год в США у каждого 2000 детей диагностируется синдром ДиДжорджи различной степени, только от 5 до 10 из них рождаются без вилочковой железы. Это состояние называется «полным синдромом Ди Джорджи». Менее четверти детей с этой тяжелой формой имеют подходящего брата или сестру, который может использоваться в качестве источника донорских Т-клеток, излечивающих болезнь. По ее словам, для оставшихся младенцев не существует долгосрочного лечения, за исключением трансплантации тимуса, которую команда Маркерта выполнила для замены Т-клеточного иммунитета.Несколько предыдущих попыток заменить ткань тимуса у пациентов ДиДжорджи было трудно интерпретировать, потому что, как подозревает Маркерт, лечили младенцев, у которых уже был низкий, но уже существующий уровень иммунной функции, и эти младенцы обычно поправляются без терапии.
Это состояние называется «полным синдромом Ди Джорджи». Менее четверти детей с этой тяжелой формой имеют подходящего брата или сестру, который может использоваться в качестве источника донорских Т-клеток, излечивающих болезнь. По ее словам, для оставшихся младенцев не существует долгосрочного лечения, за исключением трансплантации тимуса, которую команда Маркерта выполнила для замены Т-клеточного иммунитета.Несколько предыдущих попыток заменить ткань тимуса у пациентов ДиДжорджи было трудно интерпретировать, потому что, как подозревает Маркерт, лечили младенцев, у которых уже был низкий, но уже существующий уровень иммунной функции, и эти младенцы обычно поправляются без терапии.
Т-клетки, названные так потому, что они представляют собой иммунные клетки, созревающие в вилочковой железе, состоят из клеток-помощников и клеток-убийц, которые ищут и уничтожают инфицированные клетки в организме. И Т-клетки, и В-клетки, которые представляют собой специализированные иммунные клетки, вырабатывающие антитела, сигнализирующие о наличии инфекции, работают вместе, чтобы защитить человека от вирусов, бактерий и других патогенов. По словам Маркерта, без Т-клеток инфекция, которая мало повлияет на здорового человека, может быть смертельной.
По словам Маркерта, без Т-клеток инфекция, которая мало повлияет на здорового человека, может быть смертельной.
Маркерт впервые попробовал эту технику в 1993 году, когда позвонила семья из Теннесси, надеясь на помощь своему ребенку. Под руководством соавторов доктора Ребекки Бакли, иммунолога, первопроходца в лечении детей с ТКИН (тяжелый комбинированный иммунодефицит), и доктора Бартона Хейнса, эксперта по функции тимуса, Маркерт извлек кусок ткани вилочковой железы размером с большой палец, который был бы отброшен после детской кардиохирургии.Затем, как всегда, Маркерт попросил родителей ребенка, перенесшего операцию по устранению проблемы с сердцем, для разрешения использовать ткань. Когда ребенок рождается, вилочковая железа практически покрывает его сердце. «Она располагается наверху сердца и спускается каскадом вниз. А поскольку орган такой большой, большинство операций на сердце младенца приводят к удалению части железы», — сказала она. Маркерт берет от 2 до 10 граммов ткани обратно в лабораторию, тонко нарезает ее и культивирует до двух недель — достаточно долго, чтобы разрушить большинство зрелых Т-клеток в железе.
Все, что ей нужно для трансплантации, — это эпителиальные клетки железы, функция которых состоит в том, чтобы «обучать» незрелые Т-клетки, которые отправляются в тимус после того, как стволовые клетки костного мозга производят их. «Эти незрелые Т-клетки попадают в тимус для обучения», — говорит она. «Это как в школу. Требуется около трех месяцев, чтобы узнать, какие клетки принадлежат человеку, а какие нет».
Поскольку молодая ткань тимуса наиболее активна, Markert использует только донорскую ткань тимуса от детей, перенесших операцию, в возрасте до 3 месяцев.
После того, как тимус достаточно долго находится в культуре и образцы крови ребенка-донора собраны и проверены на наличие инфекций, к работе приступают детские хирурги. Они кладут полоски вилочковой железы рядом, «как бекон на сковороде», глубоко в мышцу бедра ребенка ДиДжорджи. «Это самая большая мышца в их маленьких телах, а кровеносные сосуды в мышце бедра превращаются в полоски вилочковой железы, питают их и омолаживают», — сказала она. Это произошло с четырьмя младенцами ДиДжорджи.У выживших младенцев последующая биопсия показала нормальную ткань тимуса в мышце бедра.
По словам Маркерта, с возрастом вилочковая железа сжимается, и ее становится трудно найти рядом с сердцем. Это потому, что Т-клетки, уже образованные железой, предназначены для обеспечения пожизненного иммунитета путем постоянного деления. Но можно адаптировать эту технику трансплантации к взрослым, чья иммунная система полностью лишена Т-клеток, например тем, кому была сделана трансплантация пуповинной крови для лечения рака — процедура, которая иногда может повредить иммунную систему пациента. и у пациентов с ВИЧ, у которых не развиваются Т-лимфоциты, несмотря на терапию.
Исследование, которое длилось семь лет, финансировалось за счет грантов Национальных институтов здравоохранения, Фонда Макса Кейда и Centeon Pharmaceutics.
Также вместе с Маркертом, Хейнсом и Бакли над исследованием работали врачи и исследователи Duke доктор Сэмюэл Махаффи, доктор Андреас Бок, доктор Лаура Хейл, Эми Клостер, Таня Маклафлин, Милена Батварова, доктор Дэниел Доук, доктор Ричард Куп. , Доктор Донна Костю, доктор Фрэнсис Уорд, Шерри Шифф и доктор Генри Райс.
Младенцы с синдромом ДиДжорджи, спасенные благодаря иммуносупрессии, трансплантации тимуса
Луиза Маркерт, М.Н., К.э.н. Полноразмерное изображение доступно через контакт |
Дюрхэм, Северная Каролина — Исследователи из Медицинского центра Университета Дьюка разработали комбинированную технику подавления иммунитета и трансплантации тимуса, чтобы спасти младенцев, рожденных с полным синдромом ДиДжорджи, смертельным генетическим заболеванием.
У младенцев с полным синдромом ДиДжорджи нет вилочковой железы, железы, важной для созревания Т-клеток — специализированных иммунных клеток, которые помогают защитить организм от вирусов, бактерий и других патогенов.Тимус учит Т-клетки бороться с инфекциями, не поражая собственные ткани ребенка.
Duke — единственный центр, предлагающий трансплантацию тимуса как лекарство от иммунного дефекта. Без этого лечения младенцы с полным синдромом ДиДжорджи не смогут бороться с инфекциями и умрут.
До недавнего времени некоторые младенцы с полным диагнозом ДиДжорджи не могли получить трансплантат тимуса, потому что некоторые из их клеток костного мозга спонтанно трансформировались в ложные Т-клетки.Эти Т-клетки атакуют как собственные ткани организма, так и чужеродные ткани, поэтому трансплантаты тимуса будут отвергнуты.
Основываясь на 12-летнем опыте лечения синдрома Ди Джорджи, Луиза Маркер, доктор медицинских наук, доцент педиатрии в Медицинском центре Университета Дьюка, и ее коллеги обнаружили, что подавление ложных Т-клеток с помощью иммунодепрессанта в течение трех дней непосредственно перед операцией по трансплантации привели к успешной трансплантации тимуса. Пятеро из шести младенцев, перенесших новую процедуру, выжили и теперь живут дома; один скончался от ранее существовавшей респираторной инфекции.«Это действительно работает для этой группы населения», — сказал Маркерт. «Это все еще экспериментально, но сейчас это лучший вариант».
Иммунодепрессант, тимоглобулин, нацелен только на Т-клетки, сказал Маркерт. «Он менее эффективен, чем любая другая химиотерапия. Нам действительно нужно убить только Т-клетки, и достаточно времени для трансплантации», — сказала она.
Метод трансплантации и результаты лечения шести младенцев с синдромом ДиДжорджи появятся в октябре.15, 2004, печатный выпуск журнала Blood и доступны в Интернете на веб-сайте журнала http://www.bloodjournal.org. Исследование финансировалось Национальным институтом здравоохранения.
Не каждому ребенку, рожденному с синдромом ДиДжорджи, потребуется пересадка тимуса. Более легкие формы заболевания встречаются примерно у одного ребенка из 4000. Из них только один из 250 детей — от пяти до десяти ежегодно в США — будет иметь полный синдром ДиДжорджи с отсутствием вилочковой железы.
Заболевание часто первоначально диагностируется путем выявления врожденных дефектов, характерных для полного ДиДжорджи, включая аномалии сердца, низкий уровень кальция из-за отсутствия паращитовидной железы, дефекты пищевода и лицевые аномалии, такие как низко посаженные уши, широко посаженные глаза и маленькие челюсть. Расстройство может возникать спонтанно или передаваться по наследству. Менее чем в половине случаев у младенцев с полным синдромом ДиДжорджи будет дефект 22-й хромосомы.
Маркер отмечает, что полный диагноз ДиДжорджи был упущен во многих случаях, потому что генетическое тестирование дефекта на хромосоме 22 дает нормальный результат, несмотря на наличие характерных врожденных дефектов.Это вводящее в заблуждение открытие может отсрочить лечение, подвергая младенца риску серьезной инфекции.
Идеальное время для трансплантации ткани вилочковой железы — три месяца после рождения, сказал Маркерт. «Главное — сделать это до того, как разовьются инфекции», — сказала она.
Ткань вилочковой железы для трансплантации происходит из ткани, которая в противном случае была бы выброшена во время кардиохирургических операций на младенцах-донорах в возрасте до шести месяцев. Поскольку характерно большая вилочковая железа младенца часто препятствует доступу к сердцу, во многих операциях хирурги должны удалять части вилочковой железы, чтобы получить доступ к сердцу.Родители младенцев-доноров соглашаются передать выброшенные ткани для трансплантации. Клиницисты культивируют донорскую ткань в течение двух недель, одновременно выполняя тестирование, чтобы гарантировать, что никакие заболевания не передаются с трансплантированной тканью тимуса.
Детские хирурги, работающие с Маркертом, трансплантируют тонкие полоски донорской ткани тимуса в бедренную мышцу младенца-реципиента, где, скорее всего, образуется сеть кровеносных сосудов, доставляющих питание и кислород. После трансплантации незрелые белые кровяные клетки из костного мозга ребенка мигрируют в ткань тимуса, где они обучаются различать микробы и собственные клетки организма.Примерно через три или четыре месяца после трансплантации появляются зрелые Т-клетки — последний шаг к функционированию иммунной системы.
Реципиенты трансплантата остаются в изоляторах больницы Дьюка, либо в педиатрическом отделении, либо в Общем клиническом исследовательском центре Дьюка, финансируемом Национальным центром исследовательских ресурсов Национальных институтов здравоохранения. Такая изоляция помогает предотвратить развитие инфекций у младенца до того, как сформируются зрелые Т-клетки.
На данный момент Маркерт выполнил трансплантацию тимуса 26 младенцам с полным синдромом ДиДжорджи, включая шестерых, получивших новое иммуносупрессивное лечение.«Я узнаю кое-что от каждого из них, что улучшит лечение следующего пациента», — сказала она.
Соавторы исследования: коллеги из Герцога Мэрилин Алексиефф; Джи Ли; Марселла Сарзотти, доктор философии; Даниэль Одзаки; Блайт Девлин; Дебра Седлак; Грегори Семповски, доктор философии; Лаура Хейл, доктор медицины; Генри Райс, доктор медицины; Самуэль Махаффи, доктор медицины; и Майкл Скиннер, доктор медицины
###
Заявление об ограничении ответственности: AAAS и EurekAlert! не несут ответственности за точность выпусков новостей, размещенных на EurekAlert! участвующими учреждениями или для использования любой информации через систему EurekAlert.
Размер тимуса и его корреляты среди детей, поступивших с тяжелым острым недоеданием: перекрестное исследование в Уганде | BMC Pediatrics
Дизайн и условия исследования
Это было перекрестное исследование, которое было частью рандомизированного контролируемого исследования, оценивающего влияние пробиотиков на диарею среди детей, поступивших с SAM; зарегистрирован на сайте www.isrctn.com (ISRCTN16454889) и результаты которого были опубликованы [16]. Пациентов набирали в течение 18 месяцев, начиная с марта 2014 г.Исследование проводилось в отделении питания Мванамугиму (MNU), расположенном в Национальной специализированной больнице Мулаго, большой учебной больнице на 1500 коек в Кампале, Уганда. Отделение принимает около 120 детей с тяжелой формой истощения в месяц на стационарную терапевтическую помощь, а также обеспечивает амбулаторную диетическую реабилитацию в клинике амбулаторной терапевтической помощи (ОТК) MNU.
Критерии отбора
Мы включили детей в возрасте 6–59 месяцев, поступивших с SAM в MNU и чьи опекуны дали согласие на участие в исследовании.SAM определялся как окружность середины плеча (MUAC) <11,5 см или Z-оценка массы тела к росту (WHZ) <-3 SD или двуногий отек с ямками. В рамках рандомизированного контролируемого исследования мы исключили пациентов с тяжелыми состояниями, такими как шок, тяжелая респираторная недостаточность при поступлении, с массой тела менее 4,0 кг и очевидной инвалидностью, чья реакция на диетологическую реабилитацию обычно затруднена. Мы также включили 30 практически здоровых детей из того же социального статуса, возрастной группы и сообществ, что и пациенты с SAM, но чьи WHZ были> -1.Они были выбраны для обеспечения эталонного размера вилочковой железы для детей, не страдающих от недостаточного питания в тех же условиях.
Сбор данных
Детей, которые соответствовали критериям отбора в течение периода исследования, последовательно зачисляли до тех пор, пока не был достигнут требуемый размер выборки. После предоставления письменного информированного согласия педиатр-исследователь или медицинский работник заполнял анкету при зачислении. Анкета включала анамнез с акцентом на демографические данные, описание имеющихся симптомов, медицинский осмотр и диагноз.На следующий день был взят более подробный диетический и социально-экономический анамнез. В рамках медицинского осмотра диетологи трижды провели антропометрические измерения и взяли среднее значение. Длину или рост измеряли с помощью доски для измерения длины ребенка (Infant / Child Shorr-Board®, Мэриленд, США) и MUAC с помощью измерительной ленты с точностью до 1 мм. Вес тела измеряли с помощью цифровых весов (Seca 813 Hamburg, Германия) с точностью до 0,1 кг. WHZ рассчитывались с использованием Стандартов роста детей Всемирной организации здравоохранения (ВОЗ) [17].Здоровые контрольные были подвергнуты тем же анкетам и тестам, что и дети с SAM. Лечение детей с SAM было начато в соответствии с рекомендациями Интегрированного лечения острого недоедания (IMAM) [18], но переход на другой корм осуществлялся в соответствии с рекомендациями ВОЗ [19].
Анализы крови
Четыре мл крови были взяты из венепунктов в гепаринизированные вакуумные пробирки (Becton Dickinson, Franklin Lakes, NJ USA). Образцы для полного анализа крови анализировали с использованием счетчика Коултера и выражали в количестве клеток на кубический миллиметр (клеток / мм 90 · 103 3 90 · 104).Серологическое тестирование на ВИЧ проводилось с помощью экспресс-тестов (Determine HIV-1/2 от Abbott Laboratories, США), а положительные образцы были подтверждены с помощью набора для анализа на ВИЧ 1/2 Stat-Pak Dipstick (Chembio Diagnostic systems, INC, США). Все дети в возрасте до 18 месяцев, у которых был положительный серологический тест, были отправлены на анализ ДНК / ПЦР на ВИЧ в больничной клинике по борьбе с ВИЧ. Плазму получали центрифугированием при 1300–2200 G в течение 10 минут, затем хранили при -80 o ° C до отправки на сухом льду в Копенгагенский университет, Департамент питания, физических упражнений и спорта, Дания.С-реактивный белок (CRP) плазмы измеряли с помощью высокочувствительного набора на ABX Pentra 400 (Horiba, Montpellier, France).
Измерение вилочковой железы
Зависимой переменной был размер вилочковой железы, измеренный с помощью ультразвукового сканирования. Ультразвуковое сканирование вилочковой железы было выполнено на второй день приема одним из двух педиатров, участвовавших в исследовании, которые прошли обучение до начала исследования.
Сканирование проводилось в отделении MNU на хорошо отгороженной кровати, чтобы обеспечить темноту для лучшей видимости.Во время процедуры пытались успокоить детей. Использовали ультразвуковой сканер (SonoScape A6 Guangdong, Китай) с детским абдоминальным зондом (изогнутый). Процедура выполнялась, когда ребенок лежал на спине или на коленях матери, как показано на рис. 1.
Рис. 1Положение для ультразвукового сканирования (исходное изображение)
Сагиттальная область была получена путем размещения датчика под углом 90 градусов к верхней части грудины, где тимус визуализировался как имеющий однородную эхогенность, подобную эхогенности печени и селезенки, как показано на рис.2. Отслеживали окружность самой большой доли вилочковой железы и записывали измерение площади. Все измерения были выполнены в двух экземплярах, и использовалось среднее значение двух измерений. Один исследователь (NNB) выполнил около 96% сканирований.
Рис. 2Ультразвуковое сканирование ребенка с SAM
Размер выборки 400 был рассчитан для рандомизированного контролируемого исследования, на основании которого было проведено это исследование.
Анализ данных
Данные были дважды введены в EpiData v.3.1 (EpiData, Оденсе, Дания) и проанализированы с использованием STATA версии 2 (Колледж Стейшн, Техас, США).Средние и медианы были рассчитаны для непрерывных переменных. Были составлены перекрестные таблицы, и критерий хи-квадрат использовался для категориальных переменных, а t-критерий — для сравнения средних значений между детьми с SAM и здоровыми людьми из контрольной группы. У одного ребенка с SAM был аномально большой тимус 5,11 см 2 , и он был исключен из анализа, так как у него предполагалось лимфома. У троих детей с невидимым тимусом была выделена половина наименьшего видимого размера вилочковой железы, и они были включены в анализ.Из анализа были исключены 11 детей с SAM и 3 референтных ребенка из сообщества, которые пропустили ультразвуковое сканирование. Модель линейной регрессии использовалась для определения факторов, связанных с размером тимуса у детей с SAM. Сначала был проведен одномерный анализ коррелятов размера тимуса, затем каждая переменная контролировалась по возрасту и полу. Те, у кого значение p <0,05, считались статистически значимыми.
Произошла ошибка при настройке вашего пользовательского файла cookie
Произошла ошибка при настройке вашего пользовательского файла cookieЭтот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Произошла ошибка при настройке вашего пользовательского файла cookie
Произошла ошибка при настройке вашего пользовательского файла cookieЭтот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie.Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie.Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
У моего маленького сына увеличена вилочковая железа
Вопрос
Моему маленькому сыну, которому сейчас 16 месяцев, в четыре месяца поставили диагноз: увеличенная вилочковая железа.
За этим последовала серия «синих поворотов», когда он терял дыхание и окрашивал губы в синий оттенок.
Ему сделали компьютерную томографию и частые ультразвуковые исследования грудной клетки, и он будет находиться под наблюдением до двух лет.
Наш семейный врач признал, что у него очень мало знаний по этому вопросу, и нам было интересно, не могли бы вы рассказать нам, как эта проблема может повлиять на нашего сына, когда он станет старше и активнее.
Мы не совсем понимаем роль вилочковой железы в организме.
Ответ
Вилочковая железа — это мягкий сплюснутый розовато-серый орган, расположенный в верхней части грудной клетки под грудиной.
Он относительно велик у новорожденного (размером с кулак ребенка) и продолжает расти в детстве до полового созревания, после чего постепенно уменьшается в размерах.
Тимус играет жизненно важную роль в защите иммунной системы организма от вторжения чужеродных организмов.
Если вилочковая железа не развивается, пока ребенок еще находится в утробе матери, иммунная система не может нормально функционировать.
Когда у вашего сына были «синие повороты» и исследования показали, что у него увеличена вилочковая железа, врачи, наблюдающие за ним, возможно, задавались вопросом, давит ли эта железа на его трахею и вызывает ли какие-то затруднения с дыханием.
Не зная подробностей случая вашего сына, трудно сказать, как увеличенная вилочковая железа может повлиять на него, когда он станет старше.
Но для вас важно понимать, как его состояние повлияет на него, так почему бы вам не попросить поговорить со специалистом, который ухаживает за ним, или с одним из врачей в его команде, когда вы в следующий раз пойдете в клинику? больница?
Они смогут ответить на ваши вопросы, и, надеюсь, это успокоит вас.
С уважением
Медицинская бригада NetDoctor
Последнее обновление
Этот контент создается и поддерживается третьей стороной и импортируется на эту страницу, чтобы помочь пользователям указать свои адреса электронной почты. Вы можете найти больше информации об этом и подобном контенте на сайте piano.io.
Смещение ларинго-трахеи и респираторный дистресс у ребенка с врожденной гиперплазией тимуса
Гиперплазия тимуса обычно является бессимптомным состоянием, наблюдаемым в младенчестве.Пятинедельный мальчик поступил с респираторным дистресс-синдромом и нарушением питания, при котором рентгенография грудной клетки и бронхоскопия показали сильное смещение гортани и трахеи. Сонография и МРТ подтвердили диагноз гиперплазия тимуса. Кортикостероидная терапия привела к улучшению клинических симптомов. Гиперплазия тимуса может привести к ларинго-трахеальному смещению и респираторной недостаточности у новорожденных и детей младшего возраста.
1. Введение
Хотя увеличение тимуса — обычное и физиологическое обнаружение на рентгеновских снимках детей и новорожденных, симптоматическая гиперплазия — очень редкое состояние.Помимо рентгена, для подтверждения диагноза в сложных случаях использовались УЗИ, КТ и МРТ [1, 2]. Методы лечения симптоматических пациентов все еще противоречивы, а кортикостероидная терапия симптоматической гиперплазии тимуса пока не доказала свою эффективность [3]. Этот отчет представляет собой уникальный случай симптоматической гиперплазии тимуса и сильного ларинго-трахеального отклонения, продемонстрированного рентгенологическим исследованием грудной клетки и бронхоскопией, который можно успешно лечить кортикостероидами.
2. История болезни
Мы сообщаем о пятинедельном младенце, поступившем в нашу больницу с историей инспираторного стридора и расстройства кормления с рождения. Беременность и роды прошли без осложнений. Клиническое обследование не показало, кроме инспираторного стридора, одышки и тахипноэ, других патологий нет. Анализ крови показал нормальный анализ крови, электролиты, показатели функции печени и почек и свертываемость крови. Газы крови и сатурация кислорода тоже были в норме. Первоначальный рентгеновский снимок, показанный на рисунке 1 (а), показал значительное смещение трахеи влево из-за большой массы в верхнем грудном отверстии.На УЗИ поставлен предположительный диагноз гиперплазия тимуса. Во время вдоха вилочковая железа двигалась краниально, что сопровождалось инспираторным стридором. Увеличение щитовидной железы или лимфатических узлов не обнаружено. Дополнительная МРТ подтвердила объемное поражение в верхнем грудном отверстии с плотностью, аналогичной ткани тимуса, и максимальной шириной 3,2 см (рис. 1 (b)). Трахея не была сужена (рис. 1 (в)). Бронхоскопия показала сильный изгиб гортани и трахеи влево, но никаких других аномалий.
Поскольку у ребенка сохранялась респираторная недостаточность и его было трудно кормить, мы решили провести терапию кортикостероидами. Мы начали терапию метилпреднизолоном 4 мг / кг в течение одной недели (вес ребенка 4,5 кг), постепенно снижали и прекращали через четыре недели, последняя доза составляла 1 мг 1 раз в сутки. Побочных эффектов кортикостероидов в виде гипертонии, глюкозурии и электролитных нарушений не наблюдалось. Клинически инспираторный стридор, тахидиспное расстройство и нарушение питания исчезли через четыре дня лечения.Через два месяца после обращения мы выполнили второй рентген грудной клетки (рис. 1 (d)), показавший анатомически нормальную трахею без смещения или обструкции трахеи. Сонографически также было четкое уменьшение ткани тимуса. При клиническом наблюдении у ребенка не было рецидивов симптомов через 1, 2 и 7 месяцев после терапии.
3. Обсуждение
Хотя увеличение тимуса является частым и физиологическим признаком рентгеновских снимков детей и новорожденных, симптоматическая гиперплазия — очень редкое состояние.Состояние истинной гиперплазии тимуса определяется как увеличение размера и веса железы при сохранении нормальной микроскопической архитектуры. Существуют три разные формы. Во-первых, истинная гиперплазия тимуса без какого-либо основного заболевания, во-вторых, как форма феномена отскока, вызванного стероидной терапией, химиотерапией, лечением гормоном роста или тяжелым стрессом, и в-третьих, связанная с эндокринными аномалиями, саркоидозом, миастенией (MG) и синдромом Беквита-Видемана ( BWS) [4].
Большинство опухолей средостения в педиатрической популяции имеют нейрогенное происхождение (33%) или лимфомы (41%). Однако первичные поражения тимуса (такие как кисты тимуса, тимолипомы и гиперплазия тимуса) составляют лишь 2,5% опухолей средостения, тогда как тимомы составляют около 1% и обычно имеют агрессивное течение и низкую выживаемость [5]. В нашем случае биопсия не проводилась, потому что возраст и результаты крови, а также морфология МРТ сделали лимфому маловероятной.
Вилочковая железа может иметь непонятную массу, похожую на массу, поскольку ее размер, форма, положение и характер роста изменчивы.Для подтверждения диагноза гиперплазии тимуса и исключения злокачественных новообразований может потребоваться рентген грудной клетки и УЗИ тимуса, а в некоторых случаях также МРТ или КТ [1, 2]. В частности, УЗИ является легкодоступным диагностическим инструментом, который показывает типичную морфологию, а также может продемонстрировать корреляцию инспираторного стридора с краниальным движением гипертрофированного тимуса [1, 2].
Если морфологическая диагностическая визуализация свидетельствует в пользу этого диагноза гиперплазии тимуса, особенно у младенцев с симптомами, можно рассмотреть исследование кортикостероидов и тщательное наблюдение в качестве терапии первой линии [1].Кортикостероиды способны уменьшить объем тимуса и добиться его частичной инволюции и тем самым предотвратить инвазивное хирургическое вмешательство у пациентов с симптомами [3]. Было показано, что краткосрочное и долгосрочное применение кортикостероидов вызывает инволюцию тимуса [6]. Однако текущая литература о возможном благоприятном воздействии кортикостероидов при гиперплазии тимуса все еще остается противоречивой [3]. Некоторые рекомендуют стресс-тест, чтобы помочь в постановке правильного диагноза, поскольку пероральное введение стероидов обычно приводит к инволюции образования тимуса.К сожалению, этот тест не является специфическим, и лимфатические опухоли также будут инволютированы. Кортикостероидная терапия требует длительного наблюдения, поскольку может произойти рецидив гиперплазии тимуса после естественного или ятрогенного избытка стероидов. Через семь месяцев после терапии у нашего пациента не было симптомов.
Операция по-прежнему может потребоваться, когда новообразование увеличивается и может повлиять на развитие легких, или если симптомы невозможно контролировать иным способом. Сообщалось о пациентах, которым потребовалась хирургическая тимэктомия или даже дополнительная легочная лобэктомия или экстренное хирургическое вмешательство при таких состояниях, как кровоточащие внутригрудные кисты тимуса [7].
 Он расположен в верхнем отделе грудной клетки и состоит из двух долей, соединяющихся в передней части трахеи. Железа растет до наступления половой зрелости, достигая массы 30–40 грамм, затем постепенно уменьшается (обратное развитие).
Он расположен в верхнем отделе грудной клетки и состоит из двух долей, соединяющихся в передней части трахеи. Железа растет до наступления половой зрелости, достигая массы 30–40 грамм, затем постепенно уменьшается (обратное развитие).

